-
已知aAn+、bB(n+1)+、cCn-、dD(n+1)-具有相同的电子层结构,关于A、B、C、D四种元素的叙述正确的是( )
A.气态氢化物的稳定性:D>C
B.原子序数:b>a>c>d
C.最高价氧化物对应水化物的碱性:B>A
D.四种元素一定属于短周期元素难度: 中等查看答案及解析
-
对于易燃易爆有毒有腐蚀性的化学物质,往往会在其包装上贴危险警告标签.下图所列物质与危险警告标签对应错误的是( )
A.
浓硫酸
B.
金属汞
C.
四氯化碳
D.
硝酸铵难度: 中等查看答案及解析
-
下列关于化学学习和研究的说法错误的是( )
A.假说是一种推测性说明,属于研究物质性质基本程序的一个必需步骤
B.化学家们已能够在微观层面上操纵分子和原子,组装分子材料、器件等
C.运用分类的方法,可根据物质所属的类别预测物质的性质
D.化学模型有助于解释一些化学现象难度: 中等查看答案及解析
-
3He可以作为核聚变材料,以下关于3He的说法正确的是( )
A.比4He少一个质子
B.比4He多一个中子
C.与4He互为同分异构体
D.与4He互为同位素难度: 中等查看答案及解析
-
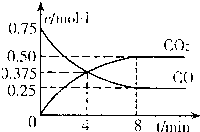
2009年11月,国务院常务会议决定,到2020年我国单位国内生产总值二氧化碳排放比2005年下降40%一45%,作为约束性指标纳入国民经济和社会发展的中长期规划.将CO2转化成有机物可有效实现碳循环.CO2转化成有机物的例子很多,如:
①6CO2+6H2OC6H12O6+6O2
②CO2+3H2CH3OH+H2O
③CO2+CH4CH3COOH
④2CO2+6H2CH2=CH2+4H2O
对以上反应的叙述,正确的是( )
A.最节能的是反应①
B.因为CH3OH有毒,故反应②无应用价值
C.反应③中的两种反应物都是可再生的天然物质
D.反应④是工业生产乙烯的一种主要方法难度: 中等查看答案及解析
-
下列涉及有机物的性质或应用的说法错误的是( )
A.干馏煤可以得到甲烷、苯和氨等重要化工原料
B.石油裂解的主要目的是生产有机化工原料,例如乙烯、丙烯等
C.2CH3CH2OH+O22CH3CHO+2H2O属于氧化反应
D.纤维素、蔗糖、葡萄糖和脂肪在一定条件下都可发生水解反应难度: 中等查看答案及解析
-
如图所示,集气瓶内充满某混合气体,置于光亮处,将滴管内的水挤入集气瓶后,烧杯中的水会进入集气瓶,集气瓶内气体是( )
①H2、O2
②Cl2、CH4
③NO2、O2
④N2、H2.
A.①②③
B.②④
C.③④
D.②③难度: 中等查看答案及解析
-
NA表示阿伏加德罗常数的值.下列叙述正确的是( )
A.33.6L(常温常压)氯气与2.7g铝充分反应,转移电子数为0.3NA
B.标准状况下,22.4L乙烷含有共价键数目为8NA
C.由NA个CO和NA个N2组成的混合物中含有10NA个电子
D.1L lmol•L-1的Na2SO4溶液中含有4NA个离子难度: 中等查看答案及解析
-
下列装置或操作能达到实验目的是( )
A.
构成铜锌原电池
B.
二氧化碳制取装置
C.
利用排空气法收集CO2
D.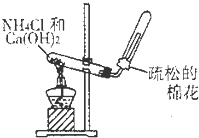
实验室制取并收集氨气难度: 中等查看答案及解析
-
2005年诺贝尔化学奖获得者施罗克等人发现,金属钼的卡宾化合物可以作为非常有效的烯烃复分解催化剂.工业上冶炼钼的化学原理为
①2MoS2+7O22MoO3+4SO2
②MoO3+2NH3•H2O═(NH4)2MoO4+H2O
③(NH4)2MoO4+2HCl═H2MoO4↓+2NH4Cl
④H2MoO4MoO3+H2O
⑤用还原剂将MoO3还原成金属钼.则下列说法正确的是( )
A.反应①和⑤都属于置换反应
B.MoO3属于碱性氧化物
C.在反应①中Mo和S均被氧化
D.利用H2、CO和铝分别还原等量的MoO3,所消耗还原剂的物质的量之比为2:2:3难度: 中等查看答案及解析
-
下列离子方程式正确的是( )
A.Fe(NO3)3溶液中加入过量的HI(强酸)溶液:2Fe3++2I-═2Fe2++I2
B.用惰性电极电解硫酸铜溶液:2Cu2++2H2O2H2↑+2Cu+O2↑
C.碳酸钡与稀硫酸反应:BaCO3+H2SO4═BaSO4+H2O+CO2↑
D.Na2SO3溶液使酸性KMnO4溶液褪色:5SO32-+6H++2MnO4-═5SO42-+2Mn2++3H2O难度: 中等查看答案及解析
-
关于小苏打水溶液的表述正确的是( )
A.HCO3-的电离程度大于HCO3-的水解程度
B.c(Na+)=c(HCO3-)+c(CO32-)+c(H2CO3)
C.c(Na+)+c(H+)=c(HCO3-)+c(CO32-)+c(OH-)
D.存在的电离有:NaHCO3═Na++HCO3-,HCO3-⇌H++CO32-,H2O⇌H++OH-,HCO3-+H2O⇌H2CO3+OH-难度: 中等查看答案及解析
-
为提纯下列物质(括号内的物质是杂质),所选用的除杂试剂和分离方法都正确的( )
被提纯的物质 除杂试剂 分离方法 A NaBr溶液(NaI) 氯水、CCl4 萃取、分液 B NH2Cl溶液(FeCl3) NaOH溶液 过滤 C CO2(CO) CuO粉末 通过灼热的CuO粉末 D SiO2(Al2O3) NaOH溶液 过滤
A.A
B.B
C.C
D.D难度: 中等查看答案及解析
-
有①Na2CO3溶液②CH3COONa溶液 ③NaOH溶液 ④CH3COONH4溶液各25mL.物质的量浓度均为0.1mol•L-1,下列说法正确的是
( )
A.四种溶液的pH大小顺序是③>②>①>④
B.若分别加入25mL 0.1mol•L-1盐酸充分反应后,pH最大的是①
C.若将四种溶液稀释相同倍数,pH变化最大的是④
D.升高温度,四种溶液的pH均减小难度: 中等查看答案及解析
-
某同学按如图所示的装置进行实验. A、B为两种常见金属,它们的硫酸盐可溶于水.当 K 闭合时,在交换膜处 SO42一从右向左移动.下列分析正确的是( )

A.溶液中c(A2+)减小
B.B的电极反应:B→B2++2e-
C.y电极上有H2产生,发生还原反应
D.反应初期,x电极周围出现白色胶状沉淀,不久沉淀溶解难度: 中等查看答案及解析
-
在恒温、恒压下,a mol A和b molB在一个容积可变的容器中发生反应:A(g)+2B(g)⇌2C(g),一段时间后达到平衡,生成n mol C.则下列说法中正确的是( )
A.物质A、B的转化率之比为l:2
B.起始时刻和达到平衡后容器中的压强之比为(a+b):(a+b-)
C.当2v正(A)=v逆(B)时,反应一定达到平衡状态
D.充入惰性气体(如Ar),平衡向正反应方向移动难度: 中等查看答案及解析