-
下列气体中,直接排放到大气而不会产生污染的是
A.NO B.O3 C.CH4 D.CO2
难度: 中等查看答案及解析
-
在化合物A2B和BC2中,B的质量分数分别约为20%和30%,则在化合物A2BC3中B的质量分数最接近
A.5% B.10% C.15% D.20%
难度: 中等查看答案及解析
-
亚碘酸钠的化学式为
A.NaI B.NaIO C.NaIO2 D.NaIO3
难度: 简单查看答案及解析
-
下列物质:①氢氟酸;②浓H2SO4;③烧碱溶液;④Na2CO3固体;⑤氧化钙;⑥浓HNO3,其中在一定条件下能与SiO2反应的有
A.①③④⑤ B.全部 C.①②⑥ D.②③⑥
难度: 简单查看答案及解析
-
将CO2,NO2,NO,SO2分别通过NaOH溶液,不能被吸收的气体
A.NO2 B.NO C.CO2 D.SO2
难度: 简单查看答案及解析
-
下列叙述错误的是
A.氨与酸反应生成铵盐 B.氨气与氯化氢气体相遇产生白烟
C.氨水中滴入酚酞溶液显红色 D.氨使湿润的蓝色石蕊试纸变红
难度: 简单查看答案及解析
-
某无色溶液能与铝作用放出氢气,该溶液中可能大量共存的是
A.Na+、Cu2+、Cl-、SO42- B.K+、CO32-、OH-、Cl-
C.H+、Ba2+、NO3-、Cl- D.K+、Mg2+、Cl-、SO32-
难度: 简单查看答案及解析
-
往100mL3mol/L的稀硝酸中加入一定量的铁铜混合粉末,充分反应后过滤,再往滤渣中滴入稀盐酸,发现有氢气产生,则滤液中
A.一定含Fe2+、不含Fe3+和Cu2+ B.含Fe2+、不含Cu2+、可能含Fe3+
C.可能含Fe2+、Fe3+和Cu2+ D.可能含Fe3+和Cu2+、不含Fe2+
难度: 简单查看答案及解析
-
下列反应的离子方程式书写正确的是
A.氯化钙溶液中通入二氧化碳气体:Ca2++CO2+H2O=CaCO3↓+2H+
B.次氯酸钙溶液中通人少量SO2气体:Ca2++2ClO一+SO2+H2O=CaSO3↓+2HClO
C.醋酸和碳酸氢钠溶液混合:CH3COOH+HCO3-=CO2↑+H2O+CH3COO-
D.碳酸氢镁溶液中加入过量石灰水:
Mg2++2HCO
+Ca2++2OH-==CaCO3↓+2H2O+MgCO3↓
难度: 简单查看答案及解析
-
将7g炭粉与14g氧气在一定条件下完全反生成21g氧化物,则生成物中CO与CO2的物质的量之比为
A.1:1 B.2:1 C.2:3 D.3:1
难度: 简单查看答案及解析
-
将0.4gNaOH和1.06g
混合并配成溶液,向溶液中滴加0.1mol·
稀盐酸。下列图像能正确表示加入盐酸的体积和生成
的物质的量的关系的是
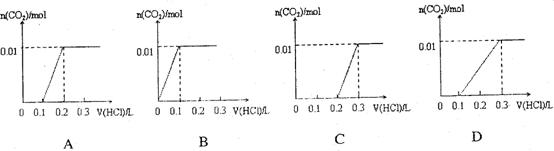
难度: 简单查看答案及解析
-
氯气和水反应生成HCl和HClO,欲从反应混合物中分离出HClO溶液,下列方法可选用的是
A.加硫酸钙,充分反应后蒸馏 B.加碳酸钙,充分反应后蒸馏
C.加氢氧化钙,充分反应后蒸馏 D.加氯化钙,充分反应后蒸馏
难度: 简单查看答案及解析
-
老师做了一个如图所示的实验,发现烧杯中酸性KMnO4溶液褪色。若将烧杯中的溶液换成含有少量KSCN的FeCl2溶液,溶液显红色。则该条件下
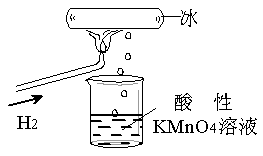
A.生成的水分子化学性质比较活泼
B.H2燃烧生成了具有氧化性的物质
C.H2燃烧的产物中可能含有一定量的H2O2
D.H2被冷却为液态氢,液氢的水溶液具有还原性
难度: 简单查看答案及解析
-
把V L含有MgS04和K2S04的混合溶液分成两等份,一份加入含a mol NaOH的溶液,恰好使镁离子完全沉淀为氢氧化镁;另一份加入含b mol BaCl2的溶液,恰好使硫酸根离子完全沉淀为硫酸钡。则原混合溶液中钾离子的浓度为
A.
mol·L-1 B.
mol·L-1
C.
mol·L-1 D.
mol·L-1
难度: 简单查看答案及解析