-
(6分)已知Cl2在70℃的NaOH溶液中,能同时发生两个反应:
Cl2 + 2NaOH = NaCl + NaClO + H2O;3Cl2 + 6NaOH = 5NaCl + NaClO3 + 3H2O
反应完后,测得溶液中NaClO和NaClO3的物质的量之比为4∶1。现有49.7g Cl2,将其通入到足量的70℃的NaOH溶液中,充分反应后得500mL溶液。计算完全反应后各生成物的物质的量浓度(不计算水的量)。
高三化学计算题简单题查看答案及解析
-
Cl2在70℃的NaOH溶液中,能同时发生两个自身氧化还原反应,反应完全后测得溶液中NaClO与NaClO3物质的量之比为4:1,溶液中NaCl与NaClO的物质的量之比为( )
A.11:2 B.1:1 C.9:4 D.5:1
高三化学单选题简单题查看答案及解析
-
Cl2在70℃的NaOH水溶液中,能同时发生两个自身氧化还原反应,反应完全后测得溶液中NaClO和NaClO3的物质的量比为4∶1,则溶液中NaCl和NaClO的物质的量之比为:
A.9∶4 B.5∶1 C.11∶2 D.1∶1 ( )
高三化学选择题中等难度题查看答案及解析
-
已知 Cl2+2NaOH═NaCl+NaClO+H2O,现有瓶NaOH溶液,质量分数为14%( 其密度为1.14g/ml)则这种溶液______升能与2.24升(标况下)Cl2恰好完全反应.
高三化学解答题中等难度题查看答案及解析
-
常温下,将一定量的氯气通入100mL 4mol/L的氢氧化钠溶液中,发生反应的化学方程式为:Cl2+2NaOH=NaCl+NaClO+H2O.充分反应后,下列说法正确的是(NA为阿伏加德罗常数)( )
A.当通入的Cl2为2.24 L时,反应中电子转移数目为0.1 NA
B.当溶液中Na+为0.4 NA时,溶液中的Cl﹣为0.2 NA
C.当电子转移数目为0.2 NA时,溶液质量增加7.1 g
D.当溶液质量增加7.1 g时,溶液中ClO﹣约为0.1 NA
高三化学选择题简单题查看答案及解析
-
常温下,将一定量的氯气通入100 mL 4 mol/L的氢氧化钠溶液中,发生反应的化学方程式为:Cl2+2NaOH → NaCl+NaClO+H2O。充分反应后,下列说法正确的是(NA为阿伏加德罗常数)
A.当通入的Cl2为2.24 L时,反应中电子转移数目为0.1 NA
B.当溶液中Na+为0.4 NA时,溶液中的Cl-为0.2 NA
C.当电子转移数目为0.2 NA时,溶液质量增加14.2 g
D.当溶液质量增加7.1 g时,溶液中ClO-为0.1 NA
高三化学单选题中等难度题查看答案及解析
-
常温下,将一定量的氯气通入100 mL 4 mol/L的氢氧化钠溶液中,发生反应的化学方程式为:Cl2+2NaOH → NaCl+NaClO+H2O。充分反应后,下列说法正确的是(NA为阿伏加德罗常数)
A.当通入的Cl2为2.24 L时,反应中电子转移数目为0.1 NA
B.当溶液中Na+为0.4 NA时,溶液中的Cl-为0.2 NA
C.当电子转移数目为0.2 NA时,溶液质量增加14.2 g
D.当溶液质量增加7.1 g时,溶液中ClO-为0.1 NA
高三化学选择题困难题查看答案及解析
-
常温下,将一定量的氯气通入100mL4mol·L-1的氢氧化钠溶液中,发生反应的化学方程式为:Cl2+2NaOH=NaCl+NaClO+H2O。充分反应后,下列说法正确的是(NA为阿伏加德罗常数)( )
A.当通入的Cl2为2.24L时,反应中电子转移数目为0.1NA
B.当电子转移数目为0.2NA时,溶液质量增加14.2g
C.当溶液中Na+为0.4NA时,溶液中的Cl-为0.2NA
D.当溶液质量增加7.1g时,溶液中ClO-为0.1NA
高三化学单选题中等难度题查看答案及解析
-
常温下,将一定量的氯气通入100mL4mol/L的氢氧化钠溶液中,发生反应的化学方程式为:Cl2+2NaOH→NaCl+NaClO+H2O。充分反应后,下列说法正确的是(NA为阿伏伽德罗常数)( )
A.当通入的Cl2为22.4L时,反应中电子转移数目为0.1NA
B.当溶液中Na+为0.4NA时,溶液中的Cl-一定为0.2mol
C.当电子转移数目为0.2NA时,生成NaCl0.2mol
D.当溶液质量增加7.1g时,溶液中Na+增加0.2NA
高三化学单选题中等难度题查看答案及解析
-
某研究性学习小组欲利用下列装置制取少量次氯酸钠,并进一步探究次氯酸钠的化学性质。
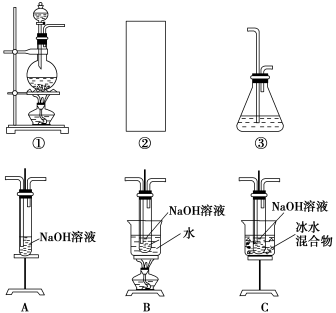
相关资料:反应Cl2+2NaOH=NaClO+NaCl+H2O属于放热反应,温度稍高时便发生副反应3Cl2+6NaOH=NaClO3+5NaCl+3H2O。
(1)制取氯气时,在烧瓶中加入一定量的二氧化锰,通过____________(填写仪器名称)向烧瓶中加入适量的浓盐酸。请在装置A、B、C中选择一个合适的装置放在②处:____________。
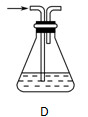
(2)部分学生认为上述装置存在缺点,他们指出在①②装置之间应增加如D所示的装置,你认为D中所盛液体是________,其作用是________________________________________。
(3)该小组对产品的性质进行了如下探究。
第一步,测其pH=10。结合相关离子方程式解释原因:_________________________________________________________________。
第二步,该小组的同学选用了紫色石蕊试液对次氯酸钠的性质进行探究。请你帮助他们完成下表:
实验操作
预期现象
结论
高三化学实验题极难题查看答案及解析