-
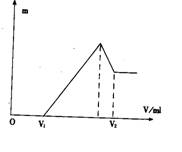
(6 分)某研究学习小组在做过氧化钠与水反应实验时,发现过氧化钠与水反应后的溶液滴加酚酞呈红色,但不久红色褪去。甲、乙、丙三个同学对此现象分别做了如下推测:
甲:因为反应后试管很热,所以很可能是溶液温度较高使红色褪去。
乙:查阅资料上载“酚酞在浓的碱溶液中因生成三钠盐而呈无色。”实验所加的水较少,红色褪去可能是生成的氢氧化钠溶液浓度较大的影响。
丙:过氧化钠具有强氧化性,生成物中O2 、H2O2(可能产物)等也具有强氧化性,可能是氧化漂白了红色物质。
(1)验证甲是否正确的方法是_________________________
(2)验证乙是否正确的方法是_________________________
难度: 简单查看答案及解析
-
(16 分)某铝合金(硬铝)中含有铝、镁、铜、硅,为了测定该合金中铝的含量,有人设计了如下实验:
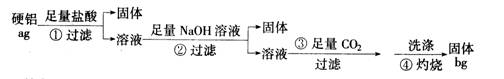
(1)补全上述①②③④各步反应的离子方程式
① Mg+2H+===Mg2++H2↑ , ___________________________
② _______________________, _______________________
Mg2++OH-===Mg(OH)2↓
③ ___________________________________
CO2+H20+ A102-===Al(OH)3↓+3HCO3-
④2A1(OH)3===Al203+H20
(2)该样品中铝的质量分数是( )
(3)第②步中加入Na0H溶液不足时,会使测定结果( )
第④步中的沉淀没有用蒸馏水洗涤时,会使测定结果( )
第④步对沉淀灼烧不充分时,会使测定结果( )
A.偏高 B.偏低 C.不影响
难度: 简单查看答案及解析
-
(12分)用下面两种方法可以制得白色的Fe(OH)2沉淀。
方法一:用不含Fe3+的FeSO4溶液与用不含O2的蒸馏水配制的NaOH溶液反应制备。
(1)用硫酸亚铁晶体配制上述FeSO4溶液时还需加入稀H2SO4和______。
(2)除去蒸馏水中溶解的O2常采用____________的方法。
(3)生成白色Fe(OH)2沉淀的操作是用长滴管吸取不含O2的NaOH溶液,插入FeSO4溶液液面下再挤出NaOH溶液。这样操作的理由是_______________________________。
方法二:在如图所示装置中,用NaOH溶液、铁屑、稀H2SO4等试剂制备。
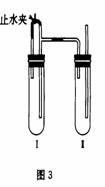
(1)在试管工里加入的试剂是_______________。
(2)在试管Ⅱ里加入的试剂是_______________。
(3)为了制得白色Fe(OH)2沉淀,在试管Ⅰ和Ⅱ中加入试剂,打开止水夹,塞紧塞子后的实验步骤是_________________________________。
(4)这样生成的Fe(OH)2沉淀能较长时间保持白色,其理由是________________________________________________________________。
难度: 简单查看答案及解析