-
葡萄糖是人体所需能量的重要来源之一。葡萄糖燃烧的热化学方程式为:
C6H12O6(s)+6O2(g)
6CO2(g)+6H2O(l) ΔH=−2800 kJ• mol−1
葡萄糖在人体组织中氧化的热化学方程式与它燃烧的热化学方程式相同。计算:
(1)100 g葡萄糖在人体内完全氧化时所产生的热量为_______________。
(2)人的体温一般要保持在36.5°C,低于此温度则要“打寒战”,并靠消耗葡萄糖释放出的能量来维持体温,与此同时有一部分能量转化为ATP。若形成 1 mol ATP需消耗10.75 g葡萄糖,则“打寒战”时会有________ %的能量转化成热量。(已知形成1 mol ATP需消耗75.24 kJ的能量)
难度: 中等查看答案及解析
-
研究化学反应中的能量变化有重要意义。请根据学过的知识回答下列问题:
(1)已知一氧化碳与水蒸气反应过程的能量变化如图所示:
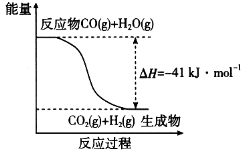
反应的热化学方程式为____________________________。
(2)化学反应可视为旧键断裂和新键形成的过程。化学键的键能是形成(或拆开)1 mol化学键时释放(或吸收)的能量。已知:N≡N键的键能是948.9 kJ•mol−1,H—H键的键能是436.0 kJ•mol−1, N—H键的键能是391.55 kJ•mol−1,则
N2(g)+
H2(g)
NH3(g)
ΔH=_____________________。
(3)依据盖斯定律可以对某些难以通过实验直接测定的化学反应的焓变进行推算。
已知:①C(s,石墨)+O2(g)
CO2(g) ΔH1=−393.5 kJ•mol−1
② 2H2(g)+O2(g)
2H2O(l) ΔH2=−571.6 kJ•mol−1
③ 2C2H2(g)+5O2(g)
4CO2(g)+2H2O(l) ΔH3=−2599 kJ•mol−1
298 K时反应2C(s,石墨)+H2(g)
C2H2(g)的焓变:ΔH=_____________________。
(4)已知:铝热反应是放热反应,又知,常温下: 4Al(s)+3O2(g)
2Al2O3(s) ΔH1
4Fe(s)+3O2(g)
2Fe2O3(s) ΔH2
下面关于ΔH1、ΔH2的比较正确的是_____________。
A.ΔH1>ΔH2 B.ΔH1<ΔH2 C.ΔH1=ΔH2 D.无法计算
难度: 中等查看答案及解析
-
观察图a和图b,根据盖斯定律,写出ΔH1、ΔH2、ΔH3、ΔH4、ΔH5和ΔH6的关系。
图a:__________________________;
图b:__________________________。
难度: 中等查看答案及解析
-
当今世界,能源的发展日益成为全世界、全人类共同关注的问题,乙烷、二甲醚的燃烧热较大,可用作燃料。如图是乙烷、二甲醚燃烧过程中的能量变化图。

请回答下列问题:
(1)乙烷的燃烧热ΔH= kJ·mol-1。
(2)等物质的量的液态乙烷比气态乙烷完全燃烧生成稳定的氧化物时放出的热量 (填“多”或“少”)。
(3)根据题图写出二甲醚完全燃烧时的热化学方程式 。
(4)二氧化碳是温室气体,从环保角度分析,放出相同的热量时选择 (填“乙烷”或“二甲醚”)作为燃料产生的CO2较少。
难度: 中等查看答案及解析
-
(1)已知2 mol氢气燃烧生成液态水时放出572 kJ的热量,反应方程式是2H2(g)+O2(g)
2H2O(l)。请回答下列问题:
①该反应的生成物能量总和____________(填“大于”、“小于”或“等于”)反应物能量总和。
②若2 mol氢气完全燃烧生成水蒸气,则放出的热量_________(填“>”“<”或“=”)572 kJ。
(2)FeS2焙烧产生的SO2可用于制硫酸。已知25 ℃、101 kPa时:
2SO2(g)+O2(g)
2SO3(g) ΔH1=−197 kJ·mol−1
H2O(g)
H2O(l) ΔH2=−44 kJ·mol−1
2SO2(g)+O2(g)+2H2O(g)
2H2SO4(l) ΔH3=−545 kJ·mol−1
则SO3(g)与H2O(l)反应的热化学方程式是____________________________。
(3)已知下列反应的热化学方程式:
①6C(s)+5H2(g)+3N2(g)+9O2(g)
2C3H5(ONO2)3(l) ΔH1
②2H2(g)+O2(g)
2H2O(g) ΔH2
③C(s)+O2(g)
CO2(g) ΔH3
则反应4C3H5(ONO2)3(l)
12CO2(g)+10H2O(g)+O2(g)+6N2(g)的ΔH为___________。
难度: 中等查看答案及解析