-
根据气象台报道,近年每到春季,沿海一些城市多次出现大雾天气,致使高速公路关闭,航班停飞。雾属于下列分散系中的
A.胶体 B.悬浊液 C.乳浊液 D.溶液
难度: 简单查看答案及解析
-
下列物质中,属于电解质的是
A.Na
CO
溶液 B.NaCl C.蔗糖 D.Cu
难度: 简单查看答案及解析
-
从分类角度看,下列变化中有一种变化与其它三种变化有本质区别,这种变化是
A.水结成冰 B.石灰石煅烧成石灰
C.铁矿石冶炼变为生铁 D.氢气还原氧化铜
难度: 简单查看答案及解析
-
下列条件下,两种气体分子数一定不相等的是
A.相同质量、不同密度的N
O和CO
B.相同体积、相同密度的CO和C
H
C.相同温度、相同压强、相同体积的O
和O
D.相同压强、相同体积、相同质量的NO
和N
O
难度: 中等查看答案及解析
-
下列实验操作均要用玻璃棒,其中玻璃棒的作用及其目的相同的是
①过滤 ②蒸发 ③溶解 ④向容量瓶转移液体
A.①和② B.①和③ C.③和④ D.①和④
难度: 中等查看答案及解析
-
双羟基铝碳酸钠是医疗上常用的一种抑酸剂,其化学式是NaAl(OH)2CO
。关于该物质的说法正确的是
A.该物质属于两性氢氧化物
B.该物质是Al(OH)3和Na2CO3的混合物
C.1 mol NaAl(OH)2CO3最多可消耗3 mol H
D.该药剂不适合于胃溃疡患者服用
难度: 中等查看答案及解析
-
现欲完成下列三个实验:①分离汽油和氯化钠溶液的混合物 ②实验室利用自来水制取蒸馏水 ③分离单质溴和水的混合物。三个实验采用的方法依次是
A.分液、萃取、蒸馏
B.萃取、蒸馏、分液
C.分液、蒸馏、萃取
D.蒸馏、萃取、分液
难度: 中等查看答案及解析
-
有体积相同的两份营养液,其配方如下:
KCl
K2SO4
ZnSO4
ZnCl2
第一份
0.3 mol
0.2 mol
0.1 mol
——
第二份
0.1 mol
0.3 mol
——
0.1 mol
两份营养液中各离子浓度
A. 完全不同 B. 完全相同 C. 仅c(K
)相同 D. 仅c(Cl
)相同
难度: 中等查看答案及解析
-
下列有关金属及其合金的说法正确的是
A.钠与氧气反应时,产物是由O2的用量决定的
B.铝箔在空气中受热可以熔化且会发生剧烈燃烧
C.金属有许多共同的物理性质,如:不透明、有金属光泽、易导电、易导热、有延展性等
D.合金中至少含两种金属
难度: 中等查看答案及解析
-
下列叙述正确的是
A.1 mol N
参加氧化还原反应时电子转移数为3×6.02×10
B.16g O
所含氧原子个数为6.02×10
C.物质的量浓度为0.5 mol·L
的MgCl
溶液,含有的Cl
数为6.02×10
D.常温常压下,22.4L SO
含分子的个数为6.02×10
难度: 困难查看答案及解析
-
某课外实验小组设计的下列实验不合理的是
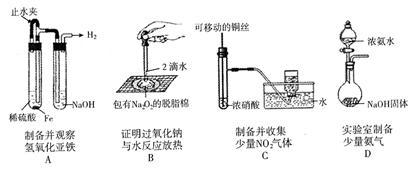
难度: 中等查看答案及解析
-
自来水可用氯气消毒,某学生用这种自来水去配制下列物质的溶液,会产生药品变质问题的是
A.NaNO
B.FeCl
C.Na
SO
D.KCl
难度: 中等查看答案及解析
-
下列有关硅的叙述中,正确的是
A.工业上通常以SiO
为原料,用氧化剂与其反应制备单质硅
B.硅是构成矿物和岩石的主要元素,硅在地壳中的含量在所有的元素中居第一位
C.硅的化学性质不活泼,在自然界中可以以游离态存在
D.硅在电子工业中,是重要的半导体材料
难度: 中等查看答案及解析
-
下列反应不属于四种基本反应类型,但属于氧化还原反应的是
A.CuO+CO
Cu+CO
B.2NaHCO
Na
CO
+H
O+CO
C.2H
+O
2H
O
D.Zn+H
SO
=ZnSO
+ H
难度: 中等查看答案及解析
-
实验室有三瓶失去标签的试剂,分别是Na
CO
、NaCl、AgNO
。实验员选择了一种试剂就把它们区别开来了,这种试剂是
A.氢氧化钠溶液 B.盐酸 C.氯化钡溶液 D.硝酸
难度: 中等查看答案及解析
-
下列操作中,溶液的颜色不发生变化的是
A.碳酸氢钠溶液中滴加稀盐酸
B.硫酸铁溶液中滴加硫氰化钾溶液
C.碘水中滴加淀粉碘化钾溶液
D.氯化铁溶液中加入还原铁粉
难度: 中等查看答案及解析
-
若在加入铝粉能放出H
的溶液中,下列各组离子一定不能大量共存的是
A.Na
、Fe
、SO
、Cl
B.Ba
、Mg
、HCO
、NO
C.Na
、K
、NO
、CO
D.K
、NO
、AlO
、OH
难度: 困难查看答案及解析
-
下列叙述不正确的是
A.NH
易液化,氨常用作制冷制
B.与金属反应时,稀HNO
可能被还原为更低价态,则稀HNO
氧化性强于浓HNO
C.铵盐受热易分解,因此贮存氨态氮肥时要密封保存,并放在阴凉通风处
D.常温下可以用铁、铝制容器盛装浓硫酸或浓硝酸
难度: 中等查看答案及解析
-
常温常压下,把二氧化碳和一氧化碳的混合气体V mL缓缓通过足量的过氧化钠固体,气体体积缩小到
mL,则二氧化碳和一氧化氮的体积比不可能是
A.2:1 B.3:2 C.3:4 D.5:4
难度: 简单查看答案及解析
-
下列反应的离子方程式中,书写正确的是
A.氯气溶于水:
B.将铝粉投入氢氧化钠溶液中:
C.铜与氯化铁溶液反应:
D.过氧化钠与水反应:
难度: 困难查看答案及解析
-
铝可与硝酸钠发生反应(未配平):Al+NaNO
+H
O
Al(OH)
+N
+NaAlO
,有关叙述正确的是
A.上述反应中水是氧化剂
B.若反应过程中转移5 mol e
则生成标准状况下N
的体积为11.2L
C.该反应的氧化产物是N
D.当消耗1 mol Al时,生成标况下N
的体积为22.4L
难度: 困难查看答案及解析
-
把Ba(OH)2溶液滴入明矾[KAl(SO4)2·12H2O]溶液中,使SO
全部转化成BaSO4沉淀,此时铝元素的存在形式是
A.Al
B.Al(OH)3 C.AlO
D.Al
和Al(OH)3
难度: 中等查看答案及解析
-
物质的量之比为2:5的锌与稀硝酸恰好反应,若硝酸被还原的产物为N
O,则该反应中被还原的硝酸与未被还原的硝酸的物质的量之比是
A.1:4 B.1:5 C.2:3 D.2:5
难度: 中等查看答案及解析
-
向一定量的FeO、Fe、Fe
O
的混合物中加入100 mL 1 mol·L
的盐酸,恰好使混合物完全溶解,放出224mL(标准状况)的气体,在所得溶液中经检验无Fe
。若用足量的CO在高温下还原相同质量的此混合物,能得到铁的质量是
A.11.2g B.5.6g C.2.8g D.无法计算
难度: 中等查看答案及解析
-
a mol FeS与b mol FeO投入到V L、c mol·L
的硝酸溶液中充分反应,产生NO气体,所得澄清溶液成分可看做是Fe(NO3)3、H2SO4的混合液,则反应中未被还原的硝酸可能为
①(a+b)×63 g ②(a+b)×189 g
③(a+b) mol ④
mol
A.①④ B.②③ C.①③ D.②④
难度: 中等查看答案及解析