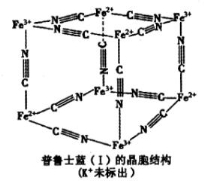
-
化学与人类生产、生活、社会可持续发展密切相关。下列说法正确的是
A.稀的食盐水能杀死H7N9禽流感病毒
B.煤经过分馏和干馏两个物理变化,可变为清洁能源
C.电镀厂的废水直接用来灌溉农田,可提高水的利用率
D.用CO2合成聚碳酸酯可降解塑料,有利于减少白色污染
难度: 中等查看答案及解析
-
下列对化学知识的认识正确的是
A.H2与T2互为同位素 B.氯化铵、氯化银都属于强电解质
C.离子化合物中一定不含共价键 D.SO2、CO均属于酸性氧化物
难度: 简单查看答案及解析
-
设NA为阿伏加德罗常数的值。下列说法正确的是
A.常温常压下,8 g甲烷中含C-H键的数目为4NA
B.25℃时,1 L pH=13的Ba(OH) 2溶液中含有的OH—数为0.2NA
C.1 mol冰醋酸和1 mol乙醇经催化加热反应生成H2O分子数为NA
D.标准状况下,2.24LCl2与过量稀NaOH溶液反应,转移的电子总数为0.1NA
难度: 中等查看答案及解析
-
下列关于有机物的表述正确的是
A.油脂可水解生成丙三醇
B.乙醇经还原可生成乙醛
C.乙烯与苯均可使酸性高锰酸钾溶液褪色
D.淀粉、蛋白质完全水解的产物互为同分异构体
难度: 中等查看答案及解析
-
下列化学反应对应的离子方程式书写正确的是
A.醋酸溶液与Mg(OH) 2反应:Mg(OH) 2 +2H+ =Mg2+ +2H2O
B.碳酸钠溶液呈碱性:CO32— +2H2O
H2CO3 +2OH—
C.NH4HCO3溶液与过量NaOH溶液反应:NH4+ +OH—=NH3·H2O
D.用惰性电极电解饱和食盐溶液:2Cl—+2H2O
2OH— +Cl2↑+H2↑
难度: 中等查看答案及解析
-
如下图所示,将甲、乙两个装有不同物质的针筒用导管连接起来,将甲针筒内的物质压到乙针筒内,进行实验,对乙针筒里的现象所作的判断不正确的是

实验序号
甲针筒内物质
乙针筒内物质
乙针筒里的现象
A
HCl
AgNO3溶液
产生白色沉淀
B
NH3
FeCl3溶液
出现红褐色沉淀
C
CO2
BaCl2
产生白色沉淀
D
Cl2
紫色石蕊溶液
先变红后褪色
难度: 中等查看答案及解析
-
ClO2是一种杀菌消毒效率高、二次污染小的水处理剂,实验室中可通过以下反应制得:
2KClO3+H2C2O4+H2SO4
2ClO2↑+K2SO4+2CO2↑+2H2O,据此,下列说法不正确的是
A.KClO3发生还原反应
B.H2C2O4在反应中被氧化
C.H2C2O4的氧化性强于ClO2的氧化性
D.每1 mol ClO2生成,该反应转移的电子数约为6.02×1023
难度: 中等查看答案及解析
-
常温下,下列各组离子能常量共存的是
A.Mg2+、K+、SO42—、NO3— B.Fe2+、H+、Cl—、NO3—
C.Cu2+、Na+、OH—、Cl— D.K+、HCO3—、Ca2+、OH—
难度: 中等查看答案及解析
-
下列物质间的转化在给定条件下能实现的是
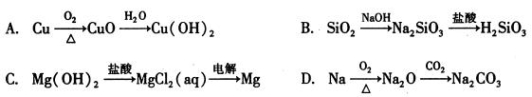
难度: 中等查看答案及解析
-
利用下列图示进行相应实验,能达到目的的是
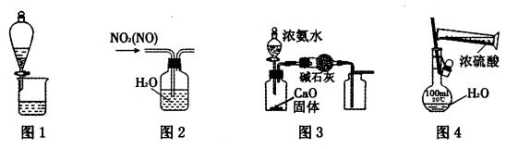
A.用图1可萃取碘水中的碘
B.用图2可除去NO2中的NO
C.用图3制取并收集干燥纯净的NH3
D.用图4配制100mL一定物质的量浓度的稀硫酸
难度: 中等查看答案及解析
-
下列相关工业制法的描述不正确的是
A.电解熔融氯化钠制取金属钠
B.电解熔融的Al(OH) 3制取金属铝
C.用石英、纯碱、石灰石为原料制玻璃
D.用焦炭在电炉中还原二氧化硅得到含杂质的粗硅
难度: 中等查看答案及解析
-
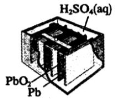
一种微生物燃料电池的结构示意图如下所示,关于该电池的叙述正确的是

A.电池工作时,电子由a流向b
B.微生物所在电极区放电时发生还原反应
C.放电过程中,H+从正极区移向负极区
D.正极反应式为:MnO2+4H+ +2e— ===Mn2+ +2 H2O
难度: 中等查看答案及解析
-
下列图示与对应的叙述相符的是

A.图甲表示催化剂能改变化学反应的焓变
B.图乙表示向氨水中加水时溶液导电性的变化情况,且溶液c(OH—)大小:a<b
C.由图丙可知反应2A(g)+B(g)
C(g)的△H >O,且 a=2
D.图丁表示向CH3COOH溶液中逐渐加入CH3COONa固体后,溶液pH的变化情况
难度: 中等查看答案及解析
-
常温下,电解质溶液的性质与变化是多样的,下列说法正确的是
A.pH相同的①CH3COONa ②NaClO ③NaOH三种溶液c(Na+)大小:①>②>③
B.往稀氨水中加水,
的值变小
C.pH=4的H2S溶液与pH=10的NaOH溶液等体积混合,存在下列等式:c(Na+)+c(H+) = c(OH—)+2c(S2—)
D.Ca(ClO) 2溶液中通入少量CO2,ClO—水解程度增大,溶液碱性增强
难度: 困难查看答案及解析
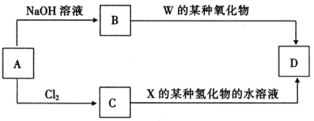
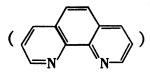 结合显橙红色,再用比色法测定。其中涉及以下反应:4FeCl3 + 2NH2OH·HCl=4FeCl2 + N2O↑+ 6HCI + H2O。
结合显橙红色,再用比色法测定。其中涉及以下反应:4FeCl3 + 2NH2OH·HCl=4FeCl2 + N2O↑+ 6HCI + H2O。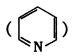 和邻啡罗啉都是含氮的有机物,l mol吡啶中含有σ键的物质的量为
和邻啡罗啉都是含氮的有机物,l mol吡啶中含有σ键的物质的量为