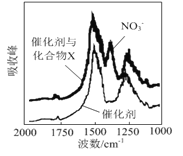
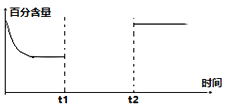
-
根据实验操作和现象不能推出相应结论的是
选项
实验操作和现象
实验结论
A
在Na2S溶液中滴加新制氯水,产生浅黄色沉淀
非金属性:C1>S
B
SO2气体通入Na2SiO3溶液中,产生胶状沉淀
酸性:H2SO3>H2SiO3
C
将KI和FeCl3溶液在试管中混合后,加入CC14,振荡,静置,下层溶液显紫红色
氧化性:Fe3+>I2
D
加热盛有少量NH4HCO3固体的试管,并在试管口放置湿润的紅色石蕊试纸,石蕊试纸变蓝
NH4HCO3呈碱性
A. A B. B C. C D. D
难度: 困难查看答案及解析
-
化学与社会、生活密切相关。对下列现象或事实的解释正确的是
A.用含有铁粉的透气小袋与食品一起密封包装,说明铁粉能吸收水分
B.浓硫酸可以盛放在铝桶中,说明铝不能与浓硫酸反应
C.硫酸铝与碳酸氢钠能制作泡沫灭火剂,利用了硫酸铝溶液与碳酸氢钠溶液混合后能发生剧烈双水解反应
D.用氢氟酸雕刻玻璃,说明氢氟酸是强酸
难度: 中等查看答案及解析
-
下列有关物质的分类或归纳的说法正确的是
A. 漂白粉、水玻璃、福尔马林都是混合物
B. 乙烯、油脂、纤维素、光导纤维都属于高分子化合物
C. PM 2.5(微粒直径约为 2.5×10-6 m)分散在空气中形成气溶胶,能产生丁达尔效应
D. 纯碱、氨水、蔗糖分别属于强电解质、弱电解质和非电解质
难度: 简单查看答案及解析
-
夹紧下列装置中的弹簧夹并进行相关操作。下列情形中,表明相应装置漏气的是( )

A. 装置①中,用手捂住试管,烧杯中出现气泡,放开手后,导管中形成一段稳定的水柱
B. 装置②中,向长颈漏斗中加入一定量水,形成水柱,随后水柱下降至与瓶中液面相平的位置
C. 装置③中,双手捂住烧瓶,导管中形成一段稳定的水柱,双手放开后,水柱慢慢回落
D. 装置④中,将a管向上提至一段高度,a、b两管之间水面形成稳定的高度差
难度: 中等查看答案及解析
-
以下离子方程式正确的的是
A. 向明矾溶液中滴加Ba(OH)2溶液,恰好使SO42-沉淀完全:2Al3++3SO42-+3Ba2++6OH-=2BaSO4↓+2Al(OH)3↓
B. Fe(NO3)2溶液中滴加少量稀盐酸:Fe2++NO3-+4H+=Fe3++NO↑+2H2O
C. 少量的SO2通入NaClO溶液:SO2+3ClO-+H2O=SO42-+Cl-+2HClO
D. Ca(HCO3)2溶液与过量NaOH溶液反应:HCO3-+Ca2++OH-=CaCO3↓+H2O
难度: 中等查看答案及解析
-
下列图示与对应的叙述相符的是( )
甲
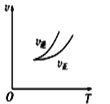 乙
乙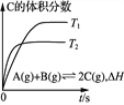 丙
丙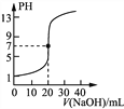 丁
丁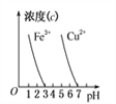
A. 由甲图甲可知正反应为放热反应
B. 乙表示在相同的密闭容器中,不同温度下的反应,该反应的ΔH>0
C. 丙表示0.1000mol·L-1NaOH溶液滴定20.00mL0.1000mol·L-1醋酸溶液的滴定曲线
D. 根据图丁,除去CuSO4溶液中的Fe3+,可加入NaOH调节pH至3~4
难度: 中等查看答案及解析
-
对下列实验过程的评价,正确的是( )
A. 某固体中加入稀盐酸,产生了无色气体,证明该固体中一定含有碳酸盐
B. 某溶液中滴加BaCl2溶液,生成白色沉淀,证明一定含有SO
C. 用萃取的方法分离汽油和煤油
D. 验证烧碱溶液中是否含有Cl-,先加稀硝酸除去OH-,再加入AgNO3溶液,有白色沉淀,证明含Cl-
难度: 困难查看答案及解析
-
标准状况下,向100 mL H2S饱和溶液中通入SO2气体,所得溶液pH变化如图所示。下列分析正确的是

A. a点对应溶液的导电性比d点强
B. 氢硫酸的酸性比亚硫酸的酸性强
C. 向d点对应的溶液中加入Ba(NO3)2溶液,产生BaSO4白色沉淀
D. H2S饱和溶液的物质的量浓度为0.05 mol·L-1
难度: 困难查看答案及解析
-
某小组拟用如图装置制备氮化钙(化学式为Ca3N2,极易与H2O反应),下列说法正确的是
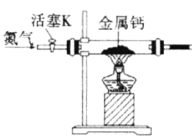
A. 打开活塞K通入N2,试管A内有气泡产生.说明装置气密性良好
B. 将产物Ca3N2放入盐酸中,能得到CaCl2和NH4Cl两种盐
C. U形管中盛放的干燥剂可以是碱石灰,也可以能用浓硫酸
D. 反应结束后,先关闭活塞K,再熄灭酒精灯待反应管冷却至室温
难度: 中等查看答案及解析
-
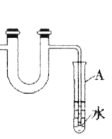
用如图装置进行实验,将液体A逐滴加入到固体B中,下列叙述正确的是
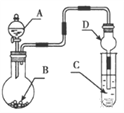
A. 若A为H2O2,B为MnO2,C中盛有Na2S溶液, C中溶液变浑浊
B. 若A为浓盐酸,B为MnO2,C中盛有KI淀粉溶液,C中溶液变蓝色
C. 若A为浓氨水,B为生石灰,C中盛有AlCl 3溶液, C中先产生白色沉淀后沉淀又溶解
D. 若A为浓H2SO4 ,B为CaCO3,C中盛有Na2SiO3 溶液,C中溶液出现白色沉淀,证明非金属性S>C>Si
难度: 困难查看答案及解析
-
硫酸亚铁是一种重要的化工原料,可以制备一系列物质(如下图所示)。下列说法错误的是

A. 常温下,(NH4)2Fe(SO4)2在水中的溶解度比FeSO4的大
B. 为防止NH4HCO3分解,生产FeCO3需在较低温度下进行
C. 可用KSCN溶液检验(NH4)2Fe(SO4)2是否被氧化
D. 碱式硫酸铁水解能产生Fe(OH)3胶体,可用作净水剂
难度: 中等查看答案及解析
-
短周期主族元素A、B、C、D的原子序数依次增大。己知A、C的原子序数之差为8,A、B、C三种元素原子的最外层电子数之和为15,B元素原子的最外层电子数等于A元素原子的最外层电子数的一半,下列叙述正确的是
A. 简单离子的半径:B>C>D B. B与D形成的化合物溶于水所得溶液显酸性
C. C与D不可能形成化合物C2D2 D. B与C形成的化合物在水溶液中能稳定存在
难度: 中等查看答案及解析
-
二氯化二硫(S2Cl2)是广泛用于橡胶工业的硫化剂,常温下是一种橙黄色有恶臭的液体,它的分子结构与H2O2类似,熔点为193K,沸点为411K,遇水很容易水解,产生的气体能使品红褪色,S2Cl2可由干燥氯气通入熔融的硫中制得。下列有关说法正确的是
A. S2Cl2的电子式为
B. 固态时S2Cl2属于原子晶体
C. S2Cl2与NaOH的化学方程式可能为:S2Cl2+6NaOH=2NaCl+Na2SO3+Na2S+3H2O
D. S2Cl2是含有极性键和非极性键的离子化合物
难度: 中等查看答案及解析
-
某温度下,对可逆反应2X(g) + Y(g)
3Z(g) + W(s) ΔH>0 的叙述正确的是
A. 加入少量W,逆反应速率增大,平衡向左移动
B. 增大压强,正反应速率增大,逆反应速率减小
C. 温度、体积不变,充入He气增大压强,反应速率会加快
D. 升高温度,混合气体的平均相对分子质量减小
难度: 中等查看答案及解析
-
NaHSO3溶液在不同温度下均可被过量KIO3氧化,当NaHSO3完全消耗即有I2析出,根据I2析出所需时间可以求得NaHSO3的反应速率。将浓度均为0.020mol/LNaHSO3溶液(含少量淀粉)10.0mL、KIO3(过量)酸性溶液40.0mL混合,记录10~55℃间溶液变蓝时间,55℃时未观察到溶液变蓝,实验结果如图。据图分析,下列判断不正确的是
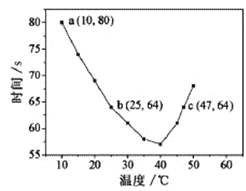
A. 40℃之前与40℃之后溶液变蓝的时间随温度的变化趋势相反
B. 图中b、c两点对应的NaHSO3反应速率相等
C. 图中a点对应的NaHSO3反应速率为5.0×10-5mol·L-1·s-1
D. 温度高于40℃时,淀粉不宜用作该实验的指示剂
难度: 简单查看答案及解析
-
下列说法或表示方法正确的是
A. 等质量的硫蒸气和硫固体分别完全燃烧,后者放出的热量多
B. 由C(金刚石,s)=C(石墨,s)△H=-1.90 kJ/mol可知,金刚石比石墨稳定
C. 氢气的燃烧热285.8kJ/mol,氢气燃烧的热化学方程式为:2H2(g)+O2(g)=2H2O(l) △H=+285.8 kJ/mol
D. 氢氧化钡晶体与氯化铵晶体混合吸热,反应物的总键能之和高于生成物的总键能之和
难度: 中等查看答案及解析
-
在3 种不同条件下,分别向容积为2L的恒容密闭容器中充入2 molA和1mol B,发生反应: 2A(g)+B(g)
2D(g)△H=QkJ/mol。相关条件和数据见下表:
实验编号
实验I
实验II
实验III
反应温度/℃
700
700
750
达平衡时间/min
40
50
30
n(D)平衡/mol
1.5
1.5
1
化学平衡常数
K1
K2
K3
下列说法正确的是
A. 升高温度能加快反应速率的原理是降低了反应的活化能,使活化分子百分数提高
B. 实验III达平衡后,保持其他条件不变,再向容器中通入1molA 和1molD,平衡不移动
C. 实验III达平衡后容器内的压强是实验1的9/10倍
D. K3>K2>K1
难度: 中等查看答案及解析
-
某无色溶液Y可能含有Na+、Fe3+、Ba2+、NH4+、Cl-、SO42-、HCO3-、HSO3-中的几种离子,溶液中阳离子浓度相同。为了确定其组成,某同学进行了如下实验(假设气体均全部逸出,忽略H2O2的分解)。下列说法不正确的是
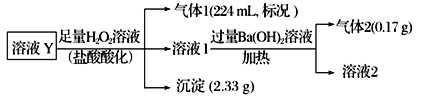
A. 溶液Y中一定不存在Fe3+、SO42-
B. 溶液Y中一定含有Cl-,且n(Cl-)=0.01 mol
C. 溶液Y中肯定存在HCO3-、HSO3-、Ba2+、NH4+
D. 溶液Y中可能存在Na+,为确定其是否存在,可取溶液1通过焰色反应实验验证
难度: 中等查看答案及解析
-
将13.6g带铁锈的铁片溶解于25mL、14mol/L的热的浓硫酸中,气体只有SO2且体积为1.12L (标准状况)。将溶液稀释至100mL,所得溶液遇KSCN溶液时无血红色出现。下列结论正确的是
A. 反应中:转移电子3.01×1022个 B. 反应后:剩余硫酸0.30 mol
C. 原混合物:n (Fe2O3):n(Fe)=1:2 D. 所得溶液:c(FeSO4)=1.7mol/L
难度: 中等查看答案及解析
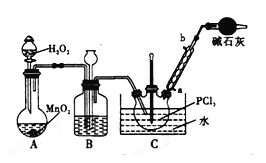
 图2
图2