-
既要在一充满空气的瓶子中,将其中的氧气除去.又不增加其他气体的成分.下列物质在瓶中燃烧可达到目的是( )
A.木炭
B.硫磺
C.铁丝
D.红磷难度: 中等查看答案及解析
-
由我国著名科学家、中国科学院院士张青莲教授主持测定了铟、铱、锑、铸等几种元素的相对原子质量新值,其中他测定核电荷数为63的铕元素的相对原子质量的新值为l52,则下列说法正确的是( )
A.铕元素原子的质子数为63
B.铕元素原子的中子数为63
C.铕元素原子的核外电子数为152
D.铕元素原子的质量为152难度: 中等查看答案及解析
-
下列现象的产生,与空气中的水蒸气无关的是( )
A.酥脆的饼干放置在空气中变软
B.夏天从冰箱取出的冰糕冒“白气”
C.冬季的早晨看到窗户的玻璃上有“冰花”
D.进入久未开启的菜窖或干涸深井使人感到气闷、头昏难度: 中等查看答案及解析
-
下列化学现象描述正确的是( )
A.把盛有红磷的燃烧匙伸入氧气中,红磷立即燃烧
B.铝箔在氧气中燃烧,火星四射,生成一种黑色固体
C.木炭在氧气中燃烧更旺,发出白光,并放出热量
D.硫在氧气中燃烧,火焰呈淡蓝色,生成一种无色的气体难度: 中等查看答案及解析
-
下列反应中,既不属于化合反应,也不属于氧化反应的是( )
A.硫在氧气中燃烧
B.石蜡在空气中燃烧
C.高锰酸钾受热分解
D.镁带在空气中燃烧难度: 中等查看答案及解析
-
人体吸入的O2有2%的转化为活性氧,它能加速人体的衰老,被称为“夺命杀手”.我国科学家尝试用亚硒酸钠(Na2SeO3)清除人体内的活性氧.Na2SeO3中的Se(硒)元素的化合价是( )
A.+2
B.+3
C.+4
D.+6难度: 中等查看答案及解析
-
用分子的观点解释下列现象,不合理的是( )
A.食物变质--分子本身发生了变化
B.汽油挥发--分子大小发生了变化
C.热胀冷缩--分子间间隔改变
D.花香四溢--分子作扩散运动难度: 中等查看答案及解析
-
某无毒气体的密度约是空气密度的5/9,且极难溶于水,在空气中不易变质.那么收集该气体所用的方法是:①向上排空气法②向下排空气法③排水法( )
A.①或②
B.①或③
C.②或③
D.①②③均可难度: 中等查看答案及解析
-
从空气质量报告中可以看出.造成某市空气污染的首要污染物是可吸入颗粒物和二氧化硫.下列对其形成主要原因的分析不合理的是( )
A.环境绿化不好.粉尘随风飘扬
B.生活和生产中燃烧煤炭
C.工业生产排放废水
D.机动车排放尾气难度: 中等查看答案及解析
-
日常生活中常见到下列现象,其中发生了化学变化的是 ( )
A.冬天的早晨,玻璃窗上出现美丽的冰花
B.自行车轮胎在烈日下爆裂
C.牛奶放置时间过长变质
D.玻璃杯被打碎难度: 中等查看答案及解析
-
高铁酸钾(化学式K2FeO4)集氧化、吸附、凝聚、杀菌等功能于一体,目前被广泛应用于自来水净化处理领域.高铁酸钾中铁元素的化合价为( )
A.+2价
B.+3价
C.+5价
D.+6价难度: 中等查看答案及解析
-
下列物质中,属于氧化物的是( )
A.蒸馏水(H2O)
B.硝酸(HNO3)
C.氧气(O2)
D.氢氧化铜[Cu(OH)2]难度: 中等查看答案及解析
-
一氧化氮(NO)为大气污染物,但少量一氧化氮在人体内,具有扩张血管、增强记忆功能.一氧化氮密度比空气大,难溶于水,极易与氧气反应.若让你收集一瓶一氧化氮气体,应选用的收集方法是( )
A.向下排空气法
B.向上排空气法
C.排水集气法
D.排水集气法或向下排空气法难度: 中等查看答案及解析
-
下列有关水分子的说法中错误的是( )
A.水分子由氢、氧两种原子构成
B.水变成蒸气时,水分子变大
C.水受热时,水分子运动加快
D.水电解时,水分子发生改变难度: 中等查看答案及解析
-
下列有关分子、原子和离子的说法正确的是( )
A.保持氧气化学性质的粒子是氧原子
B.原子的最外层电子数决定元素的种类
C.氯化钠是由离子构成的化合物
D.分子间有一定间隔,原子间没有间隔难度: 中等查看答案及解析
-
下列化学实验基本操作正确的是( )
A.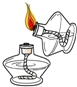
点燃酒精灯
B.
称量10.05g固体
C.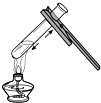
液体加热
D.
用100mL量筒量取9.5mL液体难度: 中等查看答案及解析
-
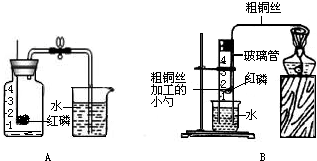
下图一次是实验室制取、收集、检验氧气和验证其性质的装置.其中错误的是( )
A.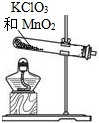
B.
C.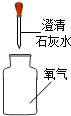
D.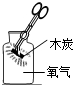
难度: 中等查看答案及解析
-
对下列实验指定容器中的水,其解释没有体现水的主要作用的是( )
A B C D 实
验
装
置
硫在氧气中燃烧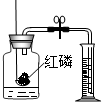
测定空气中氧气含量
铁丝在氧气中燃烧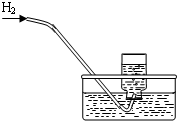
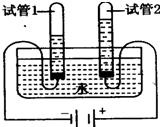
排水法收集氢气解释 集气瓶中的水:
吸收放出的热量量筒中的水:
通过水体积的变化得出O2体积集气瓶中的水:
冷却溅落融熔物,防止集气瓶炸裂集气瓶中的水:
水先将集气瓶内的空气排净,后便于观察H2何时收集满
A.A没有体现水的主要作用
B.B没有体现水的主要作用
C.C没有体现水的主要作用
D.D没有体现水的主要作用难度: 中等查看答案及解析
-
下列图中能表示保持水的化学性质的粒子是(
表示氢原子,
表示氧原子)( )
A.
B.
C.
D.难度: 中等查看答案及解析
-
对下列实验现象进行解释错误的是( )
A B C D 实验现象 用隧道显微镜获得的苯分子的图象 
品红加入水中后整个液体变为红色 水分子在不同温度下的运动情况 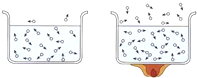
50ml水和50ml酒精混合后的体积小于100ml 
解释 分子的质量和体积都很小 分子总是在不断运动着 常温时分子不运动,加热时分子才运动 分子间有间隙
A.A选项
B.B选项
C.C选项
D.D选项难度: 中等查看答案及解析
-
如右图是元素周期表中碳元素的相关信息,对图中信息理解不正确的是( )

A.碳原子的核内质子数是6
B.碳元素属于非金属元素
C.碳原子的质量是12.01g
D.碳的相对原子质量是12.01难度: 中等查看答案及解析
-
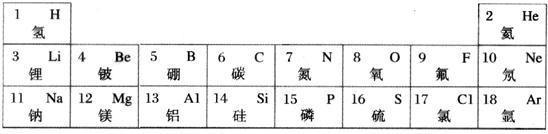
右表为元素周期表的一部分,A--E代表五种不同元素.下列说法不正确的是( )
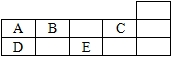
A.原子序数C>B
B.核内质子数:A=E
C.A,B,C同周期
D.D,E同族难度: 中等查看答案及解析
-
下列原子结构示意图中,表示带两个单位正电荷的离子的是( )
A.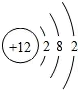
B.
C.
D.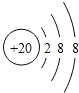
难度: 中等查看答案及解析
-
孔雀石的主要成分是Cu2(OH)2CO3.下列关于Cu2(OH)2CO3的说法正确的是( )
A.它由5种元素组成
B.它由8个原子构成
C.其中Cu的化合价为+2价
D.其中Cu的质量分数为20%难度: 中等查看答案及解析
-
2008年9月,三鹿婴幼儿奶粉因添加三聚氰胺(C3H6N6)致使一些婴幼儿患肾结石病.下列关于三聚氰胺的说法正确的是( )
A.三聚氰胺由碳、氢、氮三个元素组成
B.三聚氰胺中碳、氢、氮质量比为1:2:2
C.三聚氰胺中氮元素的质量分数为66.7%
D.三聚氰胺的相对分子质量为126g难度: 中等查看答案及解析
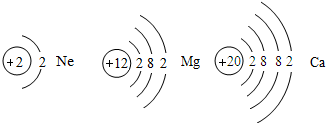
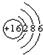 所表示的粒子符号为________,它的最外层电子数为________.
所表示的粒子符号为________,它的最外层电子数为________.