-
下列说法正确的是
A.60mL的H2S和80mL的O2混合点燃后恢复到原状况时可产生55mL的SO2
B.pH在5.6~7.0之间的雨水通常称为酸雨,故在煤燃烧时加入石灰石,可有效减少酸雨的产生
C.用PH试纸可以鉴别浓硫酸和稀硫酸
D.室温下浓硫酸或稀硝酸与铜片均不会发生剧烈的化学反应,原因是铜发生了钝化现象
难度: 简单查看答案及解析
-
将A气体通入BaCl2溶液,未见沉淀生成,然后通入B气体,有沉淀生成,再加入过量的稀盐酸后沉淀消失,则A、B气体可能是
A.SO2、H2S B.SO2、NO2 C. CO2 、NH3 D.SO2、Cl2
难度: 中等查看答案及解析
-
下列关于某些离子检验的方法,其中说法正确的是
A.向某溶液中加稀盐酸,将产生的无色无味的气体通入过量的澄清石灰水中,石灰水变浑浊,则原溶液中一定存在CO32-或HCO3-
B.向某溶液中加入硝酸钡溶液有白色沉淀产生,再加稀盐酸,沉淀不消失,则原溶液中一定存在SO42-
C.向某溶液中加入浓氢氧化钠溶液并加热,产生的气体能使湿润的蓝色石蕊试纸变红,则原溶液中一定存在NH4+
D.向某溶液中加入硝酸银溶液产生白色沉淀,再加稀盐酸,沉淀不消失,则原溶液中一定存在Cl-
难度: 中等查看答案及解析
-
下列离子方程式书写正确的是
A.将NO2气体通入NaOH溶液中:3NO2+2OH-=2NO3-+NO↑+H2O
B.将铁丝插入过量的稀硝酸中:Fe+4H++NO3-=Fe3++NO↑+2H2O
C.IBr和Cl2的化学性质相似,将IBr通入NaOH溶液中:IBr+2OH-=I-+BrO-+H2O
D.Na2S溶液通入足量SO2气体:2S2-+SO2+2H2O=3S↓+4OH-
难度: 简单查看答案及解析
-
下列叙述Ⅰ和Ⅱ均正确并且有因果关系的是
选项
叙述Ⅰ
叙述Ⅱ
A
浓硝酸和稀硝酸都具有强氧化性
浓硝酸和稀硝酸均可使紫色石蕊试液先变红后褪色
B
浓硫酸具有强氧化性和吸水性
浓硫酸可干燥H2和CO,不可干燥 SO2和NH3
C
SO2是酸性氧化物
SO2可使含有酚酞的NaOH溶液褪色
D
铵盐受热易分解
NH4Cl和NH4HCO3均可用作氮肥和制取氨气
难度: 中等查看答案及解析
-
我国有广阔的海岸线,建设海峡经济区,海水的综合利用大有可为,下图所示为海水综合利用部分流程,有关说法正确的是
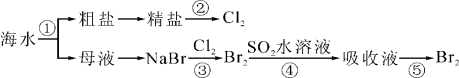
A.上述工艺流程中涉及到化合、分解、复分解和置换反应
B.①只发生了化学变化,②是工业上用电解熔融NaCl制备Cl2
C.③④涉及的反应均为氧化还原反应,⑤只需要蒸馏即可得到单质Br2
D.④中反应的离子方程式为SO2+Br2+2H2O===4H++SO42-+2Br-
难度: 简单查看答案及解析
-
3.87克锌铜合金完全溶解于150mL、密度为1.20g/cm3、质量分数为21%的稀硝酸中,得到NO气体896mL (标准状况),向反应后的溶液中加入适量的1.0mol/LNaOH溶液,恰使溶液中的金属离子全部沉淀。下列说法不正确是
A.该稀硝酸中HNO3的物质的量浓度是4.0mol/L
B.加入NaOH溶液的体积是560mL
C.被还原的硝酸的物质的量为0.04mol
D.得到的金属氢氧化物的沉淀为5.81克
难度: 简单查看答案及解析