-
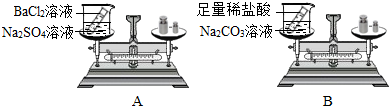
在一个密闭容器中放入M、N、Q、P四种物质,在一定条件下发生化学反应,一段时间后,测得有关数据如下表,则关于此反应认识错误的是( )
物质 M N Q P 反应前质量(g) 18 1 2 32 反应后质量(g) X 26 2 12
A.该变化的基本反应类型是分解反应
B.反应后物质M的质量为l3g
C.反应中M、P均为反应物
D.物质Q一定是该反应的催化剂难度: 中等查看答案及解析
-
下列净化水的操作中,净化效果最好的是( )
A.静置
B.过滤
C.蒸馏
D.吸附难度: 中等查看答案及解析
-
金刚石、石墨、木炭和C60都是由碳元素组成的单质,下列关于碳的单质的叙述正确的是( )
A.都是黑色固体
B.在氧气中充分燃烧时都生成二氧化碳
C.碳原子的排列方式相同
D.一定条件下,石墨转化成金刚石是物理变化难度: 中等查看答案及解析
-
氢气不同于其他气体最显著的特点是( )
A.无色无味
B.难溶于水
C.可以燃烧
D.密度最小难度: 中等查看答案及解析
-
鉴别日常生活中的下列各组物质,操作1和操作2均有错误 的是( )
选项 鉴别的物质 操作1 操作2 A 软水和硬水 滴加肥皂水 加热蒸发 B 一氧化碳和甲烷 滴加澄清石灰水 观察颜色 C 氧气和二氧化碳 滴加紫色石蕊试液 伸入燃着的木条 D 真黄金和假黄金(铜锌合金) 滴加稀盐酸 灼烧
A.A
B.B
C.C
D.D难度: 中等查看答案及解析
-
下列能源在使用的过程中,可能会引起酸雨的是( )
A.煤
B.风能
C.氢能
D.太阳能难度: 中等查看答案及解析
-
煤气有毒,一旦泄漏将对生命和财产带来严重危害.为了及时发现煤气泄漏现象,常在煤气中加入少量有特殊气味的乙硫醇(C2H5SH).乙硫醇在煤气燃烧过程中可充分燃烧,其反应的化学方程式为:2C2H5SH+9O2=4CO2+2X+6H2O,则X的化学式为( )
A.SO2
B.SO3
C.H2SO4
D.CO难度: 中等查看答案及解析
-
物质的用途和性质密切相关.下列用途主要是利用其化学性质的是( )
A.
活性炭用于防毒面具
B.
金刚石作装饰品
C.
铜丝作导线
D.
氢气作高能燃料难度: 中等查看答案及解析
-
北约对南联盟轰炸时使用含碳单质导弹轰炸电厂造成供电中断该单质是( )
A.金刚石
B.炭黑
C.石墨
D.焦炭难度: 中等查看答案及解析
-
复方冬青油软膏具有强力迅速镇痛作用.其有效成分的分子模型如下图,其化学式为C8H8O3.下列说法中不正确的是( )
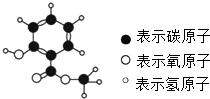
A.该有机物由3种元素组成
B.该有机物分子中氢、氧原子的个数比为8:3
C.该有机物分子中碳、氢元素的质量比为1:1
D.该有机物中含氢元素的质量分数最小难度: 中等查看答案及解析
-
在硝酸铵样品中,含有98%的硝酸铵,则该样品中氮元素的质量分数是( )
A.35%
B.34.3%
C.17.15%
D.16.8%难度: 中等查看答案及解析
-
下列区别CO和CO2气体最好的方法是( )
A.用动物实验它们的毒性
B.能否使带火星的木条复燃
C.通入澄清的石灰水
D.观察它们在水中的溶解性难度: 中等查看答案及解析
-
为了防治碘缺乏症,我国政府推广使用加碘食盐,所谓碘盐就是在食盐中加入一定量的碘酸钾(化学式:KIO3) 其中碘元素的化合价是( )
A.+1价
B.+3价
C.+5价
D.+7价难度: 中等查看答案及解析
-
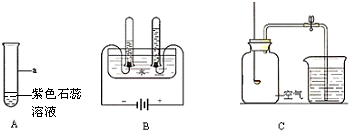
下列有关CO2的实验只能证明CO2物理性质的是( )
A.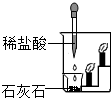
B.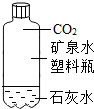
C.
D.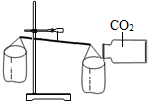
难度: 中等查看答案及解析
-
原煤(含硫元素)在氧气中不完全燃烧会生成CO、CO2 和SO2.若测得CO、CO2、和SO2的混合气体中碳元素的质量分数为24%,则其中SO2的质量分数可能是( )
A.10%
B.30%
C.50%
D.70%难度: 中等查看答案及解析
-
只含铜、氧两种元素的固体样品9.0g,测得其中含铜元素的质量为8.0g.已知铜有CuO和Cu2O两种氧化物,且均为固体.下列说法不正确的是( )
A.固体样品可能是Cu2O
B.固体样品的物质成分组合只有2种情况
C.固体样品可能是Cu、CuO与Cu2O的混合物
D.若固体样品中只含两种物质,则两种物质的质量比可能为5:4难度: 中等查看答案及解析
-
含相同质量氧元素的NO、NO2、N2O3、N2O5、N2O五种物质中,所含氮元素的质量比为( )
A.1:2:3:5:4
B.2:4:3:5:1
C.60:30:20:10:5
D.30:15:20:12:60难度: 中等查看答案及解析
-
等质量的M、N两种金属,分别与相同质量分数的足量稀盐酸反应(已知M、N在生成物中均为+2价),生成氢气质量和反应时间的关系如图所示,下列叙述正确的是( )
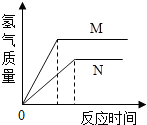
A.M、N两种金属中较活泼的是N
B.生成H2的质量M<N
C.相对原子质量较大的是N
D.产生H2的速率N>M难度: 中等查看答案及解析
-
向含有AgNO3、Cu(NO3)2的混合溶液中加入一定量的锌粉,充分反应后过滤.向滤出的固体中滴加稀盐酸,没有气体生成.下列结论正确的是( )
A.滤出的固体中一定含有Ag
B.滤出的固体一定是Ag和Cu的混合物
C.滤液中一定有Zn(NO3)2和Cu(NO3)2,可能含有AgNO3
D.滤液中一定没有AgNO3和Cu(NO3)2难度: 中等查看答案及解析
-
通过下列实验得出的结论不合理的是( )
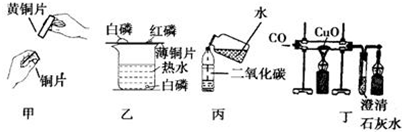
A.甲图黄铜片能在铜片上刻出明显痕迹,说明黄铜片的硬度比铜大
B.乙图薄铜片上的白磷燃烧,红磷和水中的白磷不燃烧,说明燃烧既要有氧气参加,温度又要达到可燃物的着火点
C.丙图既可以说明二氧化碳易溶于水,又可以说明它能与水反应生成碳酸
D.丁图说明一氧化碳具有还原性难度: 中等查看答案及解析