-
常用于治疗胃酸过多的是
A. 碳酸钠 B. 氢氧化铝 C. 氧化钙 D. 硫酸钡
难度: 简单查看答案及解析
-
下列我国古代的技术应用中,其工作原理不涉及化学反应的是
A. 火药使用 B. 粮食酿酒 C. 转轮排字 D. 湿法炼铜
难度: 简单查看答案及解析
-
漂粉精的有效成分是
A. Ca (ClO) 2 B. CaCl2 C. CaCO3 D. Ca(OH)2
难度: 简单查看答案及解析
-
将两种互不相溶的液体分离的方法是
A. 结晶 B. 分液 C. 蒸馏 D. 过滤
难度: 简单查看答案及解析
-
以下过程与化学键断裂无关的是
A. 氯化钠熔化 B. 金刚石熔化 C. 金属汞汽化 D. 干冰升华
难度: 简单查看答案及解析
-
有关35Cl和37Cl的说法正确的是
A. 核外电子数不同 B. 化学性质不同 C. 互为同位素 D. 中子数相同
难度: 简单查看答案及解析
-
一定条件下,氨气与氟气发生反应:4NH3+3F2→NF3+3NH4F,其中NF3空间结构与NH3相似。下列有关说法错误的是
A. 反应物和生成物均为共价化合物 B. NF3空间结构为三角锥形
C. NF3中只含极性共价键 D. NH4F中既含有离子键又含有共价键
难度: 简单查看答案及解析
-
具有下列性质的物质可能属于离子晶体的是
A. 熔点113 ℃,能溶于CS2 B. 熔点44℃,液态不导电
C. 熔点1124℃,易溶于水 D. 熔点180 ℃,固态能导电
难度: 简单查看答案及解析
-
不能检验溶液中I- 的试剂是
A. AgNO3、稀HNO3 B. 氯水、CCl4
C. 氯水、淀粉 D. KBr、稀HCl
难度: 简单查看答案及解析
-
侯氏制碱法制造纯碱同时副产氯化铵。在母液处理上,有关说法错误的是
A. 水浴加热,有利于NH4Cl更多地析出
B. 加入食盐,增大Cl-的浓度,使NH4Cl更多地析出
C. 通入氨气,增大NH4+的浓度,使NH4Cl更多地析出
D. 通入氨气,使NaHCO3转化为Na2CO3,提高析出的NH4Cl纯度
难度: 简单查看答案及解析
-
工业电解饱和食盐水时,产生氢气的电极是
A. 阳极 B. 阴极 C. 正极 D. 负极
难度: 简单查看答案及解析
-
可用来鉴别乙醇、乙醛的试剂是
A. 银氨溶液 B. 乙酸溶液 C. 氯化铁溶液 D. 氢氧化钠溶液
难度: 简单查看答案及解析
-
下列排列的顺序错误的是
A. 羟基氢原子的活泼性:CH3COOH>H2O>C2H5OH
B. 碱性:NaOH>Mg(OH)2>Al(OH)3
C. 原子半径:Na>Al>O
D. 热稳定性:HCl>PH3>H2S
难度: 中等查看答案及解析
-
制备乙酸丁酯实验装置正确的是
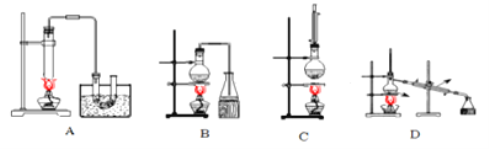
A. A B. B C. C D. D
难度: 中等查看答案及解析
-
配制一定物质的量浓度的NaCl溶液时,下列因素对结果没有影响的是
A. 溶解过程中有少量液体溅出 B. 容量瓶使用前未干燥
C. 洗涤液未全部转移到容量瓶中 D. 定容时液面未到刻度线
难度: 简单查看答案及解析
-
研究电化学腐蚀及防护的装置如右图所示。有关说法正确的是
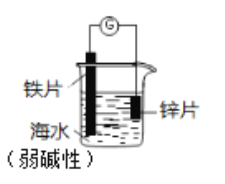
A. 锌片发生氧化反应作阴极
B. 电子从铁片经过导线流向锌片
C. 铁片上电极反应为:2H+ + 2e→H2↑
D. 该装置可用于研究牺牲阳极的阴极保护法
难度: 中等查看答案及解析
-
将等物质的量的Cl2和SO2通入BaCl2溶液,充分反应后滴入品红溶液,能观察到的现象是:①出现沉淀;②不出现沉淀;③品红溶液褪色;④品红溶液不褪色
A. ①④ B. ①③ C. ①② D. ②④
难度: 简单查看答案及解析
-
能用离子方程式H++ OH-→ H2O 表示的反应是
A. 氨水和盐酸 B. 氢氧化钠溶液和醋酸
C. 硫酸和氢氧化钡溶液 D. 硝酸和澄清石灰水
难度: 中等查看答案及解析
-
常温下pH=2的某酸HA和pH=12的NaOH溶液等体积混合,则所得溶液的pH
A. =7 B. ≥7 C. ≤7 D. 以上均有可能
难度: 中等查看答案及解析
-
NA表示阿伏加德罗常数。硫与浓硝酸反应的化学方程式为:S+6HNO3(浓)→H2SO4+6NO2↑+2H2O,有关说法正确的是
A. 氧化剂与还原剂物质的量之比为1:6 B. 每产生2.24升NO2转移电子0.1NA个
C. 随着反应进行溶液的酸性逐渐增强 D. 氧化性:HNO3(浓)>H2SO4
难度: 简单查看答案及解析

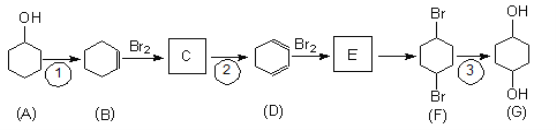
 )______________________
)______________________