-
下列物质的水溶液能导电,但属于非电解质的是( )
A、Cl2 B、CH3COOH C、SO2 D、NaCl
难度: 简单查看答案及解析
-
下列物质互为同分异构体的一组是
A、乙醇和乙酸 B、丁烷和异丁烷 C、12 C与14 C D、金刚石和石墨
难度: 简单查看答案及解析
-
某直链烷烃分子中有18个氢原子,他的分子式是( )
A.、C8H18 B、C9H18 C、 C10H18 D、C11H18
难度: 简单查看答案及解析
-
2012年2月新华网报道,加拿大开发出生产医用放射性同位素9943Tc的简单方法。下列关于99 43Tc的叙述正确的是( )
A、原子序数是99 B、质量数是43 C、中子数是99 D、电子数是43
难度: 简单查看答案及解析
-
用NA表示阿伏加德罗常数的值。下列说法正确的是( )
A、32g O2中含有的分子数为NA
B、标准状况下,22.4 L H2O中含有的分子数为NA
C、1 mol Mg与足量O2反应转移的电子数为NA
D、1 L 1 mol·L-1 CaCl2溶液中含有的氯离子数为NA
难度: 简单查看答案及解析
-
常温下,0.1mol/LCH3COONa溶液中离子浓度最大的是 ( )
A、OH- B、 H+ C、 Na+ D、CH3COO-
难度: 简单查看答案及解析
-
与MgCl2晶体中所含化学键类型相同的是 ( )
A、Na2S B、SiO2 C、HCl D、NH4Cl
难度: 简单查看答案及解析
-
密闭容器中反应CO(g) +H2O(g)
CO2(g) + H2(g)达到平衡,在其他条件不变的情况下,下列措施不能使正反应速率加快的是 ( )
A、通入水蒸气 B、 缩小容器体积 C、分离出CO2 D、升高温度
难度: 简单查看答案及解析
-
用石墨作电极,电解1 mol/L下列物质的溶液,溶液的pH保持不变的是( )
A、HCl B、NaOH C、Na2SO4 D、NaCl
难度: 简单查看答案及解析
-
加入水能抑制水的电离的物质是( )
A、碘化钾 B、氯化钠 C、 硝酸钠 D、硫酸
难度: 简单查看答案及解析
-
下列实验方法正确的是 ( )
A.用NaOH溶液鉴别SO2和CO2
B.用丁达尔效应鉴别FeCl3溶液和Fe(OH)3胶体
C.用Na2CO3溶液鉴别HCl溶液和H2SO4溶液
D.用焰色反应鉴别NaCl和NaNO3
难度: 简单查看答案及解析
-
在铁制品上镀上一定厚度的锌层,以下设计方案正确的是( )
A、锌作阳极,镀件作阴极,溶液中含有锌离子
B、铂作阴极,镀件作阳极,溶液中含有锌离子
C、铁作阳极,镀件作阴极,溶液中含有亚铁离子
D、锌用阴极,镀件作阳极,溶液中含有锌离子
难度: 简单查看答案及解析
-
把a、b、c、d四块金属浸泡在稀H2SO4中,用导线两两相连可以组成各种原电池。若a、b相连时,a上发生氧化反应;c、d相连,d上有气体逸出;a、c相连,a极减轻;b、d相连,H+ 向b极移动。则四种金属的活动顺序为( )
A、a>b>c>d B、a>c>b>d C、a>c>d>b D、b>d>c>a
难度: 简单查看答案及解析
-
下列反应中,△H和△S均大于0的是( )
A、NH3(g) + HCl(g) = NH4Cl(s)
B、CaCO3(s) = CaO(s)+ CO2(g)
C、4Al(s) + 3O2(g) = 2Al2O3(s)
D、NaOH(aq) + HCl(aq) = NaCl(aq) + H2O(l)
难度: 简单查看答案及解析
-
下列说法正确的是( )
A.相对分子质量相同的物质是同种物质
B.分子式相同的不同有机物一定是同分异构体
C.相对分子质量相差14的两种有机物,一定是属于同系物。
D.分子中含有碳与氢元素的化合物是烃类
难度: 简单查看答案及解析
-
下列有关物质用途的说法错误的是( )
A.过氧化钠可用作潜艇里氧气的来源
B.单质硅是光导纤维的主要成分
C.乙醇可用作燃料
D.食醋可用于清除暖水瓶中的水垢
难度: 简单查看答案及解析
-
在一定条件下,对于A2(g)+3B2(g)
2AB3(g)反应来说,以下化学反应速率的表示中,化学反应速率最大的是( )
A.v(A2)=0.8mol·L-1·s-1 B.v(A2)=60mol·L-1·min-1
C.v(AB3)=1.0mol·L-1·s-1 D.v(B2)=1.2mol·L-1·s-1
难度: 简单查看答案及解析
-
下列反应中,属于水解反应且使溶液显酸性的是
A.NH4+ + H2O
NH3·H2O + H+ B.HCO3—+ H2O
CO32- + H3O+
C.S2- + H2O
HS-+ OH- D.NH3 +H2O
NH4+ +OH-
难度: 简单查看答案及解析
-
下列实验装置或操作正确的是( )
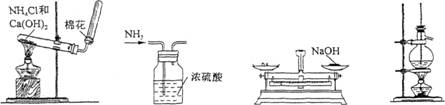
A、制取NH3 B.干燥NH3 C.称量NaOH固体 D.石油的分馏
难度: 简单查看答案及解析
-
某混合溶液中所含离子的物质的量浓度如下表,则M2+可能为 ( )
所含离子
Cl-
SO42-
H+
Mn+
物质的量浓度mol/L
2
1
2
1
A. Mg2+ B.Ba2+ C. Al3+ D.Na+
难度: 简单查看答案及解析
-
X、Y、Z均为短周期元素,它们在周期表中相对位置如图所示。若Y原子的最外层电子是内层电子数的3倍,下列说法正确的是( )
A.X的气态氢化物比Y的稳定 B.X与Y形成的化合物都易溶于水
C.Z的非金属性比Y的弱 D.原子半径:X>Y>Z>W
难度: 简单查看答案及解析
-
下列溶液一定呈中性的是( )
A、c(H+)=10-7mol/L的溶液 B、pH=7的溶液
C、c(H+)/c(OH-)=10-14的溶液 D、氨水与氯化铵的混合液中c(NH4+)=c(Cl-)
难度: 简单查看答案及解析
-
常温下列各种溶液中,可能大量共存的离子组是( )
A、pH=0的溶液中:Fe2+、NO3-、SO42-、I-
B、由水电离出的c(H+)=1×10-13mol·L-1的溶液中:Na+、AlO2-、S2-、CO32-
C、含有大量Fe3+的溶液中:Na+、I-、K+、NO3-
D、能使PH试纸显红色的溶液:Mg2+、SO42-、Na+、Cl-
难度: 简单查看答案及解析
-
关于盐类水解反应的说法正确的是( )
A、溶液呈中性的盐一定是强酸与强碱生成的盐
B、含有弱酸根离子的盐的水溶液一定呈碱性
C、盐溶液的酸碱性主要决定于形成盐的酸、碱电离程度的相对大小
D、Na2 S水解的离子方程式为:S2-+2H2O
H2S+2OH-
难度: 简单查看答案及解析
-
在0.1mol/L的氨水中存在 NH3·H2O
NH4++OH-的电离平衡,下列措施都能使该平衡向右移动的一组是 ( )
①加入少量HCl ②加入固体NaOH ③加水 ④通入氨气
⑤加热升高温度 ⑥加入NH4NO3
A、①③④⑤ B.①③④⑤⑥ C.②③④⑤ D.①③④⑥
难度: 简单查看答案及解析
-
将分别盛有熔融的氯化钾、氯化镁、氧化铝的三个电解槽串联,在一定条件下通电一段时间后,析出钾、镁、铝的物质的量之比为 ( )
A、1∶2∶3 B、3∶2∶1 C、6∶3∶1 D、6∶3∶2
难度: 简单查看答案及解析
-
下列说法正确的是( )
A、凡是放热反应都是自发的
B、难溶电解质的溶解平衡是一种动态平衡
C、利用沉淀反应除杂时,可使杂质离子完全沉淀
D、pH=5的盐酸稀释1000倍后,溶液的pH增到8
难度: 简单查看答案及解析
-
mA(g)+nB(g)
pC(g)+qQ(g)当m、n、p、q为任意整数时,达到平衡的标志是( )
①体系的压强不再改变 ②绝热体系的温度不再改变 ③各组分的浓度不再改变
④各组分的质量分数不再改变 ⑤反应速率vA: vB: vC: vD = m:n:p:q
⑥单位时间内m mol A断键反应,同时p mol C也断键反应
A.③④⑤⑥ B.②③④⑥ C.①③④⑤ D.①③④⑥
难度: 简单查看答案及解析
-
碱性电池具有容量大、放电电流大的特点,因而得到广泛应用。锌-锰碱性电池以氢氧化钾溶液为电解液,电池总反应式为:Zn(s)+2MnO2(s)+H2O(l)=Zn(OH)2(s)+Mn2O3(s)。则下列说法正确的是( )
A.电池工作时,MnO2发生还原反应
B.电池负极的电极反应式为:2MnO2+H2O+2e-→Mn2O3+2OH-
C.电池工作时,K+移向负极
D.电池工作时,电路中每通过0.1mol电子,锌的质量理论上减少6.5g
难度: 简单查看答案及解析