-
下列叙述中属于物质化学性质的是( )
A.镁在空气中燃烧
B.水能结成冰
C.硫酸具有酸性
D.干冰升华难度: 中等查看答案及解析
-
下列气体在焊接金属时不能用作保护气的是( )
A.氮气
B.二氧化碳
C.氦
D.氖难度: 中等查看答案及解析
-
下列有关媒体的报道与化学知识不相违背的( )
A.某洗发水不含任何化学物质
B.科研机构发明了一种用植物秸秆生产乙醇的新工艺
C.有关部门利用明矾对饮用水进行消毒杀菌,从而解决了灾民饮水难的问题
D.科研人员发明了一种特殊催化剂,可以使水变为汽油难度: 中等查看答案及解析
-
下列有关分子和原子的说法中,正确的是( )
A.原子是由质子和中子构成的
B.保持水的化学性质的粒子是氢原子和氧原子
C.分子的质量总比原子的质量大
D.分子和原子都可以构成物质难度: 中等查看答案及解析
-
锌铬黄(化学式:ZnCrO4)常用于制防锈涂料.锌铬黄中铬元素的化合价为( )
A.+1
B.+2
C.+6
D.+7难度: 中等查看答案及解析
-
下列实验操作正确的是( )
A.
称量固体
B.
用橡皮塞塞住试管
C.
加热液体
D.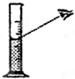
量取液体难度: 中等查看答案及解析
-
在水溶液中,一般不会与其它物质发生复分解反应的是( )
A.NaCl
B.KNO3
C.NaOH
D.H2SO4难度: 中等查看答案及解析
-
某微粒的结构示意图如图所示,下列有关该微粒的说法错误的是( )
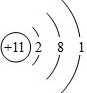
A.该微粒的原子核外电子数为11
B.该图表示的微粒是一种原子
C.该微粒属于非金属元素
D.该微粒在化学反应中易失去1个电子难度: 中等查看答案及解析
-
下列说法正确的是( )
A.氧气用于火箭发射是利用氧气的可燃性
B.一氧化碳用于炼铁是因为它能与铁的氧化物发生置换反应
C.常温下,白磷放置在空气一段时间能自然的原因是白磷的着火点低于常温
D.二氧化碳用于灭火,是由于二氧化碳不可燃、不助燃且密度比空气大难度: 中等查看答案及解析
-
往Cu(NO3)2、Zn(NO3)2的混合溶液中加入一些铁粉,待反应完成后再过滤,不可能的情况是( )
A.滤纸上有Cu,滤液中有Cu2+、Zn2+、Fe2+
B.滤纸上有Cu,滤液中有Zn2+、Fe2+
C.滤纸上有Cu、Fe,滤液中有Cu2+、Zn2+、Fe2+
D.滤纸上有Cu、Fe,滤液中有Zn2+、Fe2+难度: 中等查看答案及解析
-
“三效催化转换器”可将汽车尾气中的有毒气体处理为无污染的气体,下图为该反应的微观示意图(未配平),其中不同符号的球代表不同种原子.下列说法不正确的是( )

A.乙和丙中所含元素种类相同
B.甲和丁中同种元素化合价不相等
C.该反应中共有三种元素
D.化学方程式中乙、丁的化学计量数均为1难度: 中等查看答案及解析
-
下列物质按单质、氧化物、化合物、混合物的顺序排列的是( )
A.金刚石、生石灰、粗食盐、冰水
B.水银、干冰、熟石灰、天然气
C.苛性钠、铁锈、纯碱、石油
D.硫磺、液态氧、粗食盐、胆矾难度: 中等查看答案及解析
-
下列有关物质的鉴别、分离、提纯所用的试剂或方法错误的是( )
选项 实验目的 所用试剂或方法 A 鉴别硝酸铵固体和氢氧化钠固体 水 B 区分失去标签的浓硫酸和稀硫酸 水或小木条 C 除去生石灰中含有的杂质石灰石 水或稀盐酸 D 从H2O2溶液制取氧气的残余物中分离出MnO2 过滤或蒸发
A.A
B.B
C.C
D.D难度: 中等查看答案及解析
-
向4支装有质量和质量分数均相同的稀硫酸的试管中,分别加入适量的Mg、MgO、Mg(OH)2、MgCO3,反应完全后(反应物均完全反应),对应得到①②③④四个溶液,则其中浓度最大的是( )
A.①
B.②
C.③
D.④难度: 中等查看答案及解析


