-
下列叙述正确的是
A. CO和CaO分别属于酸性氧化物和碱性氧化物
B. 蒸馏和蒸发分别可以从海水中得到淡水和粗盐
C. 自然固氮和人工固氮分别是物理变化和化学变化
D. 石油分馏可获得乙烯、苯及其衍生物
难度: 简单查看答案及解析
-
2010年上海世博会中国馆——“东方之冠”的主体结构为四根巨型钢筋混凝土制成的核心筒。其中的钢属于

A. 合金 B. 复合材料 C. 纯净物 D. 有机材料
难度: 简单查看答案及解析
-
实验室用氯化铵和消石灰制氨气的装置和下列哪种制气装置相同
A. 加热氯酸钾、二氧化锰混合物制O2
B. 石灰石和稀盐酸反应制CO2
C. MnO2催化过氧化氢溶液分解制O2
D. MnO2与浓HCl加热制取氯气
难度: 简单查看答案及解析
-
能正确表示下列化学反应的离子方程式的是
A.铁与稀盐酸反应: 2Fe + 6H+ = 2Fe3+ + 3H2↑
B.铝粉投入到NaOH溶液中: 2Al+2OH- + 6H2O ══ 2[Al(OH)4]-+3H2↑
C.氯化铁溶液中加入铁粉: 2Fe3+ + Fe══3Fe2+
D.AlCl3溶液中加入足量的氨水: Al3++ 3OH- ══ Al(OH)3↓
难度: 困难查看答案及解析
-
用聚光手电筒照射下列分散系,可观察到丁达尔效应的是
A.KOH溶液 B.Fe(OH)3胶体 C.盐酸 D.NaNO3溶液
难度: 简单查看答案及解析
-
下列各组物质中,化学键类型完全相同的是
A. N2和NaOH B. CO2和H2O
C. MgO和NH4Cl D. HCl和KCl
难度: 简单查看答案及解析
-
下列有关化学反应速率和限度的说法中,不正确的是
A. 实验室用H2O2分解制O2,加入MnO2后,反应速率明显加快
B. 在金属钠与足量水反应中,增加水的量能加快反应速率
C. 2SO2+O2
2SO3反应中,SO2的转化率不能达到100%
D. 实验室用碳酸钙和盐酸反应制取CO2,用碳酸钙粉末比块状反应要快
难度: 简单查看答案及解析
-
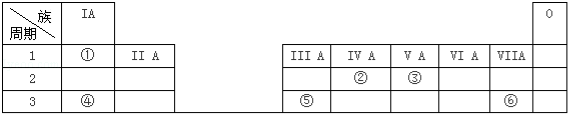
已知同周期X、Y、Z三种元素的最高价氧化物对应水化物酸性由强到弱的顺序为HXO4>H2YO4>H3ZO4,则下列判断中正确的
A. 元素非金属性按X、Y、Z的顺序增强
B. 阴离子的半径按X、Y、Z的顺序增大
C. 气态氢化物的稳定性按X、Y、Z的顺序增强
D. 单质的氧化性按X、Y、Z的顺序增强
难度: 简单查看答案及解析
-
下列叙述中正确的是
A. 碳单质有同素异形体,氧单质没有
B. 在氧化还原反应中,非金属单质一定是氧化剂
C. 某元素从化合态变为游离态时,该元素一定被还原
D. 可以用萃取的方法将溴单质或碘单质从它们的水溶液中提取出来
难度: 简单查看答案及解析
-
日本福岛核电站泄漏的核燃料衰变产物有放射性元素
、
等,其中
是个双刃剑,医院可以用它来治疗甲状腺癌;但是如果没有癌症,它也可能诱发甲状腺癌。下列有关说法中不正确的是
A. 碘131I原子核所含中子数是78
B. 核能的利用证实原子的可分性
C. 碘127I原子和放射性碘原子131I属于同位素
D. 碘127I原子和碘131I原子的质子数不同
难度: 简单查看答案及解析
-
下列有关物质检验的实验结论正确的是
实 验 操 作
现 象
实 验 结 论
A
向某溶液中加入硝酸酸化的氯化钡溶液
生成白色沉淀
溶液中一定含有SO42-
B
将某气体通入品红溶液中
品红溶液褪色
该气体一定是SO2
C
往某溶液中加入KSCN溶液
显血红色
溶液中一定含有Fe3+
D
往某溶液中加入盐酸
产生无色气体
溶液中一定含有CO32-
A. A B. B C. C D. D
难度: 简单查看答案及解析
-
用铜、银和硝酸银溶液设计一个原电池,下列对该原电池的判断正确的是
A.铜作负极被氧化 B.银为正极被还原
C.正极反应为:Ag+ + e-=Ag D.NO3-向正极移动
难度: 简单查看答案及解析
-
设NA表示阿伏加德罗常数值,下列叙述正确的是
A.NA个氧气分子和NA个氢气分子的质量比为16∶1
B.标准状况下,22.4LH2O含有的分子数为NA
C.11.2L 氯气中含有的原子数为NA个
D.2L 1mol/L Na2SO4溶液中Na+离子数为2NA个
难度: 简单查看答案及解析
-
工业上制取ClO2的化学反应:2NaClO3 + SO2 + H2SO4 = 2ClO2 + 2NaHSO4,下列说法正确的是
A. SO2在反应中作还原剂 B. NaClO3在反应中被氧化
C. H2SO4 在反应中作氧化剂 D. 1mol氧化剂在反应中失去1mol电子
难度: 简单查看答案及解析
-
结合SO2的特点,分析以下对SO2的物质分类及其性质的预测中,不正确的是
①碱性氧化物 可与烧碱反应生成盐和水 ② 非电解质 熔融状态不导电
③电解质 水溶液能导电 ④ 酸性氧化物 可与水反应生成酸
A.①② B.③④ C.①③ D.②④
难度: 中等查看答案及解析
-
下列反应所得溶液中一定只含一种溶质的是
A.向NaOH溶液中通入CO2
B.向Ca(OH)2溶液中通入Cl2
C.向蒸馏水中加入少量金属Na
D.向MgSO4溶液中滴入NaOH溶液
难度: 简单查看答案及解析