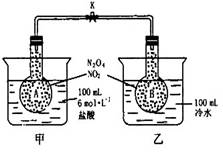
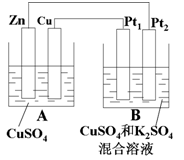
-
下列说法正确的是
A.将AlCl3溶液蒸干并灼烧后得到的物质是Al(OH)3
B.向饱和AgCl水溶液中加入盐酸,Ksp值变大
C.温度一定时,当溶液中Ag+和Cl-浓度的乘积等于Ksp值时,此溶液为AgCl的饱和溶液
D.所谓沉淀完全就是用沉淀剂将溶液中某一离子除净;
难度: 简单查看答案及解析
-
下列说法或表示方法正确的是
A.等物质的量的硫蒸气和固体硫分别完全燃烧,后者放出热量多
B.由C(石墨)= C(金刚石);△H=+1.90 kJ/mol可知,金刚石比石墨稳定
C.在101kPa时,2g氢气完全燃烧生成液态水,放出285.8kJ热量,氢气燃烧的热化学方程式表示为:2H2(g)+O2(g)= 2H2O(l) △H=-285.8kJ/mol
D.在稀溶液中,H+(aq)+ OH-(aq) = H2O(l) △H=-57.3kJ/mol,若将含0.5molH2SO4的浓硫酸与含1molNaOH的溶液混合,放出的热大于57.3kJ
难度: 简单查看答案及解析
-
下列各式中属于正确的水解反应的离子方程式的是
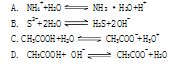
难度: 简单查看答案及解析
-
盐酸、醋酸和碳酸氢钠是生活中常见的物质,下列表述正确的是
A.在NaHCO3溶液中加入与其等物质的量的NaOH,溶液中的阴离子只有CO32-和OH-
B.将pH相同的盐酸和醋酸稀释相同倍数,醋酸的pH变化大
C.10 mL0.10 mol·L-1CH3COOH溶液加入等物质的量的NaOH后,溶液中离子的浓度由大到小的顺序是:c(Na+)>c(CH3COO-)>c(OH-)>c(H+)
D.中和体积与pH都相同HCl溶液和CH3COOH溶液所消耗NaOH物质的量相同
难度: 简单查看答案及解析
-
一定条件下,在体积为10 L的密闭容器中,1 mol X和1 mol Y进行反应:
,经60 s达到平衡生成0.3 mol Z,下列说法正确的是
A.以X浓度变化表示的反应速率为0.001 mol/(L·s)
B.将容器体积变为20 L,Z的平衡浓度变为原来的1/2
C.若增大压强,则物质Y的转化率减小
D.若升高温度,X的体积分数增大,则该反应的DH>0
难度: 简单查看答案及解析
-
体积相同的甲、乙两个容器中,分别都充有等物质的量的SO2和O2,在相同温度下发生反应:
,并达到平衡。在这过程中,甲容器保持体积不变,乙容器保持压强不变,若甲容器中SO2的转化率为p%,则乙容器中的转化率是
A. 等于p% B. 大于p% C. 小于p% D. 无法判断
难度: 简单查看答案及解析
-
某温度下重水(D2O)的离子积常数为1.6×10-15,用定义pH一样来规定
pD=-lg{c(D+)},则该温度下,下列叙述正确的是
A.纯净的重水(D2O)中,pD=7
B.1 L溶解有0.01 mol DCl的重水溶液,其pD=12.0
C.纯净的重水中,c(D+)=c(OD-)
D.1 L溶解有0.01 mol NaOD的重水溶液,其pD=12.0
难度: 简单查看答案及解析
-
在密闭容器中,反应
达到平衡后,若增大A的浓度或增大压强使平衡向右移动。下列说法中正确的是
A.C的百分含量一定增大
B. C的浓度一定增大
C.A的百分含量一定增大
D.A的转化率一定增大
难度: 简单查看答案及解析
-
在容积一定的密闭容器中,可逆反应:
符合下列图Ⅰ所示关系。由此推断,对图Ⅱ的说法正确的是
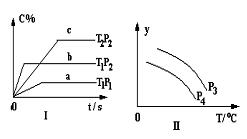
A.P3<P4,Y轴表示A2的转化率
B.P3<P4,Y轴表示A2的浓度
C.P3>P4,Y轴表示混合气体的密度
D.P3>P4,Y轴表示混合气体的平均摩尔质量
难度: 简单查看答案及解析
-
向10 mL 0.1mol·L-1的Na2CO3溶液中通入22.4mL(标准状况)CO2,当气体全部溶解时,溶液中粒子浓度关系正确的是
A.c(Na+)>c(CO32-)>c(HCO3-)>c(OH-)>c(H+)
B.c(HCO3-)=c(Na+)>c(OH-)>c(H+)
C.c(Na+)=c(HCO3-)+c(CO32-)+c(H2CO3)
D.c(OH-)=c(HCO3-)+2c(H2CO3)+c(H+)
难度: 简单查看答案及解析
-
常温下,0.1 mol·L-1某一元酸(HA)溶液中
=1×10-8,下列叙述正确的是
A.溶液中水电离出的c(H+)=10-10 mol·L-1
B.溶液中c(H+)+c(A-)=0.1 mol·L-1
C.与0.05 mol·L-1 NaOH溶液等体积混合后所得溶液中离子浓度大小关系为:c(A-)>c(Na+)>c(OH-)>c(H+)
D.上述溶液中加入一定量CH3COONa晶体或加水稀释,溶液c(OH-)均增大
难度: 简单查看答案及解析
-
下列各组中的比值等于2︰1的是
A.pH为12的烧碱溶液与Ba(OH)2溶液的物质的量浓度之比
B.K2S溶液中c(K+)与c(S2-)之比
C.相同温度下0.2mol/L醋酸溶液与0.1mol/L醋酸溶液中的c(H+)之比
D.10mL0.5mol/L的盐酸与5mL0.5mol/L的盐酸溶液中的c(H+)之比
难度: 简单查看答案及解析
-
将20mL0.4 mol·L-1硝酸铵溶液跟50mL 0.1 mol·L-1氢氧化钡溶液混合,则混合溶液中各离子浓度的大小顺序是
A.c(NO3-)> c(OH-)> c(NH4+) > c(Ba2+)
B.c(NO3-) > c(Ba2+) > c(OH-) > c(NH4+)
C.c(Ba2+) > c(NO3-) > c(OH-) > c(NH4+)
D.c(NO3-) > c(Ba2+) > c(NH4+) > c(OH-)
难度: 简单查看答案及解析
-
下列叙述正确的是
A.0.1mol·L-1氨水中,c(OH-)= c(NH4+)
B.10 mL 0.02mol·L-1HCl溶液与10 mL 0.02mol·L-1Ba(OH)2溶液充分混合,若混合后溶液的体积为20 mL,则溶液的pH=10
C.在0.1mol·L-1CH3COONa溶液中,c(OH-)= c(CH3COOH)+c(H+)
D.0.1mol·L-1某二元弱酸强碱盐NaHA溶液中,
c(Na+)= 2c(A2-)+c(HA-)+c(H2A)
难度: 简单查看答案及解析
-
甲溶液的pH=6,乙溶液的pH=2,则下列叙述正确的是
A.甲、乙两溶液的c(H+)之比为400︰1
B.甲、乙两溶液均呈酸性
C.甲中水的电离程度小于乙中水的电离程度
D.甲中水的电离程度与乙中水的电离程度无法比较
难度: 简单查看答案及解析
-
已知①CH3COOH与CH3COONa等物质的量混合配成的稀溶液,pH为4.7;②用等物质的量的HCN和NaCN配成的稀溶液中,c(CN-) < c(Na+),则下列说法不正确的是
A. CH3COONa的水解趋势大于CH3COOH的电离趋势
B. NaCN的水解趋势大于HCN的电离趋势
C. ②溶液中,c(H+)<c(OH-)
D. CH3COONa的存在抑制了CH3COOH的电离
难度: 简单查看答案及解析
-
已知一种c(H+)=1×10-3mol/L的酸和一种c(OH-)=1×10-3mol/L的碱溶液等体积混合后溶液呈酸性其原因可能是
A.生成了一种强酸弱碱盐 B.等浓度的强酸和弱碱溶液反应
C.浓的强酸和稀的强碱溶液反应 D.浓的弱酸和稀的强碱溶液反应
难度: 简单查看答案及解析
-
在下列溶液中,各组离子一定能够大量共存的是
A.使酚酞试液变红的溶液: Na+、Cl-、SO42-、Fe3+
B.使紫色石蕊试液变红的溶液:Fe2+、Mg2+、NO3-、Cl-
C.c(H+)=10-12 mol·L-1的溶液:K+、Ba2+、Cl-、Br-
D.Fe3+ 、K+、SO42-、CO32-
难度: 简单查看答案及解析
-
埋在地下的输油铸铁管道,在下列各种情况下,腐蚀速度最快的是
A.在潮湿的酸性土壤中 B.在潮湿不透气的中性土壤中
C.在干燥致密不透气的土壤中 D.在潮湿透气的盐碱地中
难度: 简单查看答案及解析
-
将102 g由氮气和氢气按1:3的物质的量之比组成的混合气体,在一定条件下通入密闭容器中反应,当
达到平衡后,平衡混合气体平均相对分子质量为12.5,则其中含氨的质量为
A.32.64 g B.65.28 g C. 3.84 g D. 38.4 g
难度: 简单查看答案及解析