-
市场上销售的加碘食盐、含氟牙膏、高钙牛奶、补铁酱油等,说明了化学与人体的健康密不可分.这里的碘、氟、钙、铁是指( )
A.单质
B.分子
C.元素
D.原子难度: 中等查看答案及解析
-
对分子、原子、离子的下列认识,其中正确的是( )
A.氢原子是最小的微粒,不可再分
B.镁原子的质子数大于镁离子的质子数
C.当液态水变成冰,水分子间不存在间隔
D.分子、原子、离子都可以直接构成物质难度: 中等查看答案及解析
-
下列物质中,属于纯净物的是( )
A.洁净的空气
B.澄清石灰水
C.蒸馏水
D.鲜橙汁难度: 中等查看答案及解析
-
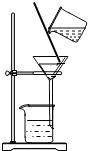
下图所示的四种变化中,与其他三种不同的是( )
A. 石油分馏
石油分馏
B.
净化水
C.
蒸发食盐水
D.
铁丝在氧气中燃烧难度: 中等查看答案及解析
-
根据微粒结构图给出的信息,下列说法错误的是( )
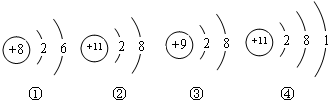
A.①④是原子
B.②③具有相对稳定结构
C.③是阳离子
D.②④属于同种元素难度: 中等查看答案及解析
-
木糖醇(C5H12O5)是一种广泛用于口香糖的防龋齿食品.下列有关木糖醇的说法不正确的是( )
A.一个木糖醇分子中含有22个原子
B.木糖醇的相对分子质量为152g
C.木糖醇由碳、氢、氧三种元素组成
D.木糖醇属于有机化合物难度: 中等查看答案及解析
-
下列化学用语中,正确的是( )
A.2个氢离子:H2+
B.氧化铁的化学式:Fe2O3
C.NaNO2中氮元素的化合价为+5价
D.加热高锰酸钾制取氧气的化学方程式:2KMnO42K2MnO3+MnO2+O2↑
难度: 中等查看答案及解析
-
配制质量分数为20%的食盐水30g,需要食盐的质量和水的体积(水的密度为1g/mL)分别为( )
A.6g,24mL
B.0.6g,29.4mL
C.20g,80mL
D.20g,100mL难度: 中等查看答案及解析
-
某环保监测站取刚降下的雨水,每隔一定时间测定其pH,数据如下:
下列有关说法不正确的是( )测定时间/分钟 1 2 4 5 pH 4.73 4.62 4.56 4.55 4.55
A.雨水酸性逐渐减弱
B.酸雨是由于空气受硫的氧化物或氮的氧化物污染形成的
C.酸雨可腐蚀某些建筑物和金属制品
D.一段时间后雨水酸性渐趋稳定难度: 中等查看答案及解析
-
下列反应属于化合反应的是( )
A.电解水制备氢气
B.木炭与氧化铜混合加热得到金属铜
C.一氧化碳在空气中燃烧得到二氧化碳
D.煅烧碳酸钙固体得到二氧化碳难度: 中等查看答案及解析
-
配制一定溶质质量分数的溶液不需用到的仪器是( )
A.(玻璃棒)
B.
C.
D.难度: 中等查看答案及解析
-
工业酒精中含有一种能使人失明的物质X,X燃烧的化学方程式为:2X+3O2
2CO2+4H2O,据此可以推断X的化学式为( )
A.CO
B.CH3OH
C.C2H5OH
D.CH4难度: 中等查看答案及解析
-
欲除去物质中的少量杂质(括号内为杂质),所采取的方法和反应的基本反应类型均正确的是( )
选项 物质 加入的试剂和操作 基本反应类型 (A) CuO(Cu) 足量稀盐酸,过滤 复分解反应 (B) CaO(CaCO3) 高温煅烧 分解反应 (C) Cu(NO3)2溶液(A gNO3) 足量铜粉,过滤 置换反应 (D) CO2(CO) 氧气,点燃 化合反应
A.选A
B.选B
C.选C
D.选D难度: 中等查看答案及解析
-
端午节前,国家食品监督部门检出一种由“返青棕叶”包装的粽子.这种“返青棕叶”多以硫酸铜为添加物,含砷、铅、汞等重金属元素,长期食用有害健康.硫酸铜是一种( )
A.氧化物
B.酸
C.碱
D.盐难度: 中等查看答案及解析
-
将铁粉加到一定量AgNO3、Cu(NO3)2的混合溶液中,充分反应后过滤,向滤渣中加入稀盐酸发现有气体逸出,则滤渣的组成成分是( )
A.铁
B.铁和铜
C.铁、铜、银
D.铁和银难度: 中等查看答案及解析
-
下列说法中错误的是( )
A.可燃物达到一定温度就可以燃烧
B.铁在潮湿的空气中容易生锈
C.回收废电池可减少对环境的污染
D.煤和石油都是重要的化工原料难度: 中等查看答案及解析
-
常温下,下列各组物质中相互间不能发生化学反应的是( )
A.铁和潮湿氧气
B.铁和硫酸铜溶液
C.二氧化碳和熟石灰
D.铜和稀盐酸难度: 中等查看答案及解析
-
在学习过程中,总结规律要严谨、全面、科学.下列总结出的规律符合这一要求的是( )
A.酸溶液一定显酸性
B.某物质一定温度时的浓溶液一定是饱和溶液
C.含有氧元素的化合物一定是氧化物
D.有单质生成的反应一定是置换反应难度: 中等查看答案及解析
-
向分别盛有少量氯化钾、氯化钡、碳酸钾溶液的三支试管中,滴入2~3滴某种试液,便能区别这三种溶液.该试液是( )
A.硝酸银溶液
B.氢氧化钙溶液
C.盐酸溶液
D.硫酸溶液难度: 中等查看答案及解析
-
某中学九年级A,B两班同学做常见酸和碱与指示剂反应的实验,使用的试剂如图所示.实验后废液分别集中到废液缸中.某研究小组对此废液进行了检测,结果如下:
请你根据实验现象判断,对该废液的成分的说法错误的是( )废液来源 检测方法和结果 A班 观察废液呈无色 B班 观察废液呈红色 
A.A班废液中一定含有盐酸
B.废液中一定含有的物质氯化钠
C.B班废液的成分中肯定没有盐酸
D.B班废液中可能含有氢氧化钙难度: 中等查看答案及解析