-
党的十九大报告中提出加快生态文明体制改革,建设美丽中国,坚持人与自然和谐共生。下列有关观念或做法不宜提倡的是
A. 青山绿水就是金山银山 B. 创建环境友好型社会人人有责
C. 大力开发森林资源,发展乡村旅游 D. 积极做好治沙工作,做到人进沙退
难度: 简单查看答案及解析
-
美国犹他州立大学(USU)和俄罗斯南联邦大学的科学家,利用计算机模型设计出比水还轻的超轻晶体铝,这种超轻晶体铝属于
A. 有机物 B. 单质 C. 化合物 D. 氧化物
难度: 简单查看答案及解析
-
下列过程以涉及化学变化为主的是
A. 积沙成塔 B. 沙里淘金 C. 海市蜃楼 D. 水果催熟
难度: 简单查看答案及解析
-
日本福岛第一核电站泄露出微量的放射性元素
。关于
的叙述正确的是
A. 核电荷数是239 B. 质子数是145
C. 中子数是94 D. 电子数是94
难度: 简单查看答案及解析
-
下列气体中,只能用排空气法收集的是
A. NO2 B. O2 C. NO D. H2
难度: 简单查看答案及解析
-
下列属于含有共价键的化合物的是
A. N2 B. CaCl2 C. KF D. NaOH
难度: 简单查看答案及解析
-
下列化学用语表示正确的是
A. 葡萄糖的实验式:CH2O
B. 氯离子的结构示意图:
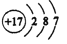
C. 乙醇分子的结构式:
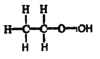
D. Na2S的电子式:
难度: 简单查看答案及解析
-
下列有机物属于髙分子化合物的是
A. 水果中含有的维生素C B. 石油中含有的C16H34
C. 芹菜中含有的纤维素 D. 植物油中含有的油脂
难度: 简单查看答案及解析
-
下列常见物质的俗名与化学式对应正确的是
A. 纯碱——NaOH B. 生石灰——Ca(OH)2
C. 胆矾——CuS04 D. 石英——SiO2
难度: 简单查看答案及解析
-
在含有较多NH4+、SO32-、NO3-的某澄清透明溶液中,能够大量共存的离子是
A. Ba2+ B. Na+ C. ClO- D. OH-
难度: 简单查看答案及解析
-
工业上常用浓氨水检查氯气管道是否泄漏,发生反应为:8NH3 +3C12=N2+6NH4C1, 该反应属于
A. 置换反应 B. 分解反应 C. 化合反应 D. 复分解反应
难度: 简单查看答案及解析
-
下列反应中,既属于氧化还原反应又属于吸热反应的是
A. Ba(0H)2•8H20与NH4Cl反应 B. 工业合成氨
C. 灼热的炭与CO2反应 D. 葡荀糖在人体内生理氧化
难度: 简单查看答案及解析
-
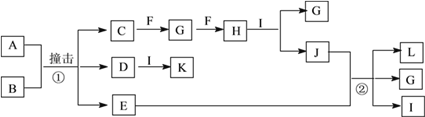
如图:W、X、Y、Z为四种物质,若箭头表示能一步转化的常见反应,其中常温下能实现图示转化关系的是
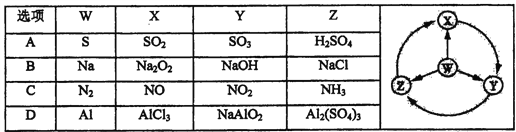
A. A B. B C. C D. D
难度: 中等查看答案及解析
-
反应SO2+O2=2SO3在密闭容器中进行。下列关于该反应的说法正确的是
A. 增大压强能减慢反应速率
B. v(SO2):v(O2)=2:1证明该反应已达到化学平衡状态
C. 当反应物和生成物浓度不变时,反应已达平衡
D. 增大02的浓度可使SO2完全转化
难度: 简单查看答案及解析
-
实验室用下图所示装置制取并收集氨气,下列说法正确的是 ( )
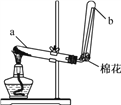
A. 试管a中的固体为氯化铵
B. 用湿润的红色石蕊试纸检验试管b中氨气是否集满
C. 氨气可用浓硫酸干燥
D. 如图装置也可用于制取并收集氧气
难度: 中等查看答案及解析
-
火法炼铜的主要反应原理:Cu2S+O2=2Cu+SO2,下列说法正确的是
A. Cu是还原产物 B. SO2只是还原产物
C. 氧化剂只有O2 D. 1molS02生成转移4 mol电子
难度: 中等查看答案及解析
-
下列有关物质的性质和应用对应关系正确的是
A. 晶体硅熔点高、硬度大,是制造太阳能电池和计算机芯片的主要材料
B. 氧化铝熔点高,常用于耐高温材料
C. 明矾溶于水能形成胶体,可用于自来水的杀菌消毒
D. 苏打溶液呈弱碱性,可用作胃酸中和剂
难度: 简单查看答案及解析
-
用下列实验装置进行相应实验,能达到实验目的的是
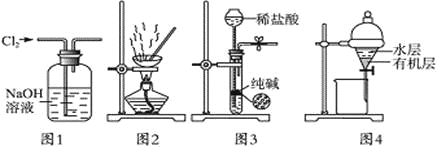
A. 用图1所示装置除去Cl2中含有的少量HCl
B. 用图2所示装置蒸干NH4Cl饱和溶液制备NH4Cl晶体
C. 用图3所示装置制取少量纯净的CO2气体
D. 用图4所示装置分离CCl4萃取碘水后已分层的有机层和水层
难度: 中等查看答案及解析
-
下列反应的离子方程式书写正确的是
A. 过量SO2通入氢氧化钙溶液中:OH﹣+SO2═HSO3﹣
B. 碳酸钙与足量醋酸反应:CaCO3+2H+═Ca2++H2O+CO2↑
C. 氯化铝溶液与过量氨水反应:Al3++4NH3•H2O═AlO2﹣+4NH4++2H2O
D. 铁与稀硫酸溶液反应:2Fe+6H+═2Fe3++3H2↑
难度: 简单查看答案及解析
-
下列物质转化是通过加成反应实现的是
A.
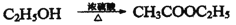
B.
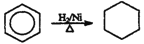
C.

D.

难度: 简单查看答案及解析
-
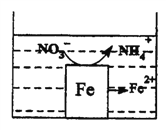
新型液氨燃料电池示意图如图,下列有关说法不正确的是

A. 该装置将化学能转化为电能
B. 氨气在电极1上发生氧化反应
C. 电子由电极2经负栽流向电极1
D. 电极2的反应式为:02+4e-+2H20=40H-
难度: 简单查看答案及解析
-
短周期元素X、Y、Z、W、Q原子序数依次增大,X原子电子数与电子层数相同,Y原子最稿正价与最低负价的代数和为2,Z为地壳中含量最高的元素,Q与Z同一主族,五种元素原子最外层电子数之和为21。下列说法正确的是
A. 原子半径大小顺序:r(W)>r(Z)>r(Y)
B. X、Y、Z三种元素形成的化合物中不可能含离子键
C. 工业上常用电解法生产W的单质
D. 简单氢化物的热稳定性:Q>Z
难度: 中等查看答案及解析
-
铁、铜混合粉末17.6 g加入到800mL 1.0mol/L的 FeCl3溶液中,充分反应后,所得溶液中Fe2+和Cu2+物质的量浓度之比为8∶1。下列有关说法正确的是
A. 混合粉末中铁与铜的物质的量之比是1∶2
B. 反应后的溶液最多还可以溶解铁粉5.6g
C. 反应后所得溶液中c(Fe2+)=1.0mol/L (假设反应前后溶液体积无变化)
D. 向反应后的溶液中加入2.0 mol/L NaOH溶液至金属离子恰好全部沉淀时,需加入NaOH溶液的体积是1.6 L
难度: 困难查看答案及解析