-
在丹麦首都哥本哈根召开的联合国气候变化大会,焦点议题之一是发展“低碳经济”,减少温室气体排放。你认为下列做法中.不能有效减少空气中CO2含量的是
A.开发利用太阳能、风能、生物能、海洋能等清洁能源
B.使用节能产品,推广节能环保汽车
C.植树造林,增加森林植被面积
D.用脱硫处理的煤代替原煤作燃料
难度: 中等查看答案及解析
-
下列说法正确的是
A.IA族元素的金属性一定比IIA族元素的金属性强
B.ⅥA族元素中氢化物最稳定的其沸点一定最高
C.非金属元素只能形成共价化合物
D.短周期中,同周期元素的离子半径从左到右逐渐减少
难度: 中等查看答案及解析
-
已知在酸性条件下能发生下列反应:Cu+→Cu+Cu2+(未配平)。NH4CuSO3与足量的10 mol/L硫酸溶液混合微热,产生下列现象:①有红色金属生成;②有刺激性气味气体产生;③溶液呈蓝色。据此判断下列说法一定合理的是
A.该反应显示硫酸具有酸性
B.NH4CuSO3中硫元素被氧化
C.刺激性气味的气体是氨气
D.反应中硫酸作氧化剂
难度: 中等查看答案及解析
-
下列有关化学用语使用正确的是
A.氧的原子结构示意图:
B.苯分子的比例模型:
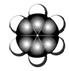
C.乙烯的最简式: C2H4 D.质量数为35的氯原子:
难度: 简单查看答案及解析
-
下列说法中,错误的是
A.蔗糖、淀粉、纤维素水解的最终产物都只是葡萄糖
B.误服重金属盐,立即服用牛奶或豆浆可解毒
C.油脂、乙酸乙酯都属于酯类,但不是同系物
D.煤的干馏可以得到苯、甲苯等芳香烃
难度: 简单查看答案及解析
-
下列各组离子在指定溶液中能大量共存的是
①无色溶液中:K+、Na+、MnO4-、SO42-
②pH=11的溶液中:CO32-、Na+、AlO2-、NO3-
③加入Al能放出H2的溶液中:Cl-、HCO3-、SO42-、NH4+
④由水电离出的c(OH-)=10-13mol·L-1的溶液中:Na+、Ba2+、Cl-、Br-
⑤有较多Fe3+的溶液中:Na+、NH4+、SCN-、HCO3-
⑥酸性溶液中:Fe2+、Al3+、NO3-、I-、Cl-
A.①② B.③⑥ C.②④ D.⑤⑥
难度: 简单查看答案及解析
-
下列实验操作或对实验事实的叙述正确的有几个
①用氨水清洗做过银镜反应的试管; ②用分液漏斗分离硝基苯和水的混合物;
③用湿润的pH试纸测定稀盐酸的pH;
④用碱式滴定管量取20.00mL0.1mol/LKMnO4溶液
⑤不慎将苯酚溶液沾到皮肤上,立即用NaOH稀溶液清洗;
⑥配制FeSO4溶液时,需加入少量铁粉和稀硫酸
A.2 B.3 C.5 D.6
难度: 简单查看答案及解析
-
向一定量的Fe、FeO、Fe2O3、Fe3O4的混合物中加入150mL4 mol·L-1的稀硝酸恰好使混合物完全溶解,放出2.24LNO(标准状况),往所得溶液中加入KSCN溶液,无红色出现。若用足量的H2在加热条件下还原相同质量的混合物,所得到的铁的物质的量为
A.0.21mol B.0.25mol C.0.3mol D.0.35mol
难度: 简单查看答案及解析
-
设NA表示阿伏加德罗常数,下列叙述正确的是
A.71 g氯气被还原得到的电子数为2NA
B.100 mL l mol·L-1的碳酸钠溶液中含有的CO32-数为0.1NA
C.标准状况下,2.24 L乙烯中含有的σ键数目为0.5 NA
D.用含有少量锌、铁、银等杂质的粗铜作阳极电解精炼,当阴极析出64 g金属时阳极失去的电子数小于2NA
难度: 简单查看答案及解析
-
下列离子方程式书写正确的是
A.NaHSO4溶液与Ba(OH)2溶液反应至中性:H++SO42-+Ba2++OH- = BaSO4↓+H2O
B.NaClO溶液与FeCl2溶液混合:Fe2+ + 2ClO- + 2H2O= Fe(OH)2↓ + 2HClO
C.NH4HSO3溶液与足量NaOH溶液反应:NH4+ + OH-= NH3↑ + H2O
D.将1mol/L NaAlO2溶液和1.5mol/L的HCl溶液等体积互相均匀混合:
6AlO2-+9H++3H2O=5Al(OH)3↓+Al3+
难度: 简单查看答案及解析
-
在溶液中有浓度均为0.01mol·L-1的Fe3+、Cr3+、Zn2+、Mf2+等离子,已知:
Ksp[Fe(OH)3]=2.6×10-39;Ksp[Cr(OH)3]=7.0×10-31
Ksp[Zn(OH)2]=1.0×10-17;Ksp[Mg(OH)2]=1.8×10-11
当氢氧化物开始沉淀时,下列哪一种离子所需溶液的pH最小
A.Fe3+ B.Cr3+ C.Zn2+ D.Mg2+
难度: 简单查看答案及解析
-
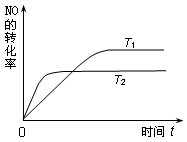
下图Ⅰ、Ⅱ分别是甲、乙两组同学将反应“AsO43-+2I-+2H+
AsO33-+I2+H2O”设计成的原电池装置,其中C1、C2均为碳棒。甲组向图Ⅰ烧杯中逐滴加入适量浓盐酸;乙组向图ⅡB烧杯中逐滴加入适量40%NaOH溶液。
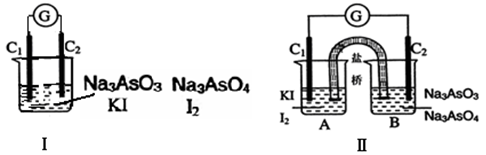
下列叙述中正确的是
A.甲组操作时,微安表(G)指针发生偏转
B.甲组操作时,溶液颜色变深
C.乙组操作时,C2做正极
D.乙组操作时,C1上发生的电极反应为I2 +2e-=2I-
难度: 简单查看答案及解析
-
“甲型H1N1”流感疫情已构成“具有国际影响的公共卫生紧急事态”。已知扎那米韦是流感病毒神经氨酸酶抑制剂,其对流感病毒的抑制是以慢结合的方式进行的,具有高度特异性,其分子结构如图所示。
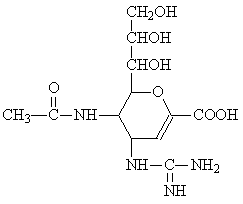
下列说法正确的是
A.该物质的分子式为C12H20N4O7
B.1mol该物质与NaOH溶液反应,可以消耗4molNaOH
C.在一定条件下,该物质可以发生消去、加成、取代等反应
D.该物质能使溴水或高锰酸钾溶液褪色,能与FeCl3溶液发生显色反应
难度: 简单查看答案及解析
-
下列叙述正确的是
A.c(NH4+)相等的(NH4)2SO4、(NH4)2Fe(SO4)2和NH4Cl溶液中,溶质浓度大小关系是:c[(NH4)2Fe(SO4)2] < c[(NH4)2SO4] < c(NH4Cl)
B.无色透明的酸性溶液中,Cu2+、K+、SO42-、NO3- 能大量共存
C.0.2mol·L-1 HCl溶液与等体积0.05 mol·L-1 Ba(OH)2溶液混合后,溶液的pH=1
D.NaHCO3溶液中:c(H+) + c(H2CO3)=c(CO32-) + c(OH-)
难度: 简单查看答案及解析