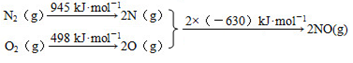-
近年我国汽车拥有量呈较快增长趋势,汽车尾气已成为重要的空气污染物.
(1)汽车内燃机工作时引起反应:N2(g)+O2(g)⇌2NO(g),是导致汽车尾气中含有NO的原因之一.
①该反应的平衡常数的表达式为K=______.
②T℃时,向容积为2L的密闭容器中充入10mol N2与5mol O2,2min后达到平衡,此时NO的物质的量为2mol,则O2的化学反应速率为______.
(2)一定量的NO发生分解的过程中,NO的转化率随时间变化的曲线如图所示.(已知:T1<T2)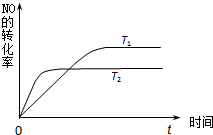
①由此推知,反应 N2(g)+O2(g)⇌2NO(g)为(填“吸热”或“放热”)______反应.
②一定温度下,能够说明反应 N2(g)+O2(g)⇌2NO(g) 已达到平衡的是(填序号)______.
a.容器内的压强不发生变化 b.NO生成的速率和NO分解的速率相等
c.NO、N2、O2的浓度保持不变 d.单位时间内生成4mol NO,同时消耗2mol N2
(3)①当发动机采用稀薄燃烧时,尾气中的主要污染物为NOx,可用CxHy(烃)催化还原NOx消除氮氧化物的污染.
已知:CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g)△H1=-574kJ•mol-1
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g)△H2
CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g)△H3=-867kJ•mol-1
则△H2=______.
②使用催化剂可以将汽车尾气的主要有害成分一氧化碳(CO)和氮氧化物(NOx)转化为无毒气体,该反应的化学方程式为______.
-
近年我国汽车拥有量呈较快增长趋势,汽车尾气已成为重要的空气污染物.
(1)汽车内燃机工作时引起反应:N2(g)+O2(g)⇌2NO(g),是导致汽车尾气中含有NO的原因之一.
①该反应的平衡常数的表达式为K=______.
②T℃时,向容积为2L的密闭容器中充入10mol N2与5mol O2,2min后达到平衡,此时NO的物质的量为2mol,则O2的化学反应速率为______.
(2)一定量的NO发生分解的过程中,NO的转化率随时间变化的曲线如图所示.(已知:T1<T2)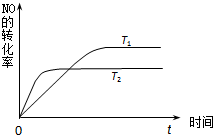
①由此推知,反应 N2(g)+O2(g)⇌2NO(g)为(填“吸热”或“放热”)______反应.
②一定温度下,能够说明反应 N2(g)+O2(g)⇌2NO(g) 已达到平衡的是(填序号)______.
a.容器内的压强不发生变化 b.NO生成的速率和NO分解的速率相等
c.NO、N2、O2的浓度保持不变 d.单位时间内生成4mol NO,同时消耗2mol N2
(3)①当发动机采用稀薄燃烧时,尾气中的主要污染物为NOx,可用CxHy(烃)催化还原NOx消除氮氧化物的污染.
已知:CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g)△H1=-574kJ•mol-1
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g)△H2
CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g)△H3=-867kJ•mol-1
则△H2=______.
②使用催化剂可以将汽车尾气的主要有害成分一氧化碳(CO)和氮氧化物(NOx)转化为无毒气体,该反应的化学方程式为______.
-
近年我国汽车拥有量呈较快增长趋势,汽车尾气已成为重要的空气污染物.
(1)汽车内燃机工作时引起反应:N2(g)+O2(g)⇌2NO(g),是导致汽车尾气中含有NO的原因之一.
①该反应的平衡常数的表达式为K=______.
②T℃时,向容积为2L的密闭容器中充入10mol N2与5mol O2,2min后达到平衡,此时NO的物质的量为2mol,则O2的化学反应速率为______.
(2)一定量的NO发生分解的过程中,NO的转化率随时间变化的曲线如图所示.(已知:T1<T2)
①由此推知,反应 N2(g)+O2(g)⇌2NO(g)为(填“吸热”或“放热”)______反应.
②一定温度下,能够说明反应 N2(g)+O2(g)⇌2NO(g) 已达到平衡的是(填序号)______.
a.容器内的压强不发生变化 b.NO生成的速率和NO分解的速率相等
c.NO、N2、O2的浓度保持不变 d.单位时间内生成4mol NO,同时消耗2mol N2
(3)①当发动机采用稀薄燃烧时,尾气中的主要污染物为NOx,可用CxHy(烃)催化还原NOx消除氮氧化物的污染.
已知:CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g)△H1=-574kJ•mol-1
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g)△H2
CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g)△H3=-867kJ•mol-1
则△H2=______.
②使用催化剂可以将汽车尾气的主要有害成分一氧化碳(CO)和氮氧化物(NOx)转化为无毒气体,该反应的化学方程式为______.
-
(12分)近年我国汽车拥有量呈较快增长趋势,汽车尾气已成为重要的空气污染物。
⑴汽车内燃机工作时引起反应:N2(g)+O2(g) 2NO(g),是导致汽车尾气中含有NO的原因之一。T ℃时,向容积为2 L的密闭容器中充入10 mol N2与5 mol O2,达到平衡后NO的物质的量为2 mol,则T ℃时该反应的平衡常数
2NO(g),是导致汽车尾气中含有NO的原因之一。T ℃时,向容积为2 L的密闭容器中充入10 mol N2与5 mol O2,达到平衡后NO的物质的量为2 mol,则T ℃时该反应的平衡常数
K=▲ 。(计算结果保留小数点后两位数字)
⑵一定量的NO发生分解的过程中,NO的转化率随时间变化的曲线如下图所示。(已知:T1<T2)
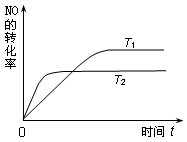
①反应 2NO(g)  N2(g)+O2(g)为(填“吸热”或“放热”)▲ 反应。
N2(g)+O2(g)为(填“吸热”或“放热”)▲ 反应。
②一定温度下,能够说明反应 2NO(g)  N2(g)+O2(g) 已达到平衡的是(填序号)▲ 。
N2(g)+O2(g) 已达到平衡的是(填序号)▲ 。
a.容器内的压强不发生变化 b.NO分解的速率和NO生成的速率相等
c.NO、N2、O2的浓度保持不变 d.单位时间内分解4 mol NO,同时生成2 mol N2
⑶①当发动机采用稀薄燃烧时,尾气中的主要污染物为NOx,可用CxHy(烃)催化还原NOx消除氮氧化物的污染。
已知:CH4(g)+4NO2(g) = 4NO(g)+CO2(g)+2H2O(g) △H1=-574 kJ·mol-1
CH4(g)+4NO(g) = 2N2(g)+CO2(g)+2H2O(g) △H2
CH4(g)+2NO2(g) = N2(g)+CO2(g)+2H2O(g) △H3=-867 kJ·mol-1
△H2=▲ 。
②使用催化剂可以将汽车尾气的主要有害成分一氧化碳(CO)和氮氧化物(NOx)转化为无毒气体,该反应的化学方程式为▲ 。
-
近年我国汽车拥有量呈较快增长趋势,汽车尾气已成为重要的空气污染物。
 ⑴汽车内燃机工作时引起反应:N2(g)+O2(g)
⑴汽车内燃机工作时引起反应:N2(g)+O2(g) 2NO(g),是导致汽车尾气中含有NO的原因之一。T ℃时,向容积为2 L的密闭容器中充入10 mol N2与5 mol O2,达到平衡后NO的物质的量为2 mol,则T ℃时该反应的平衡常数
2NO(g),是导致汽车尾气中含有NO的原因之一。T ℃时,向容积为2 L的密闭容器中充入10 mol N2与5 mol O2,达到平衡后NO的物质的量为2 mol,则T ℃时该反应的平衡常数
K=________▲ 。(计算结果保留小数点后两位数字)
⑵一定量的NO发生分解的过程中,NO的转化率随时间变化的曲线如右图所示。
(已知:T1<T2)

①反应 2NO(g)  N2(g)+O2(g)为(填“吸热”或“放热”)________▲反应。
N2(g)+O2(g)为(填“吸热”或“放热”)________▲反应。
②一定温度下,能够说明反应 2NO(g)  N2(g)+O2(g) 已达到平衡的是(填序号)▲ 。
N2(g)+O2(g) 已达到平衡的是(填序号)▲ 。
a.容器内的压强不发生变化 b.NO分解的速率和NO生成的速率相等
c.NO、N2、O2的浓度保持不变 d.单位时间内分解4 mol NO,同时生成2 mol N2
⑶①当发动机采用稀薄燃烧时,尾气中的主要污染物为NOx,可用CxHy(烃)催化还原NOx消除氮氧化物的污染。
已知:CH4(g)+4NO2(g) = 4NO(g)+CO2(g)+2H2O(g) △H1=-574 kJ·mol-1
CH4(g)+4NO(g) = 2N2(g)+CO2(g)+2H2O(g) △H2
CH4(g)+2NO2(g) = N2(g)+CO2(g)+2H2O(g) △H3=-867 kJ·mol-1
△H2=▲ 。
②使用催化剂可以将汽车尾气的主要有害成分一氧化碳(CO)和氮氧化物(NOx)转化为无毒气体,该反应的化学方程式为▲ 。
-
(12分)近年来北京市汽车拥有量呈较快增长趋势,汽车尾气已成为重要的空气污染物。
(1)汽车内燃机工作时引起反应:N2(g)+O2(g) 2NO(g),是导致汽车尾气中含有NO的原因之一。T℃时,向容积为2 L的密闭容器中充入10molN2与5molO2,达到平衡后NO的物质的量为2mol,则T℃时该反应的平衡常数K=________。(计算结果保留小数点后两位数字)
2NO(g),是导致汽车尾气中含有NO的原因之一。T℃时,向容积为2 L的密闭容器中充入10molN2与5molO2,达到平衡后NO的物质的量为2mol,则T℃时该反应的平衡常数K=________。(计算结果保留小数点后两位数字)
(2)一定量的NO发生分解的过程中,NO的转化率随时间变化的曲线如图14所示。(已知: )
)
①反应2NO(g) N2(g)+O2(g)为(填“吸热”或“放热)________反应。
N2(g)+O2(g)为(填“吸热”或“放热)________反应。

②一定温度下,能够说明反应2NO(g) N2(g)+O2(g)已达到平衡的是(填序号)________。
N2(g)+O2(g)已达到平衡的是(填序号)________。
a.容器内的压强不发生变化
b.NO、N2、O2的浓度保持不变
c.NO分解的速率和NO生成的速率相等
d.单位时间内分解4mol NO,同时生成2 mol N2
(3)①当发动机采用稀薄燃烧时,尾气中的主要污染物为NOx,可用CxHy(烃)催化还原NOx消除氮氧化物的污染。
已知:CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) △H1=-574kJ·mol-1
CH4(g)+4NO(g)=2N2(g)=CO2(g)+2H2O(g) △H2
CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g) △H3=-867kJ·mol-1
△H2=________.
②使用催化剂可以将汽车尾气的主要有害成分一氧化碳(CO)和氮氧化物(NO2)转化为无毒气体,该反应的化学方程式为________。
-
近年我国汽车拥有量呈较快增长趋势,汽车尾气已成为重要的空气污染物。回答下列问题:
(l)汽车发动机工作时会引起反应:N2(g)+O2(g) 2NO(g),是导致汽车尾气中含有NO的原因之一。2000K时,向容积为2L的密闭容器中充入2molN2与2molO2,发生上述反应,经过5min达到平衡,此时容器内NO的体积分数为0.75% .则该反应在5min内的平均反应速率v(O2)=_______mol/(Lmin),N2的平衡转化率为_______,2000K时该反应的平衡常数K=_____。
2NO(g),是导致汽车尾气中含有NO的原因之一。2000K时,向容积为2L的密闭容器中充入2molN2与2molO2,发生上述反应,经过5min达到平衡,此时容器内NO的体积分数为0.75% .则该反应在5min内的平均反应速率v(O2)=_______mol/(Lmin),N2的平衡转化率为_______,2000K时该反应的平衡常数K=_____。
(2)一定量NO发生分解的过程中,NO的转化率随时间变化的关系如右图所示。
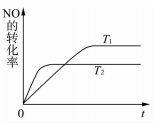
① 反应2NO(g) N2(g)+O2(g)为______反应(填“吸热”或“放热”) ;
N2(g)+O2(g)为______反应(填“吸热”或“放热”) ;
②一定温度下,能够说明反应2NO(g) N2(g)+O2(g)已达到平衡的是_____(填序号);
N2(g)+O2(g)已达到平衡的是_____(填序号);
a.容器内的压强不发生变化
b.混合气体的密度不发生变化
c. 2NO、N2、O2的浓度保持不变
d.单位时间内分解4molNO,同时生成2molN2
③ 在四个容积和温度均完全相同的密闭容器中分别加入下列物质,相应物质的量(mol)如下表所示。相同条件下达到平衡后,N2的体积分数最大的是_______(填容器代号);
| 容器代号 | NO | N2 | O2 |
| A | 2 | 0 | 0 |
| B | 0 | l | l |
| C | 0.4 | 0.6 | 0.8 |
| D | l | 0.5 | 0.4 |
(3)当发动机采用稀薄燃烧时,尾气中的主要污染物为NOx。可用CH4催化还原NOx以消除氮氧化物污染。
已知:CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) △H=-574kJ·mol-1
CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g) △H=-867kJ·mol-1
①写出CH4与NO反应生成N2、CO2、H2O(g)的热化学方程式:___________;
②使用催化剂可以将汽车尾气的主要有害成分一氧化碳(CO)和氮氧化物(NOx)转化为无毒气体,该反应的化学方程式为___________________。
-
近年我国汽车拥有量呈较快增长趋势,汽车尾气已成为重要的空气污染物。回答下列问题:
(l)汽车发动机工作时会引起反应:N2(g)+O2(g) 2NO(g),是导致汽车尾气中含有NO的原因之一。2000K时,向容积为2L的密闭容器中充入2molN2与2molO2,发生上述反应,经过5min达到平衡,此时容器内NO的体积分数为0.75% .则该反应在5min内的平均反应速率v(O2)=_______mol/(Lmin),N2的平衡转化率为_______,2000K时该反应的平衡常数K=_____。
2NO(g),是导致汽车尾气中含有NO的原因之一。2000K时,向容积为2L的密闭容器中充入2molN2与2molO2,发生上述反应,经过5min达到平衡,此时容器内NO的体积分数为0.75% .则该反应在5min内的平均反应速率v(O2)=_______mol/(Lmin),N2的平衡转化率为_______,2000K时该反应的平衡常数K=_____。
(2)一定量NO发生分解的过程中,NO的转化率随时间变化的关系如右图所示。
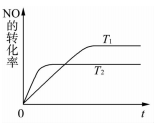
① 反应2NO(g) N2(g)+O2(g)为______反应(填“吸热”或“放热”) ;
N2(g)+O2(g)为______反应(填“吸热”或“放热”) ;
②一定温度下,能够说明反应2NO(g) N2(g)+O2(g)已达到平衡的是_____(填序号);
N2(g)+O2(g)已达到平衡的是_____(填序号);
a.容器内的压强不发生变化
b.混合气体的密度不发生变化
c. 2NO、N2、O2的浓度保持不变
d.单位时间内分解4molNO,同时生成2molN2
③ 在四个容积和温度均完全相同的密闭容器中分别加入下列物质,相应物质的量(mol)如下表所示。相同条件下达到平衡后,N2的体积分数最大的是_______(填容器代号);
| 容器代号 | NO | N2 | O2 |
| A | 2 | 0 | 0 |
| B | 0 | l | l |
| C | 0.4 | 0.6 | 0.8 |
| D | l | 0.5 | 0.4 |
(3)当发动机采用稀薄燃烧时,尾气中的主要污染物为NOx。可用CH4催化还原NOx以消除氮氧化物污染。
已知:CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) △H=-574kJ·mol-1
CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g) △H=-867kJ·mol-1
①写出CH4与NO反应生成N2、CO2、H2O(g)的热化学方程式:___________;
②使用催化剂可以将汽车尾气的主要有害成分一氧化碳(CO)和氮氧化物(NOx)转化为无毒气体,该反应的化学方程式为___________________。
-
近年我国汽车拥有量呈较快增长趋势,汽车尾气已成为重要的空气污染物。回答下列问题:
(l)汽车发动机工作时会引起反应:N2(g)+O2(g) 2NO(g),是导致汽车尾气中含有NO的原因之一。2000K时,向容积为2L的密闭容器中充入2molN2与2molO2,发生上述反应,经过5min达到平衡,此时容器内NO的体积分数为0.75% .则该反应在5min内的平均反应速率v(O2)=_______mol/(Lmin),N2的平衡转化率为_______,2000K时该反应的平衡常数K=_____。
2NO(g),是导致汽车尾气中含有NO的原因之一。2000K时,向容积为2L的密闭容器中充入2molN2与2molO2,发生上述反应,经过5min达到平衡,此时容器内NO的体积分数为0.75% .则该反应在5min内的平均反应速率v(O2)=_______mol/(Lmin),N2的平衡转化率为_______,2000K时该反应的平衡常数K=_____。
(2)一定量NO发生分解的过程中,NO的转化率随时间变化的关系如右图所示。
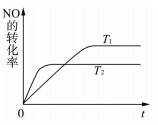
① 反应2NO(g) N2(g)+O2(g)为______反应(填“吸热”或“放热”) ;
N2(g)+O2(g)为______反应(填“吸热”或“放热”) ;
②一定温度下,能够说明反应2NO(g) N2(g)+O2(g)已达到平衡的是_____(填序号);
N2(g)+O2(g)已达到平衡的是_____(填序号);
a.容器内的压强不发生变化
b.混合气体的密度不发生变化
c. 2NO、N2、O2的浓度保持不变
d.单位时间内分解4molNO,同时生成2molN2
③ 在四个容积和温度均完全相同的密闭容器中分别加入下列物质,相应物质的量(mol)如下表所示。相同条件下达到平衡后,N2的体积分数最大的是_______(填容器代号);
| 容器代号 | NO | N2 | O2 |
| A | 2 | 0 | 0 |
| B | 0 | l | l |
| C | 0.4 | 0.6 | 0.8 |
| D | l | 0.5 | 0.4 |
(3)当发动机采用稀薄燃烧时,尾气中的主要污染物为NOx。可用CH4催化还原NOx以消除氮氧化物污染。
已知:CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) △H=-574kJ·mol-1
CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g) △H=-867kJ·mol-1
①写出CH4与NO反应生成N2、CO2、H2O(g)的热化学方程式:___________;
②使用催化剂可以将汽车尾气的主要有害成分一氧化碳(CO)和氮氧化物(NOx)转化为无毒气体,该反应的化学方程式为___________________。
-
(12分) 近年来我国汽车拥有量呈较快增长趋势,NOx是汽车尾气中的主要污染物之一。
(1)汽车发动机工作时会引发N2和O2反应,其能量变化示意图如下:
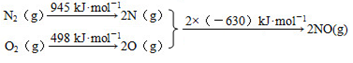
①写出该反应的热化学方程式 ,该反应的△S 0(填“>”、“<”或“=”);
②根据下图所示,只改变条件R,当N2的转化率从a3到a1时,平衡常数K 。

A.可能增大
B.一定不变
C.可能不变
D.可能减小
E.增大、减小、不变均有可能
(2)氮气是合成氨的原料之一,合成氨反应:N2(g)+3H2 (g) 2NH3(g) △H<0,500℃时将1molN2与1molH2充入容积为1L的密闭容器中发生反应,达到平衡后NH3的体积分数为20%。若升高温度至800℃,达到新的平衡时,H2的转化率 (填“增大”、“减小”或不变,下同),N2的体积分数 。
2NH3(g) △H<0,500℃时将1molN2与1molH2充入容积为1L的密闭容器中发生反应,达到平衡后NH3的体积分数为20%。若升高温度至800℃,达到新的平衡时,H2的转化率 (填“增大”、“减小”或不变,下同),N2的体积分数 。
(3)在汽车上安装高效催化转化器,将有毒气体转化为无毒气体,可有效降低NOx的排放。某研究性学习小组用气体传感器测得不同时间NO和CO的浓度如下表:
| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| c(NO)(×10-4 mol·L-1) | 10.0 | 4.50 | 2.50 | 1.50 | 1.00 | 1.00 |
| c(CO)(×10-3 mol·L-1) | 3.60 | 3.05 | 2.85 | 2.75 | 2.70 | 2.70 |
请回答下列问题:
①写出反应的化学方程式 。
②前2 s内的平均反应速率ν(N2) = 。
2NO(g),是导致汽车尾气中含有NO的原因之一。T ℃时,向容积为2 L的密闭容器中充入10 mol N2与5 mol O2,达到平衡后NO的物质的量为2 mol,则T ℃时该反应的平衡常数

N2(g)+O2(g)为(填“吸热”或“放热”)▲ 反应。
N2(g)+O2(g) 已达到平衡的是(填序号)▲ 。