-
化学与生产生活关系密切,下列说法不正确的是
A. 发射火箭采用的液氧、液氢都是纯净物,燃烧产物无污染
B. 减少燃煤发电,增加太阳能及水力发电,有利于治理雾霾
C. 垃圾中的金属、塑料及纸制品可以循环利用,因此生活垃圾要分类回收并处理
D. 用甲醛溶液浸泡食用海产品达到保鲜的目的
难度: 简单查看答案及解析
-
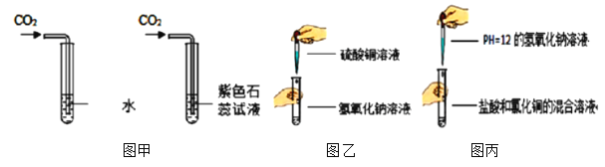
化学是一门以实验为基础的科学,下列实验过程中的现象或原理正确的是
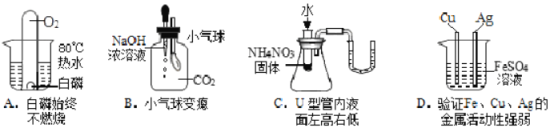
A. A B. B C. C D. D
难度: 中等查看答案及解析
-
归纳整理是学习化学的有效方法,下列有关内容错误的是
选项
现象或做法
解释
A
O2充足有助于化石燃料充分燃烧,CO2可用于档案资料或仪器仪表灭火
两种物质的分子构成不同,化学性质不同,物质的用途不同
B
实验室用向上排空气法收集CO2,用向下排空气法收集H2
气体的密度不同,使用的收集方法不同
C
在通电分解水实验中,用带火星的木条检验正极产生的气体,用燃烧的木条检验负极产生的气体
两极产生的气体不同,它们的化学性质不同,检验方法不同
D
用洗手液洗去手上的油污,用酒精擦去衣物上的油渍
油污种类不同,去污方法不同,化学反应原理不同
A. A B. B C. C D. D
难度: 中等查看答案及解析
-
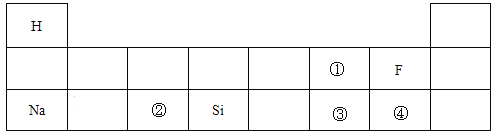
正确理解和使用化学用语是重要的科学素养,对于下列几种化学符号的说法正确的是
①H ②Fe2+ ③
④P2O5 ⑤KClO3
A. 表示阳离子的有②③
B. ④中数字“5”表示一个五氧化二磷分子中有5个氧元素
C. 表示物质组成的化学式的有①④⑤
D. ⑤中氯元素的化合价为5
难度: 简单查看答案及解析
-
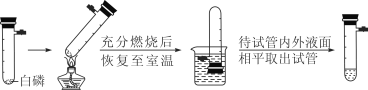
化学反应遵循质量守恒定律。四种物质在一定的条件下充分混合反应,测得反应前后各物质的质量分数如下图所示,则有关说法中不正确的是

A. 丁可能是氧化物
B. 乙可能是这个反应的催化剂
C. 生成的甲、丙两物质的质量比为8:1
D. 参加反应的丁的质量一定等于生成甲和丙的质量之和
难度: 中等查看答案及解析
-
溶液在工农业以及医疗上有着广泛应用。下表和下图是不同温度时硫酸镁的溶解度,有关说法正确的是
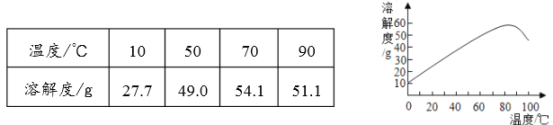
A. 硫酸镁的溶解度随温度升髙而增大
B. 硫酸镁属于易溶物质
C. 10℃时,27.7g硫酸镁和72.3g水可配制成质量分数为27.7%的硫酸镁溶液
D. 将70℃时的硫酸镁饱和溶液升温至90℃,溶液的溶质质量分数保持不变
难度: 简单查看答案及解析
-
下列实验所对应的两种方案均正确的是
选项
目的
方案一
方案二
A
除去二氧化碳中的少量水蒸气
通过浓硫酸
通过碱石灰
B
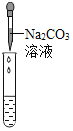
检验NaOH是否变质
加足量稀盐酸,观察
加适量氯化钡溶液,观察
C
将CuSO4转化成FeSO4
加过量的铁,反应后过滤
加氢氧化铁,反应后过滤
D
鉴别化肥NH4C1和NH4NO3
取样,加水溶解,观察
取样,加熟石灰研磨
A. A B. B C. C D. D
难度: 中等查看答案及解析