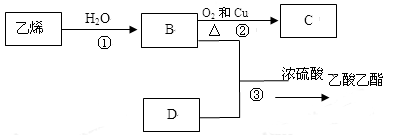
-
下列化学式只表示一种纯净物的是
A.C2H6 B.C4H10 C.C2H4Cl2 D.C
难度: 中等查看答案及解析
-
下列四种X溶液,均能跟盐酸反应,其中反应最快的是
A.10℃ 20mL 3mol/L的X溶液 B.20℃ 30mL 2molL的X溶液
C.20℃ 10mL 4mol/L的X溶液 D.10℃ 10mL 2mol/L的X溶液
难度: 中等查看答案及解析
-
CH2=C(CH3)-COOH,它不可能具有的性质是
A.使酸性高锰酸钾溶液褪色 B.发生加聚反应
C.与银氨溶液反应 D.与纯碱反应
难度: 中等查看答案及解析
-
下列说法中正确的一组是
A.H2和D2互为同位素;
B.
和
互为同分异构体;
C.正丁烷和异丁烷是同系物;
D.
和
是同一种物质
难度: 中等查看答案及解析
-
下列属于加成反应的是
A.己烯使酸性高锰酸钾溶液褪色
B.将苯滴入溴水中,振荡后水层接近无色。
C.乙烯使溴水褪色
D.甲烷与氯气混合光照一段时间后黄绿色消失。
难度: 中等查看答案及解析
-
下列属于纯净物的是
A.汽油 B.煤 C.乙烯 D.石油裂解气
难度: 简单查看答案及解析
-
下列化学用语中,书写或说法正确的是
A.乙烯的结构简式:CH2CH2
B.乙醇含有的官能团是—OH,带一个单位负电荷
C.丙烷的球棍模型为
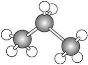
D.乙酸的分子式:C2H4O
难度: 中等查看答案及解析
-
下列混合物能用分液法分离的是
A.乙醇与乙酸 B.苯和硝基苯
C.乙酸乙酯和Na2CO3溶液 D.乙醛与水
难度: 中等查看答案及解析
-
甲烷中混有乙烯,欲除去乙烯得到纯净的甲烷,最好一次通过盛有以下哪种试剂的洗气瓶
A.澄清石灰水,浓硫酸 B.酸性高锰酸钾溶液,浓硫酸
C.溴水,烧碱溶液,浓硫酸 D.浓硫酸,酸性高锰酸钾溶液
难度: 中等查看答案及解析
-
能通过化学反应使溴水褪色,又能使高锰酸钾溶液褪色的是
A.苯 B.乙醇 C.乙烷 D.乙烯
难度: 中等查看答案及解析
-
下列有机物不能通过乙烯的加成反应制取的是
A.CH3CH2Cl B.CH2Cl—CH2Cl C.CH3—CH2OH D.CH3—COOH
难度: 中等查看答案及解析
-
两种气态烃组成的混合气体0.1 mol,完全燃烧得0.15 mol CO2和3.6 g H2O,下列关于该混合气体的说法正确的是
A.一定有乙烯 B.一定没有乙烯 C.一定有甲烷 D.一定有乙烷
难度: 中等查看答案及解析
-
下列有关除杂质(括号中为杂质)的操作中,错误的是
A.乙醇(水):加入足量生石灰充分振荡,蒸馏,收集馏出物
B.CCl4(乙醇):多次加水,振荡,分液,弃水层
C.苯(己烯):加溴水,振荡,过滤除去沉淀
D.乙酸乙酯(乙酸):加饱和碳酸钠溶液,充分振荡,分液,弃水层
难度: 中等查看答案及解析
-
如图是常见四种有机物的比例模型示意图。下列说法正确的是
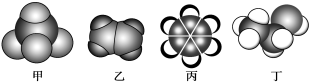
A.甲能使酸性高锰酸钾溶液褪色
B.乙可与溴水发生加成反应使溴水褪色
C.丙中的碳碳键是碳碳单键和碳碳双键交替的键
D.丁在稀硫酸作用下可与乙酸发生取代反应
难度: 中等查看答案及解析
-
如下图,下列装置能产生有效电流的是

难度: 中等查看答案及解析
-
下列关于原电池的叙述正确的是
A.原电池是化学能转变为电能的装置
B.构成原电池的正极和负极必须是两种不同的金属
C.原电池工作时,溶液中的阳离子向负极移动
D.原电池放电时,电子由负极经溶液到正极
难度: 中等查看答案及解析
-
下列事实不能用电化学理论解释的是
A.锅炉的内壁镶嵌有一定量的锌块 B.镀锌的铁制品比镀锡的铁制品耐用
C.用铝质铆钉接铁板,铁不易被腐蚀 D.铝片不用特殊方法保存
难度: 中等查看答案及解析
-
如图所示装置中,观察到电流计指针偏转;M棒变粗;N棒变细,由此判断表中所列M、N、P物质,其中可以成立的是
M
N
P
A
Zn
Cu
稀H2SO4溶液
B
Cu
Fe
稀HCl溶液
C
Ag
Zn
AgNO3溶液
D
Zn
Fe
Fe(NO3)3溶液
难度: 中等查看答案及解析
-
在同温同压下,下列各组热化学方程式中,ΔH1>ΔH2的是
A.2H2(g)+O2(g)=2H2O(l) ΔH1 2H2(g)+O2(g)=2H2O(g) ΔH2
B.S(g)+O2(g)=SO2(g) ΔH1 S(s)+O2(g)=SO2(g) ΔH2
C.C(s)+1/2O2(g)=CO(g) ΔH1 C(s)+O2(g)=CO2 (g) ΔH2
D.H2(g)+Cl2(g)=2HCl(g) ΔH1 1/2H2(g)+1/2Cl2(g)=HCl(g) ΔH2
难度: 中等查看答案及解析
-
(2004全国I卷)已知25℃、101kPa下,石墨、金刚石燃烧的热化学方程式分别为
C(石墨) + O2(g)=CO2(g) △H=-393.51kJ ·mol-1
C(金刚石) + O2(g)= CO2(g) △H=-395.41kJ ·mol-1
据此判断,下列说法中正确的是
A.由石墨制备金刚石是吸热反应;等质量时,石墨的能量比金刚石的低
B.由石墨制备金刚石是吸热反应;等质量时,石墨的能量比金刚石的高
C.由石墨制备金刚石是放热反应;等质量时,石墨的能量比金刚石的低
D.由石墨制备金刚石是放热反应;等质量时,石墨的能量比金刚石的高
难度: 中等查看答案及解析
-
下列反应中反应物的总能量比生成物低的是
A.镁与二氧化碳反应
B.铁和稀硫酸的反应
C.氢氧化钡晶体的粉末和氯化铵晶体混合
D.木炭在氧气中燃烧
难度: 中等查看答案及解析
-
据报导我国最近合成多种元素的新同位素,其中一种是
(铪),它的中子数是
A.72 B.113 C.185 D.257
难度: 简单查看答案及解析
-
下列各组中属于同位素关系的是
A.
与
B.T2O与H2O C.
与
D.金刚石与石墨
难度: 简单查看答案及解析
-
下列各组元素性质递变情况错误的是
A.Li、Be、B原子最外层电子数逐渐增多
B.N、O、F原子半径依次增大
C.P、S、Cl最高正价依次升高
D.Li、Na、K、Rb的金属性依次增强
难度: 简单查看答案及解析
-
下列叙述中错误的是
A.原子半径:Cl>S>O B.还原性:Na>Mg>Al
C.稳定性:HF>HCl>HBr D.酸性:HClO4>H2SO4>H3PO4
难度: 中等查看答案及解析
-
电子层数相同的三种元素X、Y、Z,已知其最高价氧化物对应水化物的酸性强弱为HXO4> H2YO4> H3ZO4。下列判断错误的是
A.原子半径:X>Y>Z B.气态氢化物的稳定性:HX>H2Y>ZH3
C.非金属性:X>Y>Z D.单质氧化性:X>Y>Z
难度: 中等查看答案及解析
-
下列关于元素周期律的叙述正确的是
A.随着元素原子序数的递增,原子最外层电子总是从1到8重复出现
B.随着元素原子序数的递增,原子半径从大到小(稀有气体除外)发生周期性变化
C.随着元素原子序数的递增,元素最高正价从+1到+7、负价从-7到-1重复出现
D.元素性质的周期性变化是指原子核外电子排布的周期性变化、原子半径的周期性变化及元素主要化合价的周期性变化
难度: 中等查看答案及解析
-
国际无机化学命名委员会在1989年做出决定,把长式元素周期表原先的主副族及族号取消,由左至右改为18列。如碱金属为第1列,稀有气体元素为第18列。按此规定,下列说法中错误的是
A.第9列元素中没有非金属元素
B.第17列为卤族元素
C.只有第2列元素原子的最外层有2个电子
D.在整个18列元素中,第3列元素种类最多
难度: 中等查看答案及解析
-
下列事实,不能说明氯元素的非金属性比硫元素强的是
A.盐酸是强酸,氢硫酸是弱酸 B.HClO4酸性比H2SO4强
C.氯气与H2S能发生置换反应 D.受热时,氯化氢比硫化氢稳定
难度: 中等查看答案及解析
-
下列物质中含有自由移动氯离子的是
A.氯酸钾 B.液态氯化氢 C.熔融的氯化钾 D.液氯
难度: 简单查看答案及解析
-
下列变化中,不需要破坏化学键的是
A.氯化氢溶于水 B.加热氯酸钾使其分解
C.碘升华 D.氯化钠溶于水
难度: 中等查看答案及解析
-
某元素原子最外层只有1个电子,它跟卤素相结合时,所形成的化学键是
A.一定是共价键 B.一定是离子键
C.可能是共价键,也可能是离子键 D.以上说法均不正确
难度: 中等查看答案及解析
-
下列各分子中,化学键类型不同的是
A.H2O、CO B.MgF2、H2O C.KOH、Mg(OH)2 D.HCl、HBr
难度: 中等查看答案及解析
-
在N2+3H2
2NH3反应中,自反应开始至2s末,氨的浓度由0变为0.4mol/L,则以氢气的浓度变化表示该反应在2s内的平均反应速率是
A.0.3mol/(L·s) B.0.4 mol/(L·s)
C.0.6 mol/(L·s) D.0.8 mol/(L·s)
难度: 中等查看答案及解析
-
在密闭容器中进行X2(g)+Y2(g)
2Z(g)的反应,已知起始时其中X2、Y2、Z各物质浓度分别为0.1mol∙L-1、0.3mol∙L-1、0.2mol∙L-1,反应达到平衡时,各物质浓度可能是
A.c(X)=0.2mol∙L-1 B.c(Y2)=0.35mol∙L-1
C.c(Y2)=0.2mol∙L-1 D.c(Z)=0.4mol∙L-1
难度: 中等查看答案及解析
-
在2A(g) +B(g)
3C(g) +4D(g)反应中,表示该反应速率最快的是
A.v(A)=0.5mol·L-1· s-1 B.v(B)=0.3 mol·L-1· s-1
C.v(C)=0.6 mol·L-1· s-1 D.v(D)=1 mol·L-1· s-1
难度: 中等查看答案及解析
-
可逆反应2NO+O2
2NO2二氧化氮红棕色在密闭容器中反应,达到平衡状态的标志是
A.NO2、NO和O2 三者共存
B.单位时间内生成n molO2的同时生成2n mol NO
C.容器中颜色不再变化
D.容器中NO2、NO、O2的物质的量浓度之比为2:2:1的状态
难度: 中等查看答案及解析
-
反应C(s)+H2O(g)
CO(g)+ H2(g)在一容积可变的密闭容器中进行。下列条件的改变对其反应速率几乎无影响的是
A.压缩容器体积,增大体系压强
B.加入适当的催化剂
C.保持压强不变,充入惰性气体使容器容积增大
D.保持容器容积不变,充入惰性气体使体系压强增大
难度: 中等查看答案及解析
-
(3分)写出下列物质的结构式
(1)(CN)2
(2)HClO
(3)S3Cl2
难度: 中等查看答案及解析