-
(4分)热化学方程式:
(1)在标准状况下的11.2L甲烷完全燃烧生成CO2 和液态水放出444.8KJ热量(298K),其热化学方程式为 。
(2)已知断裂下列1mol化学键需要吸收的能量分别为:C=O:745KJ/mol , O=O:496kJ/mol , C-H:414KJ/mol 则断裂1molH-O键需要提供的能量为 kJ
高一化学填空题中等难度题查看答案及解析
-
H2、CO、CH4、CH3OH等都是重要的能源,也是重要为化工原料。
(1)已知25℃,1.01×105Pa时,,8.0Dg CH4完全燃烧生成二氧化碳气体和液态水放出444. 8kJ热量。写山该反应的热化学反应方程式:____________________。
(2)为倡导“节能减排”和“低碳经济”, 降低大气中CO2的含量及有效地开发利用CO2,工业上可以用CO2来生产燃料甲醇。
在体积为2L的密闭容器中,充入lmol CO2和3mol H2,一定条件下发生反应:CO2(g) +3H2(g)
CH3OH(g) + H2O(g)。经测得CO2和CH3OH(g)的物质的量随时间变化如图所示。
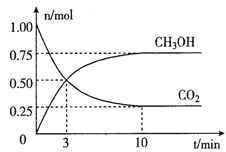
①从反或开始到平衡,CO2的平均反应速率v(CO2)=____。
②达到平衡时,H2的转化率为__________。
③下列措施不能提高反应速率的是__________。
A.升高温度 B.加入催化剂 C.增大压强 D.及时分离出CH3OH
(3)工业上也用CO和H2为原料制备CH3OH,反应方程式为:CO(g) +2H2(g)
CH3OH( g),在一体积固定的密闭容器中投入一定量的CO和H2气体进行上述反应。下列叙述中能说明上述反应达到平衡状态的是______。
A.反应中CO与CH3OH的物质的量之比为1:1
B.混合气体的压强不随时间的变化而变化
C.单位时间内每消耗1molCO,同时生成1mclCH3OH
D. CH3OH的质量分数在混合气体中保持不变
E.混合气体的密度保持不变
高一化学综合题中等难度题查看答案及解析
-
CH4(其中C为-4价)既是一种重要的能源,也是一种重要的化工原料。
(1)已知8.0gCH4完全燃烧生成二氧化碳和液态水时放出444.8kJ热量。若一定量的甲烷完全燃烧生成二氧化碳和液态水时放出1334.4kJ的热量,则需要标准状况下的氧气约___L。
(2)以CH4为燃料可设计成结构简单、能量转化率高、对环境无污染的燃料电池,其工作原理如图甲所示,通入2.24L(已换算为标准状况)a气体时,通过质子交换膜转移的H+数目为___(设NA为阿伏加德罗常数的值)。
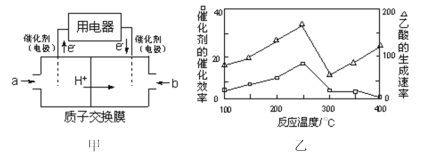
(3)在一定温度和催化剂作用下,CH4与CO2可直接转化成乙酸,这是实现“减排”的一种研究方向。
①在不同温度下,催化剂的催化效率与乙酸的生成速率如图乙所示,则该反应的最佳温度应控制在___℃左右。
②该反应催化剂的有效成分为偏铝酸亚铜(CuAlO2,难溶物)。将CuAlO2溶解在稀硝酸中生成两种盐并放出NO气体,其反应的离子方程式为___。
③CH4还原法是处理NOx气体的一种方法。已知一定条件下CH4与NOx反应转化为N2、CO2和H2O,若标准状况下8.96LCH4可处理22.4LNOx,则x值为___。
高一化学综合题中等难度题查看答案及解析
-
(6分)由Zn—Cu—H2SO4组成的原电池,工作一段时间后,锌片的质量减少了6.5g。求:
(1)原电池生成氢气_______L(标准状况)。
(2)已知:1mol氢气完全燃烧放出285.8kJ的热量。将(1)中获得的氢气燃烧,可以得到_________kJ的热量。
(3)若起始时刻两电极质量相等,将电解质溶液改为硫酸铜溶液,当电池输出相同的电量时,电池两极的质量差为__________g。
高一化学计算题中等难度题查看答案及解析
-
甲烷与甲醇(CH3OH,液态)都属于清洁能源,已知每摩尔甲烷完全燃烧生成液态水和 CO2时放出的热量约为 890.3kJ,每摩尔甲醇完全燃烧生成液态水和 CO2 时放出的热量约为 726.0kJ。
(1)相同质量的甲烷与甲醇完全燃烧,生成液态水和 CO2 时放出热量较多的是_____。从共用电子对的偏离情况来看,甲烷分子中的共价键属于_____,甲醇分子的结构可以看成是甲烷分子中的一个H 原子被原子团(—OH)取代而得到,请根据甲烷的电子式写出甲醇分子的电子式_____。
(2)甲醇燃烧的热化学方程式为_____,1mol 甲醇完全燃烧,若生成水蒸气和 CO2 则放出的热量_____726.0kJ(填>、<或=)。
高一化学填空题中等难度题查看答案及解析
-
(1)8g CH4气体完全燃烧生成CO2气体和液态水放出445 kJ热量。
①写出表示甲烷燃烧热的热化学方程式____________________________________。
②若1molCH4气体完全燃烧生成CO2气体和水蒸气,放出热量_____890 kJ( 填“>”、 “<”、“= ”)。
(2)已知在298K时:①C(石墨,s)+1/2O2(g)=CO(g) ΔH1=-111kJ·mol-1
②H2(g)+1/2O2(g)=H2O(g) ΔH2=-242kJ·mol-1
③C(石墨,s)+O2(g)=CO2(g) ΔH3=-394kJ·mol-1
利用盖斯定律,写出298K时一氧化碳与水蒸气转化为氢气和二氧化碳的热化学方程式:_________。
高一化学计算题中等难度题查看答案及解析
-
CH4既是一种重要的能源,也是一种重要的化工原料。
(1)已知8.0 g CH4完全燃烧生成液态水放出444.8 kJ热量。则CH4 (g)+2O2(g)=CO2(g)+2H2O(l) ΔH=____________kJ·mol-1。
(2)在一定温度和催化剂作用下,CH4与CO2可直接转化成乙酸,这是实现“减排”的一种研究方向。
①在不同温度下,催化剂的催化效率与乙酸的生成速率如图所示,则该反应的最佳温度应控制在 ___________左右。
②该反应催化剂的有效成分为偏铝酸亚铜 (CuAlO2,难溶物)。将CuAlO2溶解在稀硝酸中生成两种盐并放出NO气体,其离子方程式为 _____________________。
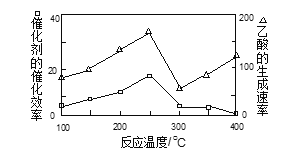
(3)CH4还原法是处理NOx气体的一种方法。已知一定条件下CH4与NOx反应转化为N2和CO2,若标准状况下8.96 L CH4可处理22.4 L NOx,则x值为_______________。
高一化学综合题中等难度题查看答案及解析
-
已知充分燃烧a g乙炔(C2H2)气体时生成22.4L二氧化碳气体(已折算成标准状况下)和液态水,并放出热量b kJ,则乙炔燃烧的热化学方程式正确的是( )
A.2C2H2(g)+5O2(g) 4CO2(g)+2H2O(l);△H=-4b kJ/mol
B.C2H2(g)+
O2(g) 2CO2(g)+H2O(l);△H=2b kJ/mol
C.2C2H2(g)+5O2(g) 4CO2(g)+2H2O(l);△H=-2b kJ/mol
D.2C2H2(g)+5O2(g) 4CO2(g)+2H2O(l);△H=b kJ/mol
高一化学选择题简单题查看答案及解析
-
H2、CO、CH4、CH3OH等都是重要的能源,也是重要为化工原料。
(1)已知25℃,1.01×105Pa时,8.0g CH4完全燃烧生成二氧化碳气体和液态水放出444.8kJ热量。写出该反应的热化学反应方程式:___________________________________________。
(2)为倡导“节能减排”和“低碳经济”,降低大气中CO2的含量及有效地开发利用CO2,工业上可以用CO2来生产燃料甲醇。在体积为2L的密闭容器中,充入lmol CO2和3mol H2,一定条件下发生反应:CO2(g) + 3H2(g)
CH3OH(g) + H2O(g)。经测得CO2和CH3OH(g)的物质的量随时间变化如图所示。
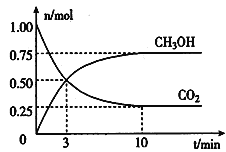
①从反应开始到平衡,CO2的平均反应速率v(CO2)=___________________。
②达到平衡时,H2的转化率为__________。
③该反应的平衡常数K=___________________(表达式)。
④下列措施不能提高反应速率的是__________。
A.升高温度 B.加入催化剂 C.增大压强 D.及时分离出CH3OH
(3)工业上也用CO和H2为原料制备CH3OH,反应方程式为:CO(g) + 2H2(g)
CH3OH(g),在一体积固定的密闭容器中投入一定量的CO和H2气体进行上述反应。下列叙述中能说明上述反应达到平衡状态的是______。
A.反应中CO与CH3OH的物质的量之比为1:1
B.混合气体的压强不随时间的变化而变化
C.单位时间内每消耗1 mol CO,同时生成1 mol CH3OH
D.CH3OH的质量分数在混合气体中保持不变
E.混合气体的密度保持不变
高一化学综合题中等难度题查看答案及解析
-
4 g甲烷在氧气中燃烧生成CO2和液态水,放出222.5 KJ热量,写出甲烷燃烧的热化学方程式________
高一化学填空题简单题查看答案及解析