-
酯和油脂的水解又称为
A.中和反应 B.不可逆反应 C.取代反应 D.复分解反应
难度: 简单查看答案及解析
-
关于元素周期律和元素周期表的下列说法,正确的是()
A.目前发现的所有元素占据了周期表里全部位置,不可能再有新的元素被发现
B.元素的性质随着原子序数的增加而呈周期性变化
C.俄国化学家道尔顿为元素周期表的建立做出了巨大的贡献
D.同一主族的元素从上到下,金属性呈周期性变化
难度: 简单查看答案及解析
-
下列说法中正确的是( )
A.油脂的主要成分是高级脂肪酸甘油酯,属于酯类
B.酯基“
”不能发生加成反应,故油脂不能使溴水褪色
C.
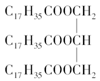 的名称为软脂酸甘油酯
的名称为软脂酸甘油酯D.酯在碱性条件下的水解叫皂化反应
难度: 简单查看答案及解析
-
仔细分析下列表格中烃的排列规律,判断排列在第15位烃的分子式是( )

A.C6H12 B.C6H14 C.C7H12 D.C7H14
难度: 简单查看答案及解析
-
下列关于乙烯的说法中,不正确的是()
A.是无色气体,比空气略轻,难溶于水
B.与溴水发生取代反应而使溴水褪色
C.乙烯的产量标志着一个国家的石油化工水平
D.可用点燃法鉴别乙烯和甲烷
难度: 简单查看答案及解析
-
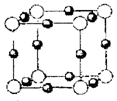
下图是某有机分子的比例模型,黑色的是碳原子,白色的是氢原子,灰色的是氧原子。该物质不具有的性质是()

A.与氢氧化钠溶液反应 B.与稀硫酸反应C.发生酯化反应D.使紫色石蕊试液变红
难度: 简单查看答案及解析
-
X、Y-、Z+三种微粒的电子层结构相同,则一定不能再相等的是( )。
A.中子数 B.质量数 C.电子数 D.核电荷数
难度: 简单查看答案及解析
-
化学家们合成了一种新物质——五星烷,其键线式如图所示(已知:CH2CHCH2CHO的键线式为:
)。下列有关五星烷的说法正确的是 ( )
A.五星烷与乙烷互为同系物
B.五星烷的化学式为C15H20
C.五星烷分子中含有7个五元环D.五星烷的一氯代物有三种
难度: 简单查看答案及解析
-
A、B、C 三种醇同足量的金属钠反应,在相同条件下产生相同体积的氢气,消耗这三种醇的物质的量之比为3:6:2,则 A、B、C 三种醇分子中羟基数之比是
A. 3:2:1 B. 2:6:3 C. 3:6:2 D. 2:1:3
难度: 简单查看答案及解析
-
下列关于羟基和氢氧根的说法中,不正确的是( )。
A.羟基比氢氧根少一个电子
B.两者的组成元素相同
C.羟基不带电,氢氧根带一个单位负电荷
D.羟基比氢氧根性质稳定
难度: 简单查看答案及解析
-
已知A、B、C、D、E是核电荷数依次增大的五种短周期元素,原子半径按D、E、B、C、A的顺序依次减小,B和E同主族。下列推断不正确的是( )
A.A、B、E一定在不同周期
B.C的最高价氧化物的水化物可能显碱性
C.A、D可能在同一主族
D.C和D的单质可能化合形成离子化合物
难度: 简单查看答案及解析
-
现有①溴水②烧碱溶液③纯碱溶液④小苏打溶液⑤2-丁醇⑥酸性高锰酸钾溶液,其中能和乙酸反应的是
A.①②③④⑤ B. ②③④⑤ C. ②③④ D. ①②③④⑤⑥
难度: 简单查看答案及解析
-
对H2O的电离平衡不产生影响的粒子是
A. H: Cl: B. 26M3+ C.
D.
难度: 简单查看答案及解析
-
设NA表示阿伏加德罗常数的值,下列传述不正确的是( )
A.标准状况下,11.2L三氯甲烷所分子数为0.5NA
B.常温常压下,1mol甲基(-CH3)所含电子数为9NA
C.常温常压下,22g氧气和26g臭氧混合后,混合气体所含氧原子总数为3NA
D.标准状况下,将22.4L的NO2通入足量水中发生反应,转移的电子总数为
NA
难度: 简单查看答案及解析
-
钠与下列物质反应都能够产生氢气:①H2O;②CH3COOH;③CH3CH2OH。试推断这三种物质电离出H+的难易程度(从难到易的顺序)( )
A.①②③ B.②③① C.③①② D.②①③
难度: 简单查看答案及解析
-
有四种有机物
④葡萄糖,其中既能发生酯化反应又能发生加成反应的是 ( )
A.①② B.③④ C.①③④ D.①②③
难度: 简单查看答案及解析
-
在一定的温度、压强下,向100 mL CH4和Ar的混合气体中通入400 mL O2,点燃使其完全反应,最后在相同条件下得到干燥气体460 mL,则反应前混合气体中CH4和Ar的物质的量之比为( )
A.1∶4 B.1∶3 C.1∶2 D.1∶1
难度: 简单查看答案及解析
-
下列物质中一定不含有羟基的是:
A.HNO3 B.H2O C.NaOH D.CH3CH2OH
难度: 简单查看答案及解析
-
下列物质中不能发生银镜反应的是
A、 葡萄糖 B、蔗糖 C、淀粉水解产物 D、纤维素水解产物
难度: 简单查看答案及解析
-
短周期元素X、Y、Z的原子序数依次递增,其原子的最外层电子数之和为13。X与Y、Z位于相邻周期,Z原子最外层电子数是X原子内层电子数的3倍或者是Y原子最外层电子数的3倍。下列说法正确的是( )
A.X的氢化物溶于水显酸性 B.X与Y形成化合物的化学式为X2Y2
C.Y的氧化物是离子化合物 D.X和Z的最高价氧化物对应水化物都是弱酸
难度: 简单查看答案及解析
-
PASS是新一代高效絮凝净水剂,它由X、Y、Z、W、R五种短周期元素组成,五种元素原子序数依次增大。X原子是所有原子中半径最小的,Y、R同主族,Z、W、R同周期,Y原子的最外层电子数是次外层的3倍,Z是常见的金属,其氢氧化物能溶于强碱溶液但不溶于氨水,W单质是人类将太阳能转变为电能的常用材料。下列说法正确的是( )
A.它们的原子半径依次增大 B.WY2能与碱反应,但不能与任何酸反应
C.Z与Y形成的化合物是一种耐高温材料 D.热稳定性:X2R >X2Y
难度: 简单查看答案及解析
-
如下图所示为氢氧燃料电池的原理示意图,按照此图的提示,下列叙述不正确的是( )

A.a电极是负极
B.b电极的电极反应为:4OH--4e-====2H2O+O2↑
C.氢氧燃料电池是一种具有应用前景的绿色电源
D.氢氧燃料电池是一种不需要将还原剂和氧化剂全部储藏在电池内的新型发电装置
难度: 简单查看答案及解析