-
地壳中含量居第二位的非金属元素是
A.铁 B.铝 C.氧 D.硅
难度: 简单查看答案及解析
-
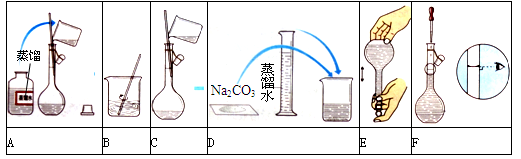
下图中能实现人工固氮的是

难度: 简单查看答案及解析
-
下列关于钠的叙述中,不正确的是
A.钠燃烧时发出黄色的火焰 B.钠燃烧时生成氧化钠
C.钠有很强的还原性 D.钠原子的最外层只有一个电子
难度: 简单查看答案及解析
-
下列物质不属于合金的是
A.青铜 B.铝 C.钢 D.生铁
难度: 简单查看答案及解析
-
现在CO和CO2 两种气体,它们所含氧原子的物质的量均为1 mol ,则 CO 与CO2的分子数之比为
A.1 :1 B.1 :2 C.2 :1 D.3 :2
难度: 中等查看答案及解析
-
下列各组混合物可用如图装置分离的是
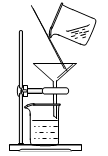
A.汽油和植物油
B.碳酸钙和水
C.酒精和水
D.四氯化碳和碘
难度: 简单查看答案及解析
-
“X”光透视常用钡餐作造影剂。钡餐的主要成分为硫酸钡,其化学式是BaSO4 ,BaSO4属于
A.单质 B.混合物 C.化合物 D.氧化物
难度: 简单查看答案及解析
-
“纳米材料”是指直径从几纳米至几十纳米的材料,目前已广泛应用于催化剂及军事技术中,如果将纳米材料分散到液体分散剂中,所得混合物
A.不能透过滤纸 B.一定是浊液
C.一定是溶液 D.有丁达尔效应
难度: 简单查看答案及解析
-
下列各组离子在溶液中为无色,且能大量共存的是
A.Cu2+、SO42-、Na+、Cl- B.Na+、CO32-、H+、K+
C.Mg2+、H+、SO42-、NO3- D.Ag+、NO3-、K+、Cl-
难度: 中等查看答案及解析
-
除去Na2CO3 固体中少量NaHCO3的最佳方法是
A.加入适量盐酸 B.加入NaOH溶液
C.加热 D.配成溶液后通入CO2
难度: 简单查看答案及解析
-
实验室需用500mL 0.1mol• L-1NaOH溶液,下列有关配制该溶液的说法中不正确的是
A.应选用500mL的容量瓶
B.应称取2.0 g NaOH固体
C.将称量的NaOH固体置于烧杯中用适量水溶解
D.将溶解的NaOH溶液直接注入容量瓶中,再加入蒸馏水至刻度线
难度: 中等查看答案及解析
-
下列关于浓硝酸和浓硫酸的叙述中正确的是
A.常温下均可用铝制容器运输
B.露置在空气中,容器内酸液质量都减小
C.常温下均能与铜较快反应
D.露置在空气中,容器内酸液质量都增大
难度: 简单查看答案及解析
-
下列叙述正确的是
A.SO42-的摩尔质量为96g• mol-1
B.1mol物质的质量等于该物质的式量
C.1molO2的质量为32 g• mol-1
D.CO2的摩尔质量为44g
难度: 简单查看答案及解析
-
下列化学方程式中,能用离子方程式:Ba2+ + SO42- = BaSO4↓表示的是
A.Ba(OH)2 + (NH4)2SO4 == BaSO4↓ + 2NH3•H2O
B.Ba(OH)2 + H2SO4 == BaSO4↓ + 2H2O
C.BaCO3 + H2SO4 == BaSO4↓ + 2H2O + CO2↑
D.BaCl2 + Na2SO4 == BaSO4↓ + 2NaCl
难度: 中等查看答案及解析
-
根据反应式:①2Fe3++2I-
2Fe2++I2 和② Br2+2Fe2+
2Fe3++ 2Br-,可判断离子的还原性从强到弱的顺序是
A.Br-、Fe2+、I- B.I-、Fe2+、Br-
C.Br-、I-、Fe2+ D.Fe2+、I-、Br-
难度: 简单查看答案及解析
-
下列各组物质相互反应能得到Al(OH)3的是
A.铝与NaOH溶液反应 B.AlCl3与过量的氨水反应
C.AlCl3与过量的NaOH溶液反应 D.Al2O3与过量的NaOH溶液反应
难度: 简单查看答案及解析