-
将含O2和CH4的混合气体充入装有23.4gNa2O2的密闭容器中点燃,反应结束后,容器温度为150℃,压强为0pa,将残留物溶于水无气体逸出。下列叙述正确的是( )
A.原混合气体中O2和CH4的体积比为2:1
B.原混合气体中O2和CH4的体积比为1:3
C.残留固体中有Na2CO3和NaOH
D.残留固体中只有Na2CO3
难度: 中等查看答案及解析
-
多硫化钠Na2Sx(x>2)在结构上与Na2O2、FeS2、CaC2等有相似之处。Na2Sx在碱性溶液中可被NaClO氧化为Na2SO4,而NaClO被还原为NaCl,反应中Na2Sx与NaClO的物质的量之比为1︰16,则x的值是 ( )
A、5 B、4 C、3 D、2
难度: 中等查看答案及解析
-
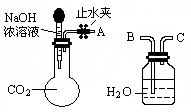
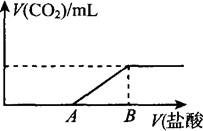
甲试管中盛有0.5mol/L Na2CO3溶液10mL,慢慢往试管中加入1mol/L的盐酸7.0mL;乙试管中盛有1mol/L的盐酸7.0mL,慢慢往试管中滴加0.5mol/L Na2CO3溶液10mL,那么甲、乙两试管中产生的CO2物质的量大小关系为 ( )
A、甲=乙 B、甲>乙 C、甲<乙 D、无法确定
难度: 中等查看答案及解析
-
NaH是一种离子化合物,与水反应时生成烧碱和氢气,它也能和乙醇等反应产生氢气。下列关于NaH的叙述中正确的是 ( )
A.与水反应时,水作氧化剂
B.LiH中阳离子半径小于阴离子半径
C.跟乙醇反应时,放出氢气的速度比跟水反应时更快
D.与水反应时,生成的烧碱是还原产物
难度: 中等查看答案及解析
-
在烧杯中加一些水,滴入几滴酚酞溶液,然后把一小块钠放入水中,从这个实验过程观察到的反应现象中,不可能得出的结论是 ( )
A.钠比较柔软 B.钠与水反应生成碱
C.钠与水反应放热 D.钠与水反应放出气体
难度: 中等查看答案及解析
-
将4.6g钠放入95.4g水中, 所得溶液的质量分数是 ( )
A 等于4.6% B等于8% C 4.6% ~8% D 大于 8%
难度: 中等查看答案及解析
-
如下图带漏斗U型管中装有足量的煤油和水的混合物,静置后投入一小块碱金属。可观察到金属在煤油和水的界面a附近上下往复运动,下列说法不正确的是 ( )
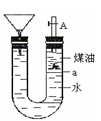
A.此碱金属可能是钾或钠
B.反应一段时间煤油会燃烧
C.碱金属上下运动是由于与水反应产生了氢气
D.若是金属锂则不能观察到上述现象
难度: 中等查看答案及解析
-
“神州七号”三兄弟——LiH、LiD、LiT。其中Li的质量数为7,对这三种物质的下列说法正确的是 ( )
A.质子数之比为1:2:3 B.中子数之比为1:1:1
C.摩尔质量之比为8:9:10 D.化学性质不相同
难度: 中等查看答案及解析
-
把钠放入滴有酚酞试液的水中,下列现象不会出现的是 ( )
A.钠浮在水面上 B.钠熔化成小球
C.溶液中产生较多的气泡 D.水溶液变成红色
难度: 中等查看答案及解析
-
下面关于Na2CO3和NaHCO3性质的叙述,不正确的是 ( )
A.在水中的溶解度:碳酸钠>碳酸氢钠
B.热稳定性:碳酸钠>碳酸氢钠
C.等质量的碳酸钠和碳酸氢钠分别与足量的盐酸反应,前者产生二氧化碳少
D.足量的碳酸钠和碳酸氢钠分别与等物质的量的盐酸反应,两者产生二氧化碳一样多
难度: 中等查看答案及解析
-
将一定量的金属钠放入一定物质的量浓度的NaOH溶液中,反应完成后,NaOH溶液的物质的量浓度 ( )
A.增大 B.不能确定 C. 减少 D.不变
难度: 中等查看答案及解析
-
把金属钠2.3g溶于水中,要使所得溶液中,钠离子与水分子个数之比为1:100,则所需要水的质量是 ( )
A.181.8g B.180g C.181.6g D.220g
难度: 中等查看答案及解析
-
如图所示,在密闭容器中,一边装有一定量的金属钠,一边装有一定量的氧化汞,同时加热容器的两部分,钠和氧化汞都完全反应后,恢复到原温度,容器内空气的成分仍不变。则钠和氧化汞的物质的量之比是 ( )
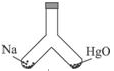
A.1:1 B.2∶1 C.23∶216.6 D.216.6∶23
难度: 中等查看答案及解析
-
将足量的CO2不断通入KOH、Ba(OH)2、KAlO2的混合溶液中,生成沉淀与通入CO2的体积的关系可表示为

难度: 中等查看答案及解析
-
下列叙述中,正确的是 ( )
A.Na比K的金属性强 B.Na和K的电子层数相同
C.Na和K都是强还原剂 D.Na和K灼烧时都能使火焰呈现紫色
难度: 中等查看答案及解析
-
由短周期元素组成的中学常见无机物A、B、C、D、E、X存在如右图转化关系(部分生成物和反应条件略去)。下列推断不正确的是 ( )
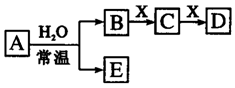
A.若X是Na2CO3,C为含极性键的非极性分子,则A一定是氯气,且D和E不反应
B.若A是单质,B和D的反应是
则E一定能还原Fe2O3C.若D为CO,C能和E反应,则A一定为Na2O2,其电子式是
D.若D为白色沉淀,与A摩尔质量相等,则X一定是铝盐
难度: 中等查看答案及解析