-
化学无处不在,下列与化学有关的说法不正确的是( )
A. 侯氏制碱法的工艺过程中应用了物质溶解度的差异
B. 用NaOH溶液雕刻工艺玻璃上的纹饰
C. Na2O可用于呼吸面具中作为氧气的来源
D. 黑火药由硫黄、硝石、木炭三种物质按一定比例混合制成
难度: 困难查看答案及解析
-
分类是化学学习和研究的常用手段,下列分类依据和结论都正确的是
A. 冰醋酸、纯碱、芒硝、生石灰分别属于酸、碱、盐、氧化物
B. HC1O、H2SO4(浓)、HNO3均具有强氧化性,都是氧化性酸
C. 漂白粉、福尔马林、冰水、王水、氯水均为混合物
D. Na2O、NaOH、Na2CO3、NaCl、Na2SO4、Na2O2都属于钠的含氧化合物
难度: 中等查看答案及解析
-
下列各物质中所含原子个数由大到小的顺序正确的是( )
①0.5mol氨气;②标准状况下22.4L氦气;③4℃时9mL水;④0.2mol磷酸
A. ①④③② B. ④③②① C. ②③④① D. ①④②③
难度: 中等查看答案及解析
-
下列叙述不正确的是( )
A. 相同条件下,N2和O2的混合气体与等体积的N2所含原子数相等
B. 等物质的量的甲基(-CH3)与羟基(-OH)所含电子数相等
C. 常温常压下28 g CO与22.4 L O2所含分子数相等
D. 16 g CH4与18 g NH4+所含电子数相等
难度: 简单查看答案及解析
-
在酸性溶液中(加热并有Ag+催化)可发生如下反应:2Mn2+ + 5R2O8X— + 8H2O == 16H+ +10RO42— + 2MnO4—根据上述反应,则R2O8X—中x的值是( )
A. 4 B. 3 C. 2 D. 1
难度: 中等查看答案及解析
-
四种短周期主族元素W、X、Y、Z的原子序数依次增大,W、X的简单离子具有相同电子层结构,X的原子半径是短周期主族元素原子中最大的,W与 Y同族,Z 与X 形成的离子化合物的水溶液呈中性。下列说法正确的是
A. 简单离子半径:W<X<Z
B. W与X形成的化合物溶于水后溶液呈碱性
C. 气态氢化物的热稳定性:W<Y
D. 最高价氧化物的水化物的酸性:Y>Z
难度: 中等查看答案及解析
-
某种Na2SO4和Fe2(SO4)3的混合溶液中,Fe3+的物质的量浓度为0.4mol/L,SO42-的物质的量浓度为0.7mol/L,则该混合溶液中Na+的物质的量浓度为
A. 0.1mol/L B. 0.15mol/L C. 0.2mol/L D. 0.25mol/L
难度: 中等查看答案及解析
-
CO2与H2的混合气体5g,在150℃时和足量的氧气混合,用电火花充分引燃,在相同状况下再将反应后所得混合气体通入到足量的Na2O2中,测得Na2O2固体增重的质量为3.4g,则原混合气体中CO2的质量分数为( )
A. 25% B. 75% C. 88% D. 32%
难度: 中等查看答案及解析
-
下列叙述中不正确的是
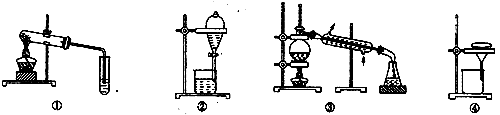
A. 可用装置①鉴别碳酸钠和碳酸氢钠 B. 可用装置②分离汽油和水的混合物
C. 可用装置③从海水中蒸馏得到淡水 D. 可用装置④把胶体粒子从分散系中分离出来
难度: 中等查看答案及解析
-
下列离子方程式正确的是
A. Na2S2O3溶液中加入稀硫酸:2S2O32-+2H+=SO42-+3S↓+H2O
B. 向NH4HSO3溶液中滴加足量KOH溶液:NH4++OH-=NH3•h2o
C. 在海带灰的滤液中加入几滴稀硫酸,再加入双氧水,能使淀粉溶液变蓝:2I-+H2O2+2H+=I2+2H2O
D. 盐碱地(含较多NaCl、Na2CO3)中加入石膏,降低土壤的碱性,涉及的方程式为:Ca2++CO32-=CaCO3↓
难度: 困难查看答案及解析
-
通过对实验现象的观察、分析、推理得出正确的结论是化学学习的方法之一。对下列实验事实的解释正确的是( )
操作、现象
解释
A
向KI淀粉溶液中加入FeCl3溶液,溶液变蓝
Fe3+能与淀粉发生显色反应
B
把生铁放置于潮湿的空气中,铁表面有一层红棕色的斑点
铁在潮湿的空气中易生成Fe(OH)3
C
向稀硝酸中加入少量铁粉,有气泡产生
说明Fe置换出溶液中的氢,生成了氢气
D
新制Fe(OH)2露置于空气中一段时间,白色物质变成了红褐色
说明Fe(OH)2易被O2氧化成Fe(OH)3
A. A B. B C. C D. D
难度: 中等查看答案及解析
-
25℃时,下列各组离子在指定溶液中一定能大量共存的是( )
A. pH=1的溶液中:Na+、K+、MnO4-、CO32-
B. c(H+)=1×10-13mol/L的溶液中:Mg2+、Cu2+、SO42-、NO3-
C. 0.1mol/LNH4HCO3溶液中:K+、Na+、NO3-、Cl-
D. 0.1mol/LFeCl3溶液中:Fe2+、NH4+、SCN-、SO42-
难度: 困难查看答案及解析
-
某无色溶液中,已知含有H+、Mg2+、Al3+等阳离子,逐滴加入NaOH(溶液),则消耗NaOH(溶液)体积(x轴)和生成沉淀量(y轴)之间的函数关系,可用下图表示,则下列图中正确的是( )
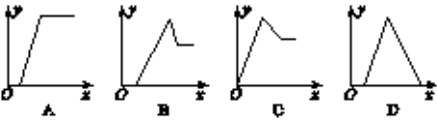
A. A B. B C. C D. D
难度: 中等查看答案及解析
-
下列推断合理的是( )
A. 明矾[KAl(SO4)2·12H2O]在水中能形成Al(OH)3胶体,可用作净水剂
B. 金刚石是自然界中硬度最大的物质,不可能与氧气发生反应
C. 浓H2SO4有强氧化性,常温下能与Cu发生剧烈反应
D. 将SO2通入品红溶液,溶液褪色后加热恢复原色;将SO2通入溴水,溴水褪色后加热也能恢复原色
难度: 简单查看答案及解析
-
将0.03 mol Cl2缓缓通入含有0.02 mol H2SO3和0.02 mol HBr的混合液中,则溶液中 H+的浓度与通入的氯气的物质的量的关系是下列图中的(纵坐标都表示氢离子的物质的量浓度( )

A. A B. B C. C D. D
难度: 中等查看答案及解析
-
向下列六种饱和溶液中分别持续通入CO2气体,最终得到沉淀或析出晶体的一组是( )
① Ba(NO3)2 ② Ca(OH)2 ③Na2SiO3④NaA1O2⑤ Na2CO3⑥ NH3和NaCl
A. ①③④⑥ B. ②③④⑥ C. ③④⑤⑥ D. ①②③⑤
难度: 中等查看答案及解析
-
向含有0.2molFeI2的溶液中加入amolBr2。下列叙述不正确的是( )
A. 当a=0.1时,发生的反应为2I-+ Br2=I2 +2Br-
B. 当 a=0.25时,发生的反应为 4Fe2++6I-+5Br2=4Fe3++3I2+10Br-
C. 当溶液中I-有一半被氧化时,c(I-)∶c(Br-)=l∶1
D. 当0.2<a<0.3时(不考虑碘与水反应),溶液中各离子浓度的关系为:2c(Fe2+) + 3c(Fe3+) +c(H+)=c(Br-)+ c(OH-)
难度: 困难查看答案及解析

