-
无机化学中也存在同分异构体,互为同分异构体的一组无机物是 ( )
A.NH4CNO与尿素CO(NH2)2
B.H2O与D2O
C.[Cr(H2O)5Cl]Cl2·H2O与[Cr(H2O)4Cl2]Cl·2H2O
D.Si(OH) 4与H4SiO4
难度: 简单查看答案及解析
-
下列化学式及结构式中,从成键情况看来不合理的是 ( )
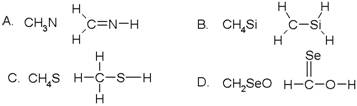
难度: 简单查看答案及解析
-
某共价化合物分子中含有C.N、O、H四种元素,且以nC.nN、nO分别表示C.N和O的原子数目,则H原子数目最多为 ( )
A.2nO+2 B.2nC+nN C.2(nC+nN) D.2nC+nN+2
难度: 简单查看答案及解析
-
下列叙述中正确的是 ( )
A.阳离子不一定是金属离子,含阳离子的物质一定含阴离子
B.阴、阳离子相互作用不一定形成离子化合物
C.离子化合物均属于强电解质,都易溶于水
D.由某金属元素的阳离子和某非金属元素阴离子组成的物质一定是纯净物
难度: 简单查看答案及解析
-
下列实验或生产操作:①蛋白质溶液中加入硫酸铵形成沉淀;②二氧化氮经加压凝成无色液体;③石蜡催化裂化;④碘受热变成碘蒸汽;⑤照相底片被感光。其中,没有新的物质生成的是 ( )
A.①④ B.②③ C.①③⑤ D.①②④
难度: 简单查看答案及解析
-
下列车员物质按照纯净物、混合物、电解质和非电解质顺序排列的是 ( )
A.盐酸、水煤气、醋酸、干冰
B.冰醋酸、福尔马林、硫酸钠、乙醇
C.单甘油酯、混甘油酯、苛性钾、石灰石
D.胆矾、漂白粉、氯化钾、氯气
难度: 简单查看答案及解析
-
航天技术测得三氧化二碳(C2O3)是金星大气层的成份之一,下列关于C2O3的说法中错误的是 ( )
A.C2O3与CO2都是碳的氧化物 B.C2O3与CO2都是碳酸的酸酐
C.C2O3与CO都具有还原性 D.C2O3与C的燃烧产物都是CO2
难度: 简单查看答案及解析
-
下列变化能够实现的是 ( )
①弱酸与盐溶液反应生成强酸
②两种氧化物发生反应有气体生成
③两种酸的溶液充分反应后溶液呈中性
④复分解反应中既没有生成水,也没有生成沉淀和气体
A.只有①③ B.只有②④ C.只有①②④ D.①②③④
难度: 简单查看答案及解析
-
下列离子方程式正确的是( )
A.等物质的量浓度的FeBr2和CuCl2混合溶液用惰性电极电解最初发生:
Cu 2+ + 2Br-
Cu +Br2
B.碳酸氢镁溶液中加入足量的烧碱溶液:
Mg2+ + 2HCO3- + 2OH- = MgCO3↓+ CO32- + 2H2O
C.Fe(NO3)3的酸性溶液中通入足量硫化氢:2Fe3++H2S===2Fe2++S↓+2H+
D.H218O中投入Na2O2:4H218O+O22-===2H2O+4OH-+18O2↑
难度: 简单查看答案及解析
-
最近,科学家用一种称为“超酸”的化合物H(CB11H6Cl6)和C60反应,使C60获得一个质子,得到一种新型离子化合物[HC60]+[CB11H6Cl6]-。该反应看起来很陌生,但反应类型上可以跟中学化学里某个熟悉的化学反应相比拟。该化学反应是 ( )
A.
B.
C.
D.
难度: 简单查看答案及解析
-
对于复分解反应:X+Y=Z+W,下列叙述正确的是 ( )
A.若Z是强酸,则X或Y必有一种是酸
B.若Y是强碱,X是盐,则Z或W必有一种是弱碱
C.若W是弱碱,Z是盐,则X或Y必有一种是强碱
D.若X是强酸,Y是盐,反应后可能有强酸或弱酸生成
难度: 简单查看答案及解析
-
“混盐”是指一种金属离子与多种酸根离子构成的盐,如氯化硝酸钙[Ca(NH3)Cl]就是一种混盐。“复盐”是指含有多种简单阳离子和一种酸根阴离子的盐如Kal(SO4)2,下列各化合物中属于混盐的是 ( )
A.CaOCl2 B.(NH4)3Fe(SO4)2 C.BiONO3 D.K3[Fe(CN)6]
难度: 简单查看答案及解析
-
被誉为“太空金属”的钛,在室温下,不与水、稀硫酸、稀盐酸和稀硝酸作用,但易溶于氢氟酸,其原因可能是 ( )
A.氢氟酸的酸性比其他酸强 B.氢氟酸的氧化性比其他酸强
C.氢氟酸的还原性比其他酸强 D.钛离子易与氟离子形成可溶性难电离物质
难度: 简单查看答案及解析
-
在催化剂作用下乙酸可通过两步反应得乙烷,反应原理如下:
①CH3COOH+2H2→CH3CH2OH+H2O
②CH3CH2OH+H2→CH3CH3+H2O
③CH3COOH+3H2→CH3CH3+2H2O
在反应过程中乙酸和乙醇会生成乙酸乙酯。为研究分别考查了加Mo(钼)和不加Mo负载型Ni(镍)催化剂催化效能,某文献记载的数据如下:
乙酸转化率
未反应的含氧化合物含量
乙酸
乙醇
温度/℃
Mo16Ni6
Ni6
Mo16Ni6
Ni6
Mo16Ni6
Ni6
240
87.2
21.8
0.53
3.24
1.03
0.14
260
89.1
27.2
0.45
3.02
0.99
0.19
下列说法不正确的是 ( )
A.上述①②③三反应均属于加成反应
B.上述①②③三反应均属于还原反应
C.乙酸加氢脱氧反应260℃比240℃下进行更有利
D.Mo16Ni6催化性能比Ni6好
难度: 简单查看答案及解析
-
a mol FeS与b mol FeO投入到V L、c mol·L-1的硝酸溶液中充分反应,产生NO气体,所得澄清溶液成分可看作是Fe(NO3)3、H2SO4的混合液,则反应中未被还原的硝酸可能为 ( )
①(a+b)×63 g ②(a+b)×189 g ③(a+b)mol ④(Vc-
)mol
A.①④ B.②③ C.①③ D.②④
难度: 简单查看答案及解析