-
常温下,柠檬水溶液的PH是3,其中的C(OH—)是 ( )
A.0.1mol/L B. 1.0×10-3 mol/L C. 1.0×10-11mol/L D. 1.0×10-7mol/L
难度: 简单查看答案及解析
-
常温下下列有关CH3COONa溶液中的关系式不正确的是 ( )
A.C((H +)>1.0×10-7mol/L
B.C(CH3COOˉ) +C(OHˉ)= C(Na +)+C(H +)
C.C(CH3COOˉ)+C(CH3COOH) =C(Na +)
D.C(OHˉ)= C(CH3COOH) +C(H +)
难度: 简单查看答案及解析
-
常温下,AgI的溶度积是8.3×10-17,在该温度下把0.01L浓度为8.0× 10-6mol/L的AgNO3溶液和0.01L浓度为4.0×10-7 mol/L的KCl溶液混合,下列说法正确的是(溶液体积变化忽略不计) ( )
A.不能确定有无AgI沉淀生成 B.没有AgI沉淀生成
C.有KNO3晶体析出 D. 有AgI沉淀生成
难度: 简单查看答案及解析
-
常温下测得NaA盐溶液的PH值是10,有关盐NaA的说法正确的是 ( )
A.强酸弱碱盐 B.强碱弱酸盐 C.强酸强碱盐 D. 弱酸弱碱盐
难度: 简单查看答案及解析
-
锌铜原电池产生电流时,阳离子 ( )
A.移向Zn极,阴离子移向CU极 B.移向CU极,阴离子移向Zn极
C.和阴离子都移向Zn极 D。和阴离子都移向CU极
难度: 简单查看答案及解析
-
下列各变化中属于原电池反应的是 ( )
A.在空气中金属铝表面迅速氧化形成保护层
B.镀锌铁皮表面有划损时,仍然能阻止铁被氧化
C.红热的铁丝与水接触,表面形成蓝黑色保护层
D.纯锌与稀硫酸反应时,有大量气泡产生
难度: 简单查看答案及解析
-
下列关于碱性锌锰电池的判断正确的是 ( )
A.Zn是正极, MnO2是负极
B.工作时电子由MnO2经外电路流向Zn
C.Zn是负极, MnO2是正极
D. Zn 电极发生还原反应,MnO2电极发生氧化反应
难度: 简单查看答案及解析
-
下列关于电解槽的叙述中不正确的是 ( )
A.与电源正极相连的是电解槽的阴极
B.与电源负极相连的是电解槽的阴极
C.在电解槽的阳极发生氧化反应
D. 电子从阳极沿导线流入电源的正极
难度: 简单查看答案及解析
-
在下列装置中(都盛有0.1mol/L H2SO4溶液)Zn片腐蚀最快的是 ( )
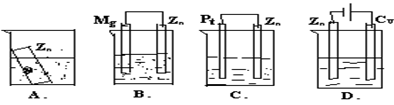
难度: 简单查看答案及解析
-
以下能级符号正确的是 ( )
A.1p B. 2d C. 3f D. 4s
难度: 简单查看答案及解析
-
下列各图中哪一个是氧原子的电子排布图 ( )
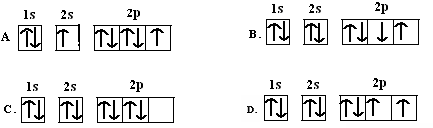
难度: 简单查看答案及解析
-
以下是基态原子的电子排布式的是 ( )
A.1s12s1 B.1s12s12p1 C.1s22s22p6 3p1 D.1s22s22p63 s2
难度: 简单查看答案及解析
-
以下关于金属的金属性的判断正确的是 ( )
A.镁和铝与同浓度的盐酸反应铝没镁反应剧烈,所以铝比镁的金属性强
B.Mg(OH)2溶液的碱性比NaOH溶液的碱性弱,所以镁比钠的金属性强
C.铁能从CuSO4溶液中置换出铜,所以铁比铜的金属性强
D.电解含Ag+和CU2+的溶液时,Ag+优先放电,所以银比铜的金属性强
难度: 简单查看答案及解析
-
在元素周期表中,原子最外电子层只有2个电子的元素 ( )
A.无法判断是哪一类元素 B.一定是稀气体元素
C.一定是过渡元素 D.一定是金属元素
难度: 简单查看答案及解析
-
将足量的AgCl分别加入下列物质中,AgCl的溶解度由大到小的排列顺序是( )
①20ml0.01mol∕LKCl溶液;②20ml0.02mol∕LCaCl2溶液;③20ml蒸馏水;
④20ml0.03mol∕LHCl溶液;⑤20ml0.05mol∕L AgNO3溶液;
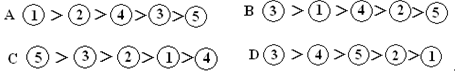
难度: 简单查看答案及解析
-
右图为直流电源电解稀Na2SO4水溶液的装置。通电后在石黑电极a和b附近分别滴加一滴石蕊溶液,下列实验现象中正确的是 ( )
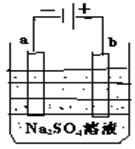
A.逸出气体的体积,a电极的小于b电极的
B.有一电极逸出有刺激性气味的气体
C.a电极附近呈红色,b电极附近呈蓝色
D.a电极附近呈蓝色,b电极附近呈红色
难度: 简单查看答案及解析