-
2015年6月5日世界“环境日”中国的主题是“践行绿色生活”。下列不符合这一主题的是
A.从自身做起,从身边小事做起,减少超前消费、炫耀性消费、奢侈性消费和铺张浪费现象
B.减少温室气体的排放,倡导“绿色低碳”的生活
C.少开私家车,提倡“绿色出行”
D.向空气中喷洒烧碱溶液,避免酸雨的发生
难度: 中等查看答案及解析
-
2015年4月,于敏获颁“影响世界华人终身成就奖”。“钚--239”是“于敏型”氢弹的重要原料。下列说法正确的是
A.239Pu原子的原子核中含有239个质子
B.238Pu、239Pu和241Pu属于不同的核素
C.238Pu与238U在元素周期表中的位置相同
D.239Pu衰变成235U属于化学变化
难度: 中等查看答案及解析
-
下列有关电解质的叙述中错误的是
A.强电解质在水溶液里或熔融状态时的电离方式是一样的
B.弱电解质溶液可能比强电解质溶液的导电性强
C.HCl是强电解质,它只能在水溶液里才能电离
D.电解质溶液导电过程中必然伴随化学变化
难度: 中等查看答案及解析
-
当我们查看葡萄酒标签上的成分信息时,常发现其成分中含有少量SO2。下列关于SO2说法正确的是
A.SO2属于非法添加剂,不该添加到葡萄酒中
B.SO2具有还原性,少量的SO2可防止葡萄酒氧化变质
C.SO2具有还原性,不能用浓硫酸干燥
D.SO2可以使酸性KMnO4溶液褪色,体现了它的漂白性
难度: 中等查看答案及解析
-
铝对生物有毒害作用,尤其对人体的毒害更加严重。下列说法不正确的是
A.不吃或少吃使用了含铝食品添加剂的食物
B.不能用铝制器皿长期存放酸性或碱性食品
C.杜绝铝制品在生产生活中的应用
D.铝不属于重金属,它使人体中毒的原理与铅不同
难度: 简单查看答案及解析
-
已知:CaCO3+2HCl=CaCl2+CO2↑+H2O ΔH<0。下列说法不正确的是
A.其它条件不变,适当增大盐酸的浓度将加快化学反应速率
B.其它条件下不变,适当增加CaCO3的用量将加快化学反应速率
C.反应过程中,化学反应速率将先增大后减小
D.一定条件下反应速率改变,ΔH<0不变
难度: 中等查看答案及解析
-
已知阿伏加德罗的值为NA。下列说法正确的是
A.28gN2与足量氢气反应,转移电子的数目为6NA
B.500mL 0.1mol·L-1的MgSO4溶液中,阴离子所带负电荷数为0.1NA
C.标准状况下,22.4L14CO2与44g14CO2所含分子数均为NA
D.2L0.2mol·L-1的稀硝酸与适量铁恰好反应(还原产物只有NO),生成NO的分子数为0.1 NA
难度: 中等查看答案及解析
-
下列离子方程式正确的是
A.向KAl(SO4)2溶液中滴加Ba(OH)2溶液至Al3+恰好沉淀完全:2Al3++3SO42-+3Ba2++6OH-=2Al(OH)3↓+3BaSO4↓
B.向NH4HSO4溶液中滴加过量NaOH溶液并加热:NH4++OH-
H2O+NH3↑
C.向AlCl3溶液中滴加过量氨水:Al3++4NH3∙H2O=[Al(OH)4]-+4NH4+
D.FeO溶于稀硝酸中:FeO+2H+=Fe2++H2O
难度: 中等查看答案及解析
-
下列关于元素周期表的说法正确的是
A.第2周期与第3周期元素从左到右,最高正化合价均从+1逐渐增大至+7,0族元素一般是0价
B.3个长周期所含元素种数相同
C.不同主族的3、4周期元素原子序数的差可能不同
D.同周期从左到右,非金属元素含氧酸的酸性逐渐增强
难度: 中等查看答案及解析
-
下列因果关系正确的是
A.因为H2O的沸点比H2S高,所以O原子得电子能力大于S原子
B.因为F原子得电子能力比Cl原子强,所以氢氟酸属于强酸
C.因为H2CO3酸性大于H2SiO3,所以CH4稳定性大于SiH4
D.因为Na+KCl(熔融)=NaCl+K↑,所以Na原子失电子能力大于K原子
难度: 中等查看答案及解析
-
二十二碳六烯酸,俗称脑黄金,是一种对人体非常重要的不饱和脂肪酸,其结构简式如图。下列相关说法不正确的是
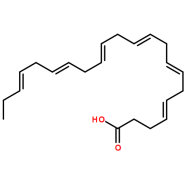
A.该物质的分子式为:C22H32O2
B.该物质能使酸性高锰酸钾溶液褪色
C.该物质一定条件下能发生取代反应
D.1mol该物质最多能与7molBr2发生加成反应
难度: 中等查看答案及解析
-
下列实验操作中,装置选择不合理的是
A
B
C
D
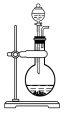
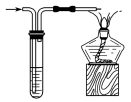
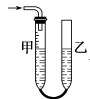
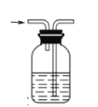
洗气瓶
快速制备少量NH3
H2的尾气处理
测量NO的体积
除去乙烯中的SO2
难度: 中等查看答案及解析
-
在体积为VL的密闭容器中存在化学平衡:2NO2(g)
N2O4(g)ΔH<0。保持温度不变,将容器体积压缩至V/2后,下列说法不正确的是
A.容器内气体颜色变深
B.容器内NO2分子数减少
C.混合气体的平均相对分子质量增大
D.NO2的物质的量分数增大
难度: 中等查看答案及解析
-
目前市面上有一种新型饭盒“即热饭盒”,其原理是在饭盒底部有两层,一层存放食盐水,另一层存放镁和铁的混合物,使用时打开隔离层,食物即可被快速加热。下列对其工作原理分析不正确的是
A.打开隔层后,形成了由食盐水、镁和铁构成的原电池
B.金属镁发生了氧化反应
C.铁是该原电池的负极
D.反应中涉及化学能、电能和热能的转化
难度: 中等查看答案及解析
-
下列对各电解质溶液的分析正确的是
A.向稀氨水中滴加稀盐酸至恰好中和:[NH4+]=[Cl-]
B.硫酸钠溶液中:[Na+]+[H+]=[OH-]+2[SO42-]
C.0.1mol∙L-1Na2S溶液中:[S2-]+[HS-]+[H2S]=[Na+]
D.向CH3COONa溶液中加适量蒸馏水:[CH3COO-]与[OH-]都减小,[OH-]/[CH3COO-]也减小
难度: 中等查看答案及解析
-
同分异构现象在有机化合物中普遍存在,C4H8Cl2的同分异构体中含有2个“-CH3”的种数是
A.2种 B.3种 C.4种 D.5种
难度: 中等查看答案及解析



