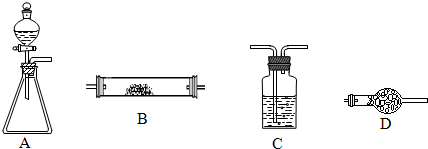
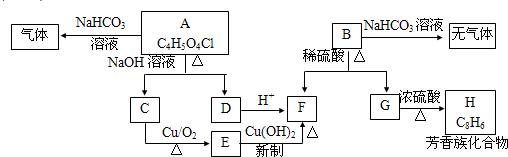
-
下列说法正确的是( )
A.明矾和漂白粉常用于水处理,两者的作用原理相同
B.18g冰比18g水中的氢键多
C.工业生产中常用焦炭等还原剂从氧化铝中获取铝
D.电解精炼铜时,当转移NA个电子时,阳极材料质量一定减轻32g难度: 中等查看答案及解析
-
常温下,甲溶液的pH是乙溶液pH的2倍,若将甲、乙两溶液等体积混合,则混合溶液的酸碱性情况为( )
A.一定呈酸性
B.一定呈碱性
C.一定呈中性
D.无法确定难度: 中等查看答案及解析
-
下列化学方程式(或离子方程式)书写正确的是( )
A.溴乙烷在一定条件下生成乙烯:CH3-CH2BrCH2=CH2↑+HBr
B.苯酚钠溶液中通入少量CO2气体:
C.大理石与醋酸反应:CaCO3+2H+=Ca2++CO2↑+H2O
D.氯化钙溶液中通入CO2气体:CaCl2+CO2+H2O=CaCO3↓+2HCl难度: 中等查看答案及解析
-
霉酚酸(Mycophenolic acid) 是一种生物活性化合物.下列有关霉酚酸的说法正确的是( )
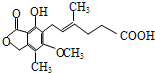
A.霉酚酸分子式为C17H21O6
B.1mol霉酚酸最多能与6molH2发生加成反应
C.霉酚酸既能发生加成反应、取代反应,又能发生氧化反应、还原反应
D.一定条件下,1mol霉酚酸最多可与4molNaOH反应难度: 中等查看答案及解析
-
在化学实验操作中,往往由于不规范导致较大的实验误差.下列有关实验中,会导致所测定结果偏大的是(其他操作均正确)( )
A.配制500mL1mol/L稀硫酸实验中,没有洗涤烧杯和玻璃棒
B.胆矾晶体结晶水含量测定实验中,坩埚没放在干燥器中冷却,冷却后用天平称量
C.用标准盐酸滴定待测NaOH溶液实验中,使用酸式滴定管开始平视,后来俯视读数
D.在中和热测定实验中,用稀氢氧化钠溶液与浓硫酸反应获得的中和热数值难度: 中等查看答案及解析
-
常温时,浓度均为0.01mol/L的四种溶液:①Na2CO3溶液,②NaHCO3溶液,③H2CO3溶液,④CH3COOH溶液.下列有关说法不正确的是( )
A.上述溶液中,将①和②等体积混合,其溶液中粒子浓度关系为2c(Na+)=3c(HCO-3)+3c(CO2-3)+3c(H2CO3)
B.上述四种溶液中,由水电离的c(OH-)的大小关系为:①>②>③>④
C.上述四种溶液中,分别加水稀释,所得溶液中c(H+)/c(OH-)的数值均增大
D.上述四种溶液中,分别加入少量的NaOH固体,此时溶液的pH均增大难度: 中等查看答案及解析
-
铅蓄电池是目前我国广泛使用的电源,关于铅蓄电池的说法正确的是( )
A.在放电时,正极发生的反应是Pb+SO2-4-2e-=PbSO4
B.在放电时,该电池的两极板质量增加相同
C.在充电时,电池中每转移1mol电子,理论上生成1mol硫酸
D.在充电时,阴极发生的反应是PbSO4-2e-+2H2O=PbO2+SO2-4+4H+难度: 中等查看答案及解析
-
合成氨反应的热化学方程式为:N2(g)+3H2(g)
2NH3(g);△H=-92.4kJ/mol现将1molN2和3molH2加入到2L的固定密闭容器中,在500℃下进行反应,10min达到平衡,NH3的体积分数为ω.下列说法正确的是( )
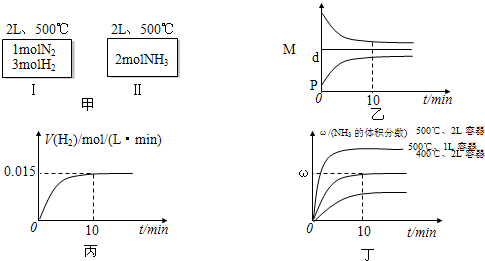
A.如甲图所示:Ⅰ、Ⅱ两种途径中达到平衡时,NH3的体积分数均为ω,且Ⅰ中放出的热量与Ⅱ中吸收的热量之和为92.4kJ
B.反应进程中,混合气体的平均相对分子质量(M)、混合气体的密度(d)、混合气体的压强(P)三者的变化趋势如图乙所示
C.若达到平衡时放出的热量为9.24kJ,则氢气的反应速度变化曲线如图丙所示
D.若起始加入的物料均为1molN2、3molH2,在不同条件下达到平衡时,NH3的体积分数变化曲线如丁图所示难度: 中等查看答案及解析