-
下列说法不正确的是
A. Ksp只与难溶电解质的性质和温度有关
B. 由于Ksp(ZnS)>Ksp(CuS),所以ZnS沉淀在一定条件下可转化为CuS沉淀
C. 其他条件不变,离子浓度改变时,Ksp不变
D. 两种难溶电解质作比较时,Ksp小的,溶解度一定小
难度: 简单查看答案及解析
-
根据盖斯定律判断如图所示的物质转变过程中正确的是( )
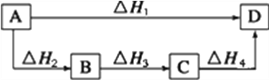
A. △H1=△H2=△H3=△H4 B. △H1+△H2=△H3+△H4
C. △H1+△H2+△H3=△H4 D. △H1=△H2+△H3+△H4
难度: 简单查看答案及解析
-
在密闭容器中进行可逆反应,A与B反应生成C,其反应速率分别用υ(A) υ(B)、υ(C)(mol·L-1·s-1)表示,且υ(A)、υ(B)、υ(C)之间有如下所示关系:υ(B)=3υ(A);3υ(C)=2υ(B)。则此反应可表示为( )
A. 2A+3B=2C B. A+3B=2C
C. 3A+B
2C D. A+3B
2C
难度: 中等查看答案及解析
-
对于A2+3B2
2C+D的反应来说,以下化学反应速率的表示中,反应速率最快的是( )
A. v(B2)=0.8mol(L·s)﹣1 B. v(A2)=0.4 mol(L·s)﹣1
C. v(C)=0.6 mol(L·s)﹣1 D. v(D)=0.1 mol(L·s)﹣1
难度: 中等查看答案及解析
-
反应:A(气)+3B(气)
2C(气); ΔH<0达平衡后,将气体混合物的温度降低,下列叙述中正确的是( )
A. 正反应速率加大,逆反应速率变小,平衡向正反应方向移动
B. 正反应速率变小,逆反应速率加大,平衡向逆反应方向移动
C. 正反应速率和逆反应速率都变小,平衡向正反应方向移动
D. 正反应速率和逆反应速率都变小,平衡向逆反应方向移动
难度: 中等查看答案及解析
-
化学平衡常数可以用 K 来表示,下列关于 K 的说法中正确的是( )
A. K 越大,反应物的转化率越小 B. K 与温度一定有关
C. K 与生成物的浓度一定有关 D. K 与反应物的浓度一定有关
难度: 中等查看答案及解析
-
用物质的量都是0.1mol的CH3COOH和CH3COONa配制成1L混合溶液,已知其中c(CH3COO-)大于c(Na+)。对该混合溶液的下列判断正确的是( )
A. c(OH-)> c(H+) B. c(CH3COOH)+c(CH3COO-)=0.2mol/L
C. c(CH3COOH)>c(CH3COO-) D. c(CH3COO-)+c(OH-)=0.2mol/L
难度: 中等查看答案及解析
-
在250C某稀溶液中,由水电离产生的c(H+)=10-13mol/L,下列有关溶液的叙述正确的是( )
A.该溶液一定呈酸性 B.该溶液一定呈碱性
C.该溶液的pH可能为1 D.该溶液的pH为7
难度: 中等查看答案及解析
-
下列根据反应原理设计的应用,不正确的是
A. CO32-+H2O
HCO3-+OH-:用热的纯碱溶液清洗油污
B. A13++3H2O
Al(OH)3(胶体)+3H+:明矾净水
C. TiCl4+(x+2)H2O(过量)
TiO2·xH2O↓+4HCl:制备TiO2纳米粉
D. SnCl2+H2O
Sn( OH)Cl↓+HCl配制氯化亚锡溶液时加入氢氧化钠溶液
难度: 中等查看答案及解析
-
铜锌原电池(如下图盐桥中含有KCl)工作时,下列叙述错误的是( )
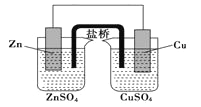
A. 负极反应为:Zn-2e- =Zn2+
B. 电池总反应为:Zn+Cu2+ =Zn2++Cu
C. 在外电路中,电子从负极流向正极
D. 盐桥中的K+移向ZnSO4 溶液
难度: 中等查看答案及解析
-
下列过程需要通电后才可以发生或进行的是( )
①电离 ②电泳 ③电解 ④电镀 ⑤电化学腐蚀
A. ①② B. ②③④
C. ②③④⑤ D. 全部
难度: 中等查看答案及解析
-
原电池的电极名称不仅与电极材料的性质有关,也与电解质溶液有关。下列说法中不正确的是( )
A. Al、Cu、稀H2SO4组成原电池,负极反应式为:Al-3eˉ=Al3+
B. Mg、Al、NaOH溶液组成原电池,其负极反应式为:Al-3eˉ+4OHˉ=AlO2ˉ+2H2O
C. 由Al、Cu、浓硝酸组成原电池,负极反应式为:Cu-2eˉ=Cu2+
D. 由Fe、Cu、FeCl3溶液组成原电池,负极反应式:Cu-2eˉ=Cu2+
难度: 中等查看答案及解析
-
用惰性电极电解下列各组中的三种电解质溶液,在电解的过程中,溶液的pH依次为升高、不变、降低的是( )
A.AgNO3 CuCl2 Cu(NO3)2
B.KCl Na2SO4 CuSO4
C.CaCl2 KOH NaNO3
D.HCl HNO3 K2SO4
难度: 中等查看答案及解析
-
下列有关说法正确的是
A.为保护海轮的船壳,常在船壳上镶入锌块
B.明矾溶于水可以使水净化,是因为明矾中的Al3+水解显酸性
C.己知工业合成氨气∆H<0,达平衡后,升高温度,正反应速率减小,逆反应速率增大
D.NH3(g) + HCl(g)=NH4Cl(s)是熵减小的反应,较低温度下能自发进行,说明该反应的∆H>0
难度: 中等查看答案及解析
-
N—H键能的含义是( )
A. 由N和H形成1 mol NH3所放出的热量
B. 把1 mol NH3的键全部拆开所吸收的热量
C. 拆开6.02×1023个N—H键所吸收的能量
D. 形成1个N—H键所放出的热量
难度: 简单查看答案及解析
-
下列过程中△H小于零的是
A. 氯酸钾分解制氧气 B. 氯化铵加热制备氨气
C. 氢气还原氧化铜 D. 实验室制备氢气
难度: 简单查看答案及解析
-
氢气是人类最理想的能源。已知在25℃、101 kPa下,1 g 氢气完全燃烧生成液态水时放出热量142.9 kJ,则下列热化学方程式书写正确的是( )
A.2H2+O2=2H2O ΔH=-142.9 kJ·mol-1
B.2H2(g)+O2(g)=2H2O(l)ΔH=-142.9 kJ·mol-1
C.2H2(g)+O2(g)=2H2O(l)ΔH=-571.6 kJ·mol-1
D.2H2(g)+O2(g)=2H2O(l)ΔH=+571.6 kJ·mol-1
难度: 中等查看答案及解析
-
在相同条件下,一定量的氢气在氧气中充分燃烧并放出热量。若生成液态水放出的热量为Q1 kJ;若生成气态水放出的热量为Q2 kJ,那么Q1与Q2的大小关系是
A.Q1>Q2 B.Q1<Q2 C.Q1=Q2 D.不能确定
难度: 简单查看答案及解析
-
在一定条件下,充分燃烧一定量的丁烷放出热量Q kJ(Q>0),经测定完全吸收生成的CO2需消耗5 mol/L的KOH溶液100 mL,恰好生成正盐,则此条件下反应C4H10(g)+13/2O2(g)===4CO2(g)+5H2O(g)的ΔH为
A. +8Q kJ/mol B. +16Q kJ/mol
C. -8Q kJ/mol D. -16Q kJ/mol
难度: 中等查看答案及解析
-
已知:4NH3+5O2
4NO+6H2O,若反应速率分别用v(NH3)、v(O2)、v(NO)、v(H2O) [mol/(L·min)]表示,则正确的关系式是()
A. 4v(NH3)=5v(O2) B. 5v(O2)=6v(H2O)
C. 2v(NH3)=3v(H2O) D. 4v(O2)=5v(NO
难度: 中等查看答案及解析
-
已知反应A+3B=2C+D在某段时间内以A的浓度变化表示的化学反应速率为2 mol·L-1·s-1,则此段时间内用B的浓度变化表示的化学反应速率为( )。
A.5 mol·L-1·s-1 B.6 mol·L-1·s-1 C.2 mol·L-1·s-1 D.3 mol·L-1·s-1
难度: 简单查看答案及解析
-
已知反应4CO+2NO2
N2+4CO2在不同条件下的化学反应速率如下,其中表示反应速率最快的是( )
A. v(CO)=1.5 mol·L-1·min-1
B. v(NO2)=0.7 mol·L-1·min-1
C. v(N2)=0.4 mol·L-1·min-1
D. v(CO2)=1.1 mol·L-1·min-1
难度: 中等查看答案及解析
-
已知反应A2(g)+2B2(g)
2AB2(g) △H <0,下列说法正确的是( )
A. 升高温度,正向反应速率增加,逆向反应速率减小
B. 升高温度有利于反应速率增加,从而缩短达到平衡的时间
C. 达到平衡后,升高温度或增大压强都有利于该反应平衡正向移动
D. 达到平衡后,降低温度或减小压强都有利于该反应平衡正向移动
难度: 中等查看答案及解析
-
可逆反应2SO2(g)+O2(g)
2SO3(g)正在逆向进行时,正反应速率和逆反应速率的大小是( )
A. v正>v逆 B. v正<v逆
C. v正=v逆 D. 不能确定
难度: 简单查看答案及解析
-
一定条件下,2SO2(g)+O2(g)
2SO3(g) ΔH<0。下列有关叙述正确的是( )
A. 升高温度,v(正)变大,v(逆)变小
B. 恒温恒容,充入O2,O2的转化率升高
C. 恒温恒压,充入N2,平衡不移动
D. 恒温恒容,平衡前后混合气体的密度保持不变
难度: 中等查看答案及解析
-
下列物质属于弱电解质的是
A. 氯化钠 B. 蔗糖 C. 次氯酸 D. 硫酸
难度: 简单查看答案及解析
-
下表中物质的分类组合正确的是( )
选项
A
B
C
D
强电解质
Al2(SO4)3
BaSO4
HF
KClO3
弱电解质
H3PO4
H2O
CaCO3
Al(OH)3
非电解质
CO2
NH3·H2O
NH3
HI
A. A B. B C. C D. D
难度: 简单查看答案及解析
-
下列物质在水溶液中的电离方程式正确的是( )
A. H2S
2H++S2-
B. NaHCO3
Na++H++CO32—
C. NaHSO4===Na++H++SO42—
D. HF===H++F-
难度: 简单查看答案及解析
-
常温下,在0.1 mol·L-1CH3COOH溶液中,水的离子积是( )
A. 1.0×10-14 B. 1.0×10-13
C. 1.32×10-14 D. 1.32×10-15
难度: 中等查看答案及解析
-
下列仪器对应的名称正确的是( )
A.
三脚架
B.
 酸式滴定管
酸式滴定管C.
 长颈漏斗
长颈漏斗D.
 蒸发皿
蒸发皿难度: 简单查看答案及解析
-
下列各物质溶液显酸性的是( )
A. NaHCO3 B. CH3COONa C. NaCl D. NH4Cl
难度: 简单查看答案及解析
-
下列各组溶液的物质的量浓度均为0.1 mol·L-1:①H2S ②NaHS ③Na2S ④H2S和NaHS混合液。下列说法正确的是( )
A. 溶液pH从大到小的顺序是③>②>①>④
B. c(H2S)从大到小的顺序是①>④>②>③
C. 在H2S和NaHS混合液中:2c(Na+)=c(H2S)+c(HS-)+c(S2-)
D. 在NaHS溶液中:c(H+)+c(Na+)=c(OH-)+c(HS-)+c(S2-)
难度: 困难查看答案及解析
-
在一定的条件下发生下列反应,其中属于盐类水解反应的是( )
A. NH4++2H2O
NH3·H2O+H3O+ B. HCO3–+ H2O
H3O+ + CO32–
C. NH3 +H2O
NH4+ +OH– D. Cl2+H2O
H++Cl–+HClO
难度: 简单查看答案及解析
-
铁棒与石墨用导线连接后,浸入0.01 mo1·L-1的食盐溶液中,可能出现的现象是( )
A. 铁棒附近产生OH- B. 铁棒被腐蚀
C. 石墨棒上放出Cl2 D. 石墨棒上放出O2
难度: 中等查看答案及解析
-
一个原电池的总反应的离子方程式是Zn+Cu2+====Zn2++Cu,该反应的原电池的正确组成是( )
正极
负极
电解质溶液
A.
Zn
Cu
CuCl2
B.
Cu
Zn
CuSO4
C.
Zn
Cu
ZnCl2
D.
Cu
Zn
ZnSO4
A. A B. B C. C D. D
难度: 简单查看答案及解析
-
有关下列装置图的说法正确的是

A.若X是盐桥,则上述装置可以形成原电池
B.若X是铜条,则上述装置不发生任何反应
C.若X是铜条,上述装置中,B电极是阴极
D.若X是铜条,上述装置中,A电极的电极反应式是:Cu2+ + 2e-=Cu
难度: 中等查看答案及解析
-
美国NASA曾开发一种铁—空气二次电池。该电池放电时,其原理如下图所示,电池反应为:2 Fe+O2+2H2O=2Fe(OH)2。
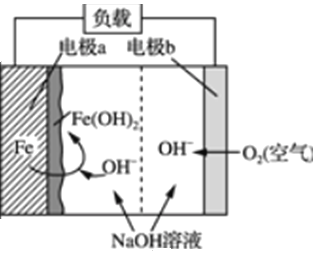
有关该电池放电时的说法正确的是 ( )
A. 由电能转变为化学能 B. a极质量不变
C. b极为电池负极 D. 电子由a极经负载流向b极
难度: 困难查看答案及解析
-
原电池的正极和电解池的阴极所发生的反应分别是( )
A.氧化、还原 B.还原、氧化
C.氧化、氧化 D.还原、还原
难度: 简单查看答案及解析
-
关于电解法精炼铜的下列说法正确的是( )
A. 粗铜作阳极,纯铜作阴极,硫酸铜为电解质溶液
B. 纯铜作阳极,粗铜作阴极,硫酸铜为电解质溶液
C. 电解结束后,溶液中Cu2+浓度不变
D. 电解结束后,溶液中Cu2+浓度变大
难度: 简单查看答案及解析
-
下列各项关于铜电极的叙述正确的是( )
A. 铜锌原电池中铜是负极
B. 用电解法精炼粗铜时粗铜作阴极
C. 在镀件上镀铜时可用金属铜作阳极
D. 电解稀硫酸制H2、O2时铜作阳极
难度: 中等查看答案及解析
-
有如右图装置,下列有关该装置的叙述正确的是( )

A. 锌极附近滴入酚酞,溶液呈红色。
B. 铁极发生的电极反应为:2H2O+O2+4e=4OH-
C. 铁极发生了吸氧腐蚀
D. 溶液中的OH-离子向铁极移动
难度: 简单查看答案及解析
-
下列叙述的方法不正确的是 ( )
A. 金属的电化学腐蚀比化学腐蚀更普遍
B. 用铝质铆钉铆接铁板,铁板易被腐蚀
C. 钢铁在干燥空气中不易被腐蚀
D. 用牺牲锌块的方法来保护船身
难度: 中等查看答案及解析
-
已知:2CO(g)+O2(g)===2CO2(g);ΔH=-566 kJ·mol-1
N2(g)+O2(g)===2NO(g);ΔH=+180 kJ·mol-1
则2CO(g)+2NO(g)===N2(g)+2CO2(g)的ΔH是( )
A. -386 kJ·mol-1 B. +386 kJ·mol-1
C. -746 kJ·mol-1 D. +746 kJ·mol-1
难度: 简单查看答案及解析


