-
生活中常见的下列物质,属于溶液的是( )
A.牛奶
B.泥水
C.生理盐水
D.植物油难度: 中等查看答案及解析
-
下列各图表示的变化中,只属于物理变化的是( )
A. 火箭发射
火箭发射
B.
煤的燃烧
C.
风力发电
D.
酸雨侵蚀难度: 中等查看答案及解析
-
酸类物质具有相似的化学性质,本质的原因是( )
A.能与指示剂作用
B.能与碱发生中和反应
C.能解离出H+
D.都含有氢元素难度: 中等查看答案及解析
-
下列关于溶液的说法:①无色;②混合物;③化合物;④均一;⑤稳定;⑥各部分性质相同,其中正确的是( )
A.①③④⑤
B.②④⑤⑥
C.①②④⑤
D.①③⑤⑥难度: 中等查看答案及解析
-
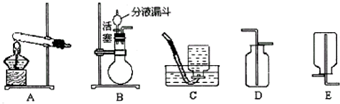
用氯化钠固体配制一定质量分数的溶液时,不需要用的仪器是( )
A.
B.
C.
D.
难度: 中等查看答案及解析
-
下列药品中,不需要密闭保存的是( )
A.浓盐酸
B.浓硫酸
C.碳酸钠
D.烧碱难度: 中等查看答案及解析
-
2008年奥林匹克运动会将在我国北京举行,可能会用大型遥控飞艇作为宣传工具以渲染活动气氛.为了飞艇在空中飞行安全而有效,你认为飞艇内最好充入的气体是( )
A.氢气
B.氦气
C.甲烷
D.氮气难度: 中等查看答案及解析
-
下列物质的名称、俗名与化学式完全对应的是( )
A.氢氧化钙 熟石灰 CaO
B.碳酸钠 火碱 Na2CO3
C.氯化钠 食盐 NaCl
D.氢氧化钠 纯碱 NaOH难度: 中等查看答案及解析
-
佛山市三水健力宝生产的“魔水”驰名中外.“魔水”内溶有一定量的二氧化碳气体.打开瓶塞.“魔水”会自动喷出.喝了“魔水”后常会打嗝.说明气体在水中的溶解度与压强、温度有关.以下关于气体溶解度的说法正确的是( )
A.压强增大,气体溶解度不变
B.压强减小,气体溶解度增大
C.温度升高,气体溶解度减小
D.温度降低,气体溶解度减小难度: 中等查看答案及解析
-
新型镁合金被大量应用于制成笔记本电脑外壳、竞赛自行车框架等,这说明镁合金具有的优异性能是( )
①熔点低 ②硬度大 ③延展性好 ④导电性强 ⑤密度小 ⑥耐腐蚀.
A.①②③
B.②③④
C.①③⑥
D.②⑤⑥难度: 中等查看答案及解析
-
下列现象不属于乳化现象在生活中的应用的是( )
A.用洗洁精洗去餐具上的油污
B.用肥皂液洗涤衣服上的油渍
C.用汽油洗去衣服上沾染的油污
D.用乳化剂稀释难溶于水的液态农药难度: 中等查看答案及解析
-
测得生活中一些物质的pH如下表,其中呈碱性的物质是( )
物质 洗涤剂 食盐水 柠檬汁 胃 液 pH 12.2 7.0 2.5 1.2
A.洗涤剂
B.食盐水
C.柠檬汁
D.胃液难度: 中等查看答案及解析
-
下列各图均表示某些酸、碱、盐溶液间的混合,其中属于中和反应的是( )
A.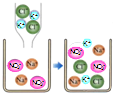
KCl溶液滴入NaNO3溶液
B.
稀盐酸滴入NaOH溶液
C.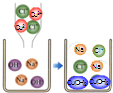
CuCl2溶液滴入NaOH溶液
D.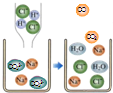
稀盐酸滴入纯碱溶液难度: 中等查看答案及解析
-
几种物质间的转化关系(反应条件均省略),其中可以通过置换反应实现的转化有( )
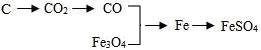
A.一个
B.二个
C.三个
D.四个难度: 中等查看答案及解析
-
冬天,人们常用甘油溶液护肤,使皮肤保持湿润.质量分数为80%的甘油溶液护肤效果最佳.配制80%的甘油溶液500g,所需甘油的质量为( )
A.80g
B.40g
C.400g
D.100g难度: 中等查看答案及解析
-
向某盐酸中逐滴加入氢氧化钠溶液,所得溶液的pH与加入氢氧化钠溶液的质量关系曲线图合理的是( )
A.
B.
C.
D.难度: 中等查看答案及解析
-
印刷铜制电路板的“腐蚀液”为FeCl3溶液.已知铜铁均能与FeCl3溶液反应,反应方程式分别为:Cu+2FeCl3═2FeCl2+CuCl2,Fe+2FeCl3═3FeCl2.现将一包铜、铁的混合粉末加入到盛有FeCl3溶液的烧杯中,充分反应后烧杯中仍有少量固体,关于烧杯中物质的组成的说法正确的是( )
A.溶液中一定含有FeCl3,固体一定是铁和铜
B.溶液中一定含有FeCl2,固体一定含有铜
C.溶液中一定含有FeCl2、CuCl2,固体一定含铜
D.溶液中一定含有FeCl2,固体一定是铁和铜难度: 中等查看答案及解析
-
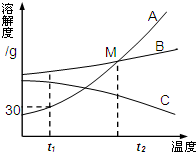
如图是a、b、c、d四种固体物质的溶解度曲线;图表是这些固体物质在部分温度时的溶解度.根据图表信息判断下列说法正确的是( )
NaCl KCl NH4Cl KNO3 10°C 35.8g 31.0g 33.3g 20.9g 60°C 37.3g 45.5g 55.2g 110.0g 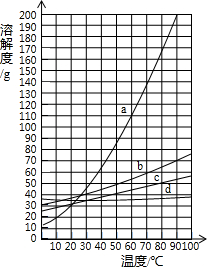
A.图中a曲线表示KNO3的溶解度曲线
B.b的溶解度小于a的溶解度
C.要从a与d的混合物中得到a,通常采用蒸发溶剂使其结晶的方法
D.KCl的不饱和溶液由60℃降温至10℃时变成饱和溶液难度: 中等查看答案及解析
-
除去下列各物质中的少量杂质所选用的试剂及操作方法均正确的是( )
项目 物质 杂质(少量) 试剂 操作方法 A KCl MnO2 足量的水 溶解、过滤、蒸发 B H2 水蒸气 适量的NaOH溶液 洗气 C FeSO4溶液 CuSO4溶液 过量的Fe粉 过滤 D CO CO2 足量氧化铁 加热
A.A
B.B
C.C
D.D难度: 中等查看答案及解析
-
A图表示硝酸钾和氢氧化钙的溶解度随温度变化的情况.B图中甲、乙试管分别盛有硝酸钾、氢氧化钙的饱和溶液,试管底部均有未溶解的固体.向烧杯中加入某种物质后,甲试管中的固体减少,乙试管中的固体增加,则加入的物质可能是( )
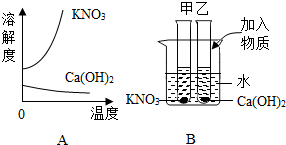
A.浓硫酸
B.硝酸铵
C.氧化钙
D.氯化钠难度: 中等查看答案及解析