-
短周期元素A、B、C的原子序数之和为37,A、B在同一周期,A+、C-具有相同的核外电子层结构。下列推测不正确的是( )
A. 同周期元素中C的氢化物稳定性最强
B. 同周期元素中A的金属性最强
C. 原子半径:A>B,离子半径:A+>C-
D. A、B、C的简单离子中,会破坏水的电离平衡的是C
难度: 简单查看答案及解析
-
下列有关说法中正确的是
A. 制作航天服的聚酯纤维和用于光缆通信的光导纤维都是新型无机非金属材料
B. 绿色化学的核心是应用化学原理对环境污染进行治理
C. 目前科学家已经制得单原子层锗,其电子迁移率是硅的10倍,有望取代硅用于制造更好的晶体管
D. 纤维素在人体内可水解为葡萄糖,是人类重要的营养物质之一
难度: 中等查看答案及解析
-
已知苯(
)分子有一类氢原子,其中二氯代物有3种,萘(
)分子有两类氢原子,其中二氯代物有10种,蒽(
 )分子有三类氢原子,其中二氯代物有
)分子有三类氢原子,其中二氯代物有A. 13种 B. 15种 C. 18种 D. 20种
难度: 困难查看答案及解析
-
下列实验中,对应的实验现象以及结论都正确且两者具有因果关系的是
选项
实验操作
实验现象
结论
A
将KI溶液滴入FeCl3溶液中,加入CCl4,振荡、静置
下层溶液显紫色
还原性:Fe2+<I-
B
将SO2通入滴有酚酞的NaOH溶液中
溶液红色褪去
SO2具有漂白性
C
将稀盐酸滴入Na2SiO3溶液中
溶液中出现凝胶
非金属性:Cl>Si
D
将稀硫酸滴入淀粉溶液中,加热一段时间,再加入新制的Cu(OH)2悬浊液并加热
溶液中未出现砖红色沉淀
淀粉未水解
A. A B. B C. C D. D
难度: 困难查看答案及解析
-
下列过程中,没有明显实验现象的是
A. 向Fe(NO3)2溶液中滴加稀硫酸 B. 将HCl通入NaAlO2溶液中
C. 加热溶有SO2的品红溶液 D. 向碳酸氢钠溶液中滴加氢氧化钠溶液
难度: 困难查看答案及解析
-
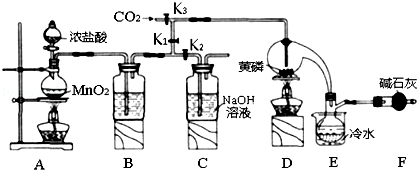
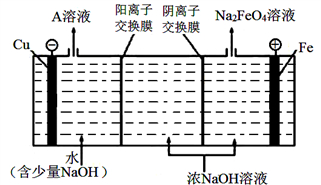
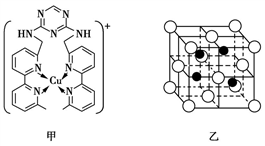
有一种瓦斯分析仪(下图甲)能够在煤矿巷道中的甲烷达到一定浓度时,通过传感器显示出来。该瓦斯分析仪工作原理类似燃料电池的工作原理,其装置如下图乙所示,其中的固体电解质是Y2O3-Na2O,O2-可以在其中自由移动。

下列有关叙述正确的的是
A. 瓦斯分析仪工作时,电池内电路中电子由电极b流向电极a
B. 电极b是正极, O2-由电极a流向电极b
C. 电极a的反应式为:CH4+5O2-―8e-=CO32- +2H2O
D. 当固体电解质中有1 mol O2-通过时,电子转移4 mol
难度: 困难查看答案及解析
-
常温下,取20mL某浓度的盐酸作为待测液,用一定物质的量浓度的NaOH溶液进行滴定(假设盐酸与NaOH溶液混合后体积变化忽略不计),滴定过程中溶液的pH变化如图所示。下列叙述正确的是
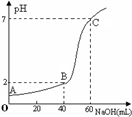
A. 所用盐酸的浓度是0.09mol·L-1,NaOH溶液浓度为0.03mol·L─1
B. 在B点,溶液中离子浓度关系为:c(Cl─)>c(Na+)>c(OH-)>c(H+)
C. A、B、C三点水的电离程度大小依次为:A>B>C
D. 滴定前,锥形瓶用待测液润洗,导致盐酸浓度偏低
难度: 困难查看答案及解析


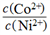 的值等于_____。
的值等于_____。

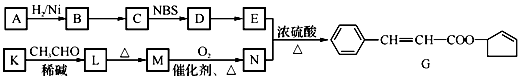
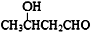 、
、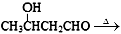 CH3CH=CHCHO+H2O
CH3CH=CHCHO+H2O