-
下列说法不正确的是
A. 有机物分子中一定含有一个或多个碳原子
B. 有机物分子中的碳原子可以相互连接成链状或环状
C. 有机物分子中的碳原子可以与其它元素的原子连接
D. 分子中含有碳原子的化合物一定是有机化合物
难度: 简单查看答案及解析
-
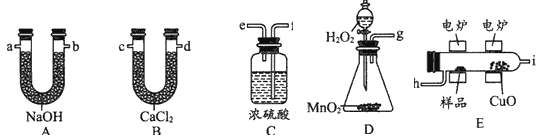
有机物的分离和提纯是有机化学研究的重要内容,分离和提纯下列物质所用的方法不正确的是
A.酒精和水——分液 B.淀粉中混有氯化钠——用半透膜进行渗析
C.汽油和柴油——分馏 D.三氯甲烷和水——分液
难度: 中等查看答案及解析
-
分子式为C5H12O且可与金属钠反应放出氢气的有机物有(不考虑立体异构)
A. 5 种 B. 6 种 C. 8种 D. 7种
难度: 中等查看答案及解析
-
下列有机物的命名中,正确的是( )
A. 2,2﹣二甲基丁烷 B. 3,3﹣二甲基丁烷
C. 2﹣乙基丁烷 D. 2,3,3﹣三甲基丁烷
难度: 简单查看答案及解析
-
己知二氯丁烷的同分异构体有9 种,则八氯丁烷的同分异构体有
A. 9 种 B. 8种 C. 7种 D. 10种
难度: 简单查看答案及解析
-
下列说法正确的是
A. 乙烷的一氯代物同分异构体有1种,二氯代物的同分异构体有3 种
B. 正戊烷的一氯代物同分异构体有3 种,二氯代物的同分异构体有9 种
C. 正丁烷的一氯代物同分异构体有2 种,二氯代物的同分异构体有5 种
D. 丙烷的一氯代物同分异构体有2 种,二氯代物的同分异构体有5 种
难度: 困难查看答案及解析
-
某化合物6.4g在氧气中完全燃烧,只生成8.8 gCO2和7.2 gH2O。下列说法中正确的是
①该化合物仅含碳、氢两种元素 ②该化合物中碳、氢原子个数比为1∶4
③无法确定该化合物是否含有氧元素 ④该化合物中一定含有氧元素
A. ②④ B. ①② C. ③④ D. ②③
难度: 中等查看答案及解析
-
下列说法中正确的是
A. 二氧化硫溶于水能导电,故二氧化硫属于电解质
B. 氢氧根离子浓度相同的氢氧化钠溶液和氨水导电能力相同
C. 硫酸是强电解质,故纯硫酸能导电
D. 硫酸钡难溶于水,故硫酸钡属于弱电解质
难度: 中等查看答案及解析
-
下列溶液一定显酸性的是
A. 溶液中c (OH-)>c (H+) B. pH<7 的溶液
C. 溶液中c (H+) =10-6mol·L-1 D. 滴加紫色石蕊试液后变红色的溶液
难度: 简单查看答案及解析
-
在铁制品上镀一定厚度的锌层,以下方案设计正确的是
A. 锌作阳极,镀件作阴极,溶液中含有锌离子
B. 铂作阴极,镀件作阳极,溶液中含有锌离子
C. 铁作阳极,镀件作阴极,溶液中含有亚铁离子
D. 锌作阴极,镀件作阳极,溶液中含有锌离子
难度: 中等查看答案及解析
-
下列说法正确的是 ( )
A. 将AlCl3溶液和Al2(SO4)3溶液分别加热、蒸干、灼烧,所得固体成分相同
B. 配制FeSO4溶液时,将FeSO4固体溶于稀盐酸中,然后稀释至所需浓度
C. 用加热的方法可以除去KCl溶液中的Fe3+
D. 洗涤油污常用热的碳酸钠溶液
难度: 中等查看答案及解析
-
下面提到的问题中,与盐的水解有关的是 ( )
①明矾和FeCl3可作净水剂
②为保存FeCl3溶液,要在溶液中加少量盐酸
③用NaHCO3与Al2(SO4)3两种溶液可作泡沫灭火剂
④在NH4Cl溶液中加入金属镁会产生氢气
A.①③④ B.②③ C.全部 D.①②④
难度: 中等查看答案及解析
-
物质的量浓度相同的下列溶液中,按pH由小到大顺序排列的是( )
A. Na2CO3NaHCO3NaCl HCl
B. Na2CO3NaHCO3HCl NaCl
C. (NH4)2SO4NH4Cl NaNO3Na2CO3
D. NH4Cl (NH4)2SO4Na2CO3NaNO3
难度: 中等查看答案及解析
-
已知常温下,Ksp(AgCl)=1.8×10-10,Ksp(AgI)=8.3×10-17。下列叙述中正确的是
A. 常温下,AgCl 在NaCl溶液中的Ksp比在纯水中的Ksp小
B. 将0.001mol·L-1的AgNO3溶液滴入KC1和KI 的混合溶液中,一定先析出AgI 沉淀
C. 向AgCl的悬浊液中加入少量KI 溶液,沉淀由白色转化为黄色
D. 向AgCl饱和溶液中加入NaCl晶体,有AgC1析出且溶液中c(Ag+)=c(C1-)
难度: 中等查看答案及解析
-
化学上常认为残留在溶液中的离子浓度小于1×10﹣5 mol·L﹣1时,沉淀就达完全。已知:常温下Ksp[M(OH)2]=1×10﹣21.则溶液中M2+沉淀完全时的pH为( )
A. 7 B. 6 C. 5 D. 4
难度: 简单查看答案及解析
-
室温条件下,现有四种溶液:①pH=2的CH3COOH溶液;②pH=2的HCl溶液;③pH=12的氨水;④pH=12的NaOH溶液,下列有关说法正确的是
A. 由水电离出的c(H+):①=②=③=④
B. 将②、③溶液混合后,pH=7,消耗溶液的体积:③=②
C. 等体积的①、②、④溶液分别与足量铝粉反应,②生成的H2的物质的量最大
D. 向溶液中加入100mL水后,溶液的pH:③>④>①>②
难度: 中等查看答案及解析
-
下列有关电解质溶液中粒子浓度关系正确的是
A. pH=a的醋酸溶液,稀释10倍后,其pH=b,则a=b-1
B. 含等物质的量的NaHSO3和Na2SO3的溶液:2c(Na+)=3[c(HSO3-)+c(SO32-)+c(H2SO3)]
C. 0.1mol·L-1盐酸与0.2mol·L-1氨水等体积混合:c(NH3·H2O)>c(Cl-)>c(NH4+)>c(OH-)
D. 含有AgCl和AgI固体的悬浊液:c(Ag+)>c(Cl-)=c(I-)
难度: 简单查看答案及解析
-
1个C 原子的单键氢化物分子是CH4,2个C原子的单键氢化物分子则为C2H6,以下各对分子间不存在类似关系的是
A. NH3与N2H4 B. SCl4与S2Cl2 C. SF6与S2F10 D. H2O与H2O2
难度: 困难查看答案及解析
-
下列表示物质结构的化学用语或模型正确的是
A. 乙烷的分子式:CH3CH3 B. CH4分子的球棍模型:

C. 乙醛结构简式:CH3COH D. 乙烯的结构简式:CH2=CH2
难度: 简单查看答案及解析
-
下列各对物质,互为同系物的是( )
A.CH3—CH===CH2与
B.
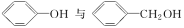
C.CH3COOCH3与CH3CH2COOCH3 D.CH3CH2Cl与CH3CHCl—CH2Cl
难度: 中等查看答案及解析
-
有机物分子
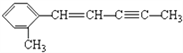 中最多有多少个原子共面( )
中最多有多少个原子共面( )A. 18 B. 19 C. 20 D. 21
难度: 中等查看答案及解析
-
在核磁共振氢谱中出现两组峰,其氢原子数之比为3︰2的化合物是

A. A B. B C. C D. D
难度: 中等查看答案及解析
-
有机物
 有多种同分异构体,其中属于酯且含有苯环结构的共有( )
有多种同分异构体,其中属于酯且含有苯环结构的共有( )A. 3种 B. 4种 C. 5种 D. 6种
难度: 中等查看答案及解析
-
某烃中碳元素和氢元素的质量比为24∶5,该烃在标准状况下的密度是2.59 g·L-1,则分子式为 ( )
A. C2H6 B. C4H10 C. C5H8 D. C7H8
难度: 简单查看答案及解析
-
对于反应A2+3B2=2C来说,以下表示中,反应速率最快的是( )
A. v(B2)="0.8" mol/(L•s) B. v(A2)="0.4" mol/(L•s)
C. v(C)="0.6" mol/(L•s) D. v(B2)="1.8" mol/(L•s)
难度: 简单查看答案及解析
-
铜板上铁铆钉长期暴露在潮湿的空气中,形成一层酸性水膜后铁铆钉会被腐蚀,示意图如下。下列说法不正确的是
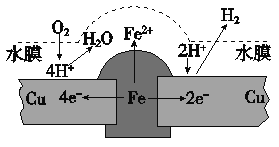
A. 因铁的金属性比铜强,所以铁铆钉被氧化而腐蚀
B. 若水膜中溶解了SO2,则铁铆钉腐蚀的速率变小
C. 铜极上的反应是2H+ + 2e- = H2↑,O2 + 4e-+ 4H+ = 2H2O
D. 在金属表面涂一层油脂,能防止铁铆钉被腐蚀
难度: 中等查看答案及解析
-
一定条件下,Na2CO3溶液中存在如下平衡:CO
+H2O
HCO
+OH-,下列说法正确的是( )
A. 稀释溶液,平衡正向移动,
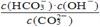 增大
增大B. 通入CO2,平衡逆向移动,溶液pH减小
C. 加入NaOH固体,平衡逆向移动,pH减小
D. 升高温度,
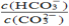 增大
增大难度: 困难查看答案及解析
-
常温下:某NaHSO3溶液的pH=5,则在NaHSO3溶液中微粒的物质的量浓度关系一定正确的是( )
A. c(Na+)>c(HSO3﹣)>c(OH﹣)>c(H+)>(SO32﹣)
B. c(Na+)+c(H+)=c(OH﹣)+c(SO32﹣)+c(HSO3﹣)
C. c(Na+)=c(SO32﹣)+c(HSO3﹣)+c(H2SO3)
D. c(OH﹣)=c(H+)+c(HSO3﹣)+c(H2SO3)
难度: 中等查看答案及解析
-
下列热化学方程式书写正确的是(△H的绝对值均正确)( )
A. S(s)+O2(g)═SO2(g);△H=﹣296.8 kJ•mol﹣1(反应热)
B. NaOH(aq)+HCl(aq)═NaCl(aq)+H2O(l);△H=+57.3 kJ•mol﹣1(中和热)
C. C2H5OH(l)+3O2(g)═2CO2(g)+3H2O(g);△H=﹣1 367.0 kJ•mol﹣1(燃烧热)
D. 2NO2═O2+2NO;△H=+116.2 kJ•mol﹣1(反应热)
难度: 中等查看答案及解析
-
25 ℃时纯水的电离度为a1,pH=2 的醋酸溶液的电离度为a2,pH=12 的氢氧化钠溶液中水的电离度为a3。 若将上述醋酸与氢氧化钠溶液等体积混合,所得溶液中水的电离度为a4。下列关系式中正确的是
A. a3=a2<a1<a4 B. a2=a3<a4<a1
C. a2<a3<a1<a4 D. a1<a2<a3<a4
难度: 中等查看答案及解析
 ___________________________________;
___________________________________;