-
地壳中含量最多的元素是
A.氧 B.硅 C.铝 D.铁
难度: 中等查看答案及解析
-
空气成分中,能供给呼吸的气体是
A.氮气 B.氧气 C.二氧化碳 D.稀有气体
难度: 中等查看答案及解析
-
下列变化属于物理变化的是
A.酒精挥发 B.牛奶变酸 C.蔬菜腐烂 D.高粱酿酒
难度: 中等查看答案及解析
-
青少年体内因缺乏钙元素易患的疾病是
A.甲状腺肿大 B.贫血 C.佝偻病 D.夜盲症
难度: 中等查看答案及解析
-
将下列厨房里常用的物质分别放入水中,不能形成溶液的是
A.食盐 B.食用油 C.白醋 D.蔗糖
难度: 中等查看答案及解析
-
下列物质中,属于纯净物的是
A.蒸馏水 B.矿泉水 C.石灰水 D.汽水
难度: 中等查看答案及解析
-
下列物质中,能作磷肥的是
A.NH4NO3 B.CO(NH2)2 C.Ca(H2PO4)2 D.K2CO3
难度: 中等查看答案及解析
-
与元素化学性质关系最密切的是
A.质子数 B.电子数 C.中子数 D.最外层电子数
难度: 中等查看答案及解析
-
下列物质的化学式书写正确的是
A.硫酸铁(FeSO4) B.氢氧化铜(CU(OH)2) C.硝酸钠(NaNO3) D.氧化汞(AgO)
难度: 中等查看答案及解析
-
下列方法能够区分硬水和软水的是
A.观察颜色状态 B.加入活性炭搅拌
C.加入肥皂水搅拌 D.加入澄清石灰水搅拌
难度: 中等查看答案及解析
-
下列实验操作正确的是
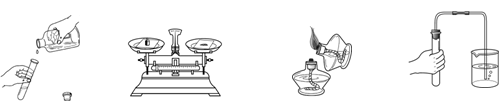
A.倾倒液体 B.称量固体 C.点燃酒精灯 D.检查装置的气密性
难度: 中等查看答案及解析
-
除去污水中的异味最有效的方法是
A.搅拌 B.过滤 C.静置 D.吸附
难度: 中等查看答案及解析
-
下列做法会损害身体健康的是
A.用生石灰做食品干燥剂 B.向汤中放入适量加碘食盐
C.用甲醛溶液浸泡海产品 D.用小苏打作焙制糕点的发酵粉
难度: 中等查看答案及解析
-
下图表示的是身边一些物质在常温时的近似pH。下列叙述不正确的是
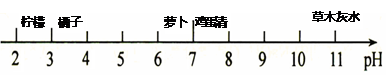
A.草木灰水呈碱性 B.鸡蛋清呈碱性
C.橘子汁的酸性比萝卜汁的酸性弱 D.柠檬汁能使紫色石蕊溶液变红
难度: 中等查看答案及解析
-
下列安全措施不正确的是
A.加油站内及附近,要严禁烟火
B.少量天然气泄漏,立即关闭阀门并开窗通风
C.不慎将燃着的酒精灯碰倒,立即用湿布盖灭
D.正在使用的家用电器着火,立即用水浇灭
难度: 中等查看答案及解析
-
物质甲长期敞口放置会变质。下列说法正确的是
A.甲一定是氢氧化钠 B.甲变质一定是与氧气发生了反应
C.甲变质后质量一定会减小 D.甲变质一定是由化学反应引起的
难度: 中等查看答案及解析
-
物质的性质与用途有密切关系。下列说法不正确的是
A.干冰升华吸热,可用于人工降雨 B.氧气能支持燃烧,可用作燃料
C.洗洁精具有乳化功能,可用于去油污 D.熟石灰呈碱性,可用于改良酸性土壤
难度: 中等查看答案及解析
-
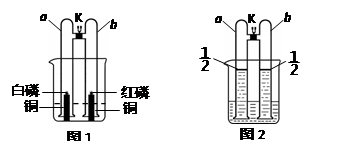
电解水的实验装置如右图所示。下列叙述不正确的是
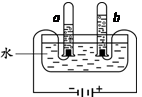
A.试管a中的气体是H2
B.试管b中的气体能使带火星的木条复燃
C.电解水产生的H2和O2的质量比为2∶1
D.电解水反应的化学方程式为2H2O
2H2↑+ O2↑
难度: 中等查看答案及解析
-
芜湖铁画是中国工艺美术中的一朵奇葩。它以低碳钢为主料,经锻打、焊接、酸洗和喷漆等多道工艺制成。下列叙述不正确的是
A.低碳钢具有延展性 B.给铁画喷漆既美观又防锈蚀
C.制铁画的原料生锈后可用稀盐酸清洗 D.制作铁画的多道工艺均属于物理变化
难度: 中等查看答案及解析
-
科学研究发现,金星大气的成分之一是三氧化二碳(C2O3)。实验证明三氧化二碳的化学性质与一氧化碳相似。下列关于三氧化二碳的叙述不正确的是
A.是一种有毒气体 B.能使澄清石灰水变浑浊
C.在一定条件下能还原氧化铁 D.在O2中充分燃烧的产物是CO2
难度: 中等查看答案及解析
-
化学中存在某些“相等”的关系。下列说法不正确的是
A.化学反应前后原子数目一定相等
B.中和反应前后溶液中水的质量相等
C.溶液加水稀释前后溶质的质量相等
D.化合物中元素的正化合价总和与负化合价总和的绝对值相等
难度: 中等查看答案及解析
-
一定质量的镁条在氧气中完全燃烧后生成氧化镁。固体质量随时间的变化关系如下图所示。其中M2与M1的差表示的是
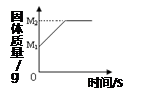
A.生成MgO的质量 B.参加反应的Mg的质量
C.参加反应的O2的质量 D.剩余的O2的质量
难度: 中等查看答案及解析
-
某净水丸分内外两层,对饮用水有杀菌消毒作用。使用时直接将它投入适量水中,外层的优氯净(C3O3N3Cl2Na)先与水反应,生成的次氯酸(HClO)具有杀菌消毒作用,几分钟后内层的亚硫酸钠(Na2SO3)会将水中的余氯(HClO等)除去。下列关于该净水丸的叙述正确的是
A.优氯净由4种元素组成
B.经过净水丸处理过的水为纯净物
C.使用净水丸时,要先破碎后再使用
D.除去余氯的反应之一:Na2SO3 + HClO = Na2SO4 + HCl,该反应不属于复分解反应
难度: 中等查看答案及解析
-
下列化学实验的“目的、操作、现象、结论”对应且合理的是
选项
目的
操作
现象
结论
A
检验集气瓶中是否集满二氧化碳
将燃烧的木条伸入集
气瓶中
木条火焰熄灭
集气瓶中已集满
二氧化碳
B
除去氢氧化钠溶液中的氢氧化钙
加过量的碳酸钠溶液,过滤
有白色沉淀产生
得到氢氧化钠溶液
C
探究物质溶解于
水的热量变化
向一定量的水中加入硝酸铵晶体,搅拌
溶液温度下降
盐类物质溶于水都能使溶液温度下降
D
比较铝和铜的金
属活动性
将砂纸打磨过的铝丝浸入硫酸铜溶液中
银白色铝丝表面有红色固体析出
铝比铜活泼
难度: 中等查看答案及解析
-
向氯化铜和稀盐酸的混合溶液中,加入过量的铁粉,充分反应后过滤。下列关于上述过程的叙述正确的是
A.滤液中一定含有FeCl3 B.过滤后得到的固体可能是纯净物
C.反应后固体的质量可能会增加 D.反应后溶液的质量一定会减少
难度: 中等查看答案及解析