-
据中央电视台报道,近年来我国的一些沿江城市多次出现大雾天气,致使高速公路关闭,航班停飞,雾中小水滴直径范围是( )
A、小于1nm B、在1nm~100nm间
C、大于100nm D、无法确定
难度: 简单查看答案及解析
-
下列物质中属于纯净物、化合物、钙盐的是( )
A、生石灰 B、熟石灰 C、碳酸钙 D、石灰石
难度: 简单查看答案及解析
-
下列反应不属于四种基本反应类型,但属于氧化还原反应的是( )
A、Fe + CuSO4 == FeSO4 + Cu
B、AgNO3 + NaCl == AgCl↓ + NaNO3
C、MnO2 + 4 HCl(浓) MnCl2 + Cl2↑ + 2 H2O
D、2KMnO4
K2MnO4 + MnO2 + O2↑
难度: 简单查看答案及解析
-
下列物质属于非电解质的是( )
A、HCl B、Fe C、蔗糖溶液 D、CH3CH2OH
难度: 简单查看答案及解析
-
现有下列四种因素:① 温度和压强 ② 所含微粒数 ③ 微粒本身大小 ④ 微粒间的距离,其中对气体物质体积有显著影响的是( )
A、① ② ③ B、① ③ ④
C、① ② ④ D.、① ② ③ ④
难度: 简单查看答案及解析
-
设NA表示阿伏加德罗常数的值,下列说法中正确的是( )
A、1 mol NH4+ 所含质子数为11NA
B、18g水中含有的电子数目为3 NA
C、标准状况下,11.2L水所含分子数为0.5NA
D、常温常压下,48gO3含有的氧原子数为NA
难度: 简单查看答案及解析
-
下列粒子的结构示意图中,表示同种元素的粒子的是( )
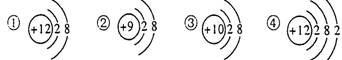
A、①② B、②③ C、③④ D、①④
难度: 简单查看答案及解析
-
做焰色反应实验用的铂丝,每试验一种样品后都必须 ( )
A、用水洗涤2~3次后再使用
B、用盐酸洗涤后,经蒸馏水冲洗,方可使用
C、用滤纸擦干后才可使用
D、用盐酸洗涤后,再在酒精灯火焰上灼烧到没有颜色,才可使用
难度: 简单查看答案及解析
-
在相同条件下,A容器中的CH4和B容器中的NH3所含氢原子数相等,则两个容器的体积比是( )
A、 1︰1 B、 4︰3 C、3︰4 D、 5︰4
难度: 简单查看答案及解析
-
今年国庆“嫦娥二号”又成功发射,据科学家预测,月球的土壤中吸附着数百万吨的
He,每百吨
He核聚变所释放出的能量相当于目前人类一年消耗的能量。在地球上氦元素主要以
He的形式存在。下列说法正确的是( )
A、
He原子核内含有4个质子
B、
比
多一个电子
C、
He和
He互为同位素
D、
He的最外层电子数为2,具有较强的金属性
难度: 简单查看答案及解析
-
在未知溶液中加入AgNO3溶液有白色沉淀生成,加入稀硝酸后,沉淀部分溶解,有无色无味气体放出,将气体通入澄清石灰水变浑浊。则水溶液中含有( )
A、Cl— SO42— B、Cl— NO3—
C、Cl— CO32— D、Cl— OH—
难度: 简单查看答案及解析
-
只用一种试剂(必要时可以加热)能把Na2SO4、NH4NO3、NaCl、(NH4)2SO4四瓶无色溶液加以区别的是( )
A.、BaCl2 B、 Ba(OH)2 C、NaOH D、AgNO3
难度: 简单查看答案及解析
-
下列各组仪器:①漏斗;②容量瓶;③分液漏斗;④天平;⑤量筒;⑥胶头滴管;⑦蒸馏烧瓶。常用于物质分离的是 ( )
A、① ③ ⑦ B、② ⑥ ⑦
C、① ④ ⑦ D、④ ⑤ ⑥
难度: 简单查看答案及解析
-
实验室使用的浓盐酸的溶质质量分数为36.5%,密度为1.19g·cm3,则物质的量浓度是( )
A、11.9 B、11.9 mol ·L-1 C、0.012 mol ·L-1 D、无法计算
难度: 简单查看答案及解析
-
现有三组:①CCl4和氯化钠溶液;②硝酸钾溶液中少量氯化钠;③氯化钠溶液和碘的水溶液,分离以上各混合液的正确方法依次是( )
A、分液、过滤、蒸馏 B、过滤、结晶、分液
C、蒸馏、分液、萃取 D、分液、结晶、萃取
难度: 简单查看答案及解析
-
从2 mol ·L-1的氯化铜溶液中取出含Cl—为3.55g的溶液,所取溶液的体积是( )
A、50mL B、25mL C、12.5mL D、0.025mL
难度: 简单查看答案及解析
-
已知某溶液中c(Na+)= 0.2mol / L,c(Mg2+)= 0.25mol / L,c(Cl—)=0.4mol / L,如果溶液中还有SO42—,那么c(SO42—)应为( )
A 、0.1mol / L B、0.3mol / L C、0.15mol / L D、0.5mol / L
难度: 简单查看答案及解析