-
化学与生活密切相关,下列说法不正确的是
A.为了防止食品受潮变质,常在食品包装袋中放入生石灰
B.不可用铝制餐具长时间存放酸性或碱性食物
C.光化学烟雾与氮氧化合物和碳氢化合物的大量排放有关
D.为防止铁制品生锈,可在铁制品的外层涂油漆或局部镀铜
难度: 中等查看答案及解析
-
对于相同状况下的12C18O和14N2两种气体,下列说法正确的是
A.若质量相等,则质子数相等 B.若分子数相等,则体积相等
C.若原子数相等,则中子数相等 D.若体积相等,则密度相等
难度: 中等查看答案及解析
-
在一定条件下,Na2CO3溶液存在CO32—+ H2O
HCO3—+OH—平衡。下列说法不正确的是
A.稀释溶液,
增大 B.通入CO2,溶液PH减小
C.升高温度,此平衡常数增大 D.加入NaOH固体,
减小
难度: 中等查看答案及解析
-
用NA表示阿伏加德罗常数的值,下列说法正确的是
A.标准状况下,5.6L NO和5.6L O2混合后的分子总数为0.5NA
B.1mol Na2O2固体中含离子总数为4NA
C.7.1gCl2与足量NaOH溶液反应转移的电子数为0.2NA
D.在标准状况下,22.4LCH4与18gH2O所含有的电子数均为10NA
难度: 困难查看答案及解析
-
下列离子方程式的书写不正确的是
A.氢氧化钡溶液与稀硫酸反应:Ba2++SO42—+H++OH—=BaSO4↓+H2O
B.Ca(ClO)2溶液中通入过量CO2:ClO—+H2O+CO2=HCO3—+HClO
C.铜溶于稀硝酸:3Cu+8H++2NO3—=3Cu2++2NO↑+4H2O
D.将AlCl3溶液滴入氨水中:3NH3·H2O+Al3+=Al(OH)3↓+3NH4+
难度: 简单查看答案及解析
-
在下列溶液中一定能大量共存的离子组是
A.pH=2的溶液:Fe2+、NH4+、Cl—、NO3—
B.能使pH试纸变深蓝色的溶液:Na+、
、S2—、CO32—
C.含有大量Fe3+的溶液:SCN—、I—、K+、Br—
D.澄清透明的无色溶液:ClO—、MnO4—、Al3+、SO42—
难度: 简单查看答案及解析
-
短周期元素X、Y、Z在元素周期表中的位置如右下图所示,下列说法正确的是 ( )
A.X、Y、Z三种元素中,X的非金属性最强
B.常压下X的单质的熔点比Z的低
C.Y的最高正化合价为+7
D.Y的氢化物的稳定性比Z的弱
难度: 中等查看答案及解析
-
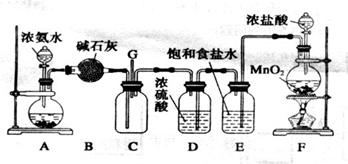
下列实验装置、选用的试剂或实验操作中,都正确的是

A.实验室用装置A制取氨气 B.用B装置吸收氨气,并防止倒吸
C.用C装置稀释浓硫酸 D.用D装置除去CO2中的HCl
难度: 中等查看答案及解析
-
为测某镁铝合金样品中铝的含量,进行下列实验:取一定量合金,加入100mL0.3mol·L—1稀硫酸,合金完全溶解,产生的气体在标准状况下体积为560mL;再加0.2mol·L—1NaOH溶液至沉淀质量恰好在此时不再变化,用去350mL NaOH溶液。则所取样品中铝的物质的量为
A.0.005mol B.0.01mol C.0.025mol D.0.03mol
难度: 中等查看答案及解析
-
某学生做如下实验:第一步,在淀粉KI溶液中,滴入少量NaClO溶液,并加入少量稀硫酸,溶液立即变蓝;第二步,在上述蓝色溶液中,滴加足量的Na2SO3溶液,蓝色逐渐消失。下列叙述中对实验原理的解释和结论不正确的是
A.氧化性:HClO>I2>SO42—
B.淀粉KI溶液变蓝是因为I—被氧化为I2,淀粉遇I2变蓝
C.蓝色消失的原因是Na2SO3溶液具有漂白性
D.若将Na2SO3溶液加入氯水中,氯水退色
难度: 困难查看答案及解析
-
X、Y、Z、W均为中学化学的常见物质,一定条件下它们之间有如图转化关系(其它产物已略去),下列说法不正确的是
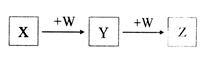
A.若W是单质铁,则Z溶液可能是FeCl2溶液
B.若W是氢氧化钠,则X与Z可反应生成Y
C.若X是碳酸钠,则W可能是盐酸
D.若W为氧气,则Z与水作用(或溶于水)一定生成一种强酸
难度: 困难查看答案及解析
-
pH=3的H2SO4溶液和pH=10的NaOH溶液混合,要使混合液的pH=7,则硫酸和氢氧化钠溶液的体积比应为( )
A.1:10 B.1:9 C.1:20 D.1:2
难度: 中等查看答案及解析
-
可逆反应A(s)+B(g)
(n为正整数)在不同条件下反应混合物中C的百分含量和反应过程所需时间的关系曲线如右图所示。下列有关叙述中一定正确的是
A.其他条件相同,
表示使用了催化剂,
没有使用催化剂
B.其他条件相同,若只改变压强,则
比
的压强大且
C.其他条件相同,若只改变温度,则
比
的温度高且Q>0
D.其他条件相同,若改变A的物质的量,则
比
消耗A的物质的量少
难度: 简单查看答案及解析
-
高功率Ni/MH(M表示储氢合金)电池已经用于混合动力汽车。总反应方程式如下:
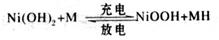
下列叙述不正确的是
A.该电池放电时的正极和充电时的阴极均发生还原反应
B.放电时负极反应为:MH+OH——e—=M+H2O
C.充电时阳极反应为:NiOOH+H2O+e—=Ni(OH)2+OH—
D.放电时每转移1mol电子,正极有1molNiOOH被还原
难度: 简单查看答案及解析
-
下列实验操作完全正确的是
编号 实验 操作
A 证明SO2有漂白性 将SO2气体通入紫色石蕊试液中,观察溶液是否退色
B 配制一定物质的量浓度的硫酸溶液1000mL 准确量取一定体积浓硫酸,放入到1000mL的容量瓶中,加水稀释,振荡摇匀定容
C 除去FeCl3溶液中混有的FeCl2 向溶液中通入过量氯水,然后加热煮沸就得到了纯净的FeCl3溶液
D 检验Br—的存在 在溶液中先加入氯水再加入CCl4,振荡、静置,观察下层溶液显橙红色
难度: 简单查看答案及解析
-
下列图示与对应的叙述相符的是

图1 图2 图3 图4
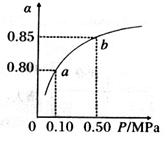
A.图1表示同温度下,pH=1的盐酸和醋酸溶液分别加水稀释时pH的变化曲线,其中曲线Ⅱ为盐酸,且b点溶液的导电性比a点强
B.图2表示0.1000 mol·L-1CH3COOH溶液滴定20.00mL0.1000 mol·L-1NaOH溶液所得到的滴定曲线
C.图3表示压强对可逆反应2A(g)+2B(g)
3C(g)+D(s)的影响,乙的压强比甲的压强大
D.据图4,若除去CuSO4溶液中的Fe3+可向溶液中加入适量CuO至pH在4左右
难度: 简单查看答案及解析