-
为了除去MgCl2洛液中的FeCl3,可在加热搅拌的条件下如入一种试剂,这种试剂是
A.NaOH B.氨水 C.Na2CO3 D.MgO
难度: 中等查看答案及解析
-
高氯酸、硫酸、硝酸和盐酸都是强酸,其酸性在水溶液中差别不大.以下是某温度下这四种酸在冰醋酸中的电离常数:
酸
HClO4
H2SO4
HCl
HNO3
Ka
1.6×10-5
6.3×10-9
1.6×10-9
4.2×10-10
从以上表格中判断以下说明不正确的是
A.在冰醋酸中硫酸的电离方程式为H2SO4═2H++SO42-
B.在冰醋酸中高氯酸是这四种酸中最强的酸
C.在冰醋酸中这四种酸没有完全电离
D.水对于这四种酸的强弱没有区分能力,但醋酸可以区分这四种酸的强弱
难度: 困难查看答案及解析
-
已知25℃时,电离常数Ka(HF)=3.6×10-4,溶度积常数Ksp(CaF2)=1.46×10-10。现向1L0 mol·L-1HF溶液中加入1L0.2 mol·L-1CaCl2溶液,则下列说法中,正确的是
A.25℃时,0.1 mol·L-1HF溶液中pH=1
B.Ksp(CaF2)随温度和浓度的变化而变化
C.加入CaCl2溶液后体系中的c(H+)浓度不变
D.该体系中有CaF2沉淀产生
难度: 困难查看答案及解析
-
一定条件下,恒容的密闭容器中,加入一定量的A与B发生反应:A(s)+2B(g)
C(g)+2D(g) ΔH<0,平衡时C的物质的量与加入B的物质的量的变化关系如图所示。下列说法正确的是

A.增加A的物质的量,正反应速率加快
B.平衡时,其他条件不变,当温度升高时,θ变大
C.图中曲线的斜率表示反应的化学平衡常数
D.平衡时,其他条件不变,再通人B,则反应混合物的温度升高
难度: 中等查看答案及解析
-
下列有关AgCl沉淀的溶解平衡的说法中,不正确的是
A.AgCl沉淀生成和溶解不断进行,但速率相等
B.AgCl难溶于水 ,溶液中没有Ag+和Cl-
C.升高温度,AgCl沉淀的溶解度增大
D.向AgCl沉淀中加入NaCl固体,AgCl沉淀的溶解度降低
难度: 中等查看答案及解析
-
若在1L蒸馏水中加入1滴(约0.05mol)0.1 mol·L-1mol﹒L-1的NaCl溶液,搅拌均匀后再滴入1滴0.1 mol·L-1AgNO3溶液,请估算是否会产生沉淀(己知AgCl的KSP=1.8×10-10)
A.否 B.是 C.可能是 D.以上都不正确
难度: 中等查看答案及解析
-
某可逆反应平衡常数表达式为K=
达到平衡状态时,如果升高温度(其它条件不变),则c(NO)减小.下列说法正确的是
A.反应的热化学方程式为NO2(g)+SO2(g)
NO(g)(g)+SO3(g) △H>0
B.一定条件下达到平衡时,缩小容器体积,增大体系压强,气体颜色加深
C.混合气体的平均摩尔质量保持不变,说明反应已达平衡
D.使用合适的催化剂可使该反应的反应速率和平衡常数增大
难度: 中等查看答案及解析
-
下列叙述与图像对应符合的是
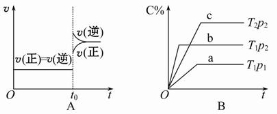
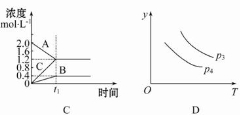
A.对于达到平衡状态的N2(g)+3H2(g)
2NH3(g)在t0时刻充入了一定量的NH3,平衡逆向移动
B.p2>p1,T1>T2
C.该图像表示的化学方程式为:2A=B+3C
D.对于反应2X(g)+3Y(g)
2Z(g) ΔH<0,y可以表示Y的百分含量
难度: 困难查看答案及解析
-
相同温度下,在体积相等的三个恒容密闭容器中发生可逆反应:N2(g)+3H2(g)
2NH3(g) △H=-92.4kJ/mol。 实验测得起始、平衡时的有关数据如下表
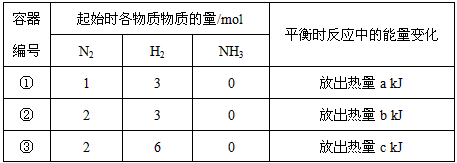
下列叙述正确的是
A.放出热量关系:a<b<92.4
B.起始时反应速率:③>②>①
C.达平衡时氨气的体积分数:①>③
D.N2的转化率:②>①>③
难度: 困难查看答案及解析
-
下列叙述正确的是
A.盐酸中滴加氨水至中性,溶液中溶质为氯化铵
B.稀醋酸加水稀释,醋酸电离程度增大,溶液的pH减小6 e; U5 G" b0 F5 ]
C.饱和石灰水中加入少量CaO,恢复至室温后溶液的pH值不变5 I0 d7 L- b% ?5 \3 L/ I8 ]8 U
D.沸水中滴加适量饱和FeCl3溶液,形成带电的胶体,导电能力增强
难度: 中等查看答案及解析
-
常温下a mol·L-1 CH3COOH稀溶液和b mol·L-1KOH稀溶液等体积混合,下列判断一定错误的是
A.若c(OH-)>c(H+),a=b B.若c(K+)>c(CH3COO-),a>b
C.若c(OH-)=c(H+),a>b D.若c(K+)<c(CH3COO-),a<b
难度: 中等查看答案及解析
-
常温下,取0.1 mol·L-1HY溶液与0.1 mol·L-1NaOH溶液等体积混合(忽略混合后溶液体积的变化),测得混合溶液的pH=9,则下列说法不正确的是
A.c(Na+)═c(Y-)+c(HY) B.c(OH-)═c9H+)+c(HY)
C.c(Y-)>c(Na+)>c(OH-)>c(H+) D.c(Na+)+c(H+)═c(OH-)+c(Y-)
难度: 中等查看答案及解析
-
下列电解质溶液的有关叙述正确的是
A.同浓度、同体积的强酸与强碱溶液混合后,溶液的pH=7+ G4 D* e% P% b
B.在含有BaSO4沉淀的溶液中加入Na2SO4固体,c(Ba2+)增大
C.含1 mol KOH的溶液与1 mol CO2完全反应后,溶液中c(K+)= c(HCO3-)
D.在CH3COONa溶液中加入适量CH3COOH,可使c(Na+)=c(CH3COO-)
难度: 中等查看答案及解析
-
常温下,向0.1 mol·L-1的硫酸溶液中逐渐加入物质的量浓度相同的的氢氧化钡溶液,生成沉淀的量与加入氢氧化钡溶液的体积关系如图所示,a、b、c、d分别表示实验时不同阶段的溶液,下列有关说法中不正确的是
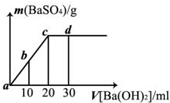
A.溶液的pH:a<b<c<d B.溶液的导电能力:a>b>d>c
C.a、b溶液呈酸性 D.c、d溶液呈碱性
难度: 困难查看答案及解析
-
室温时,M(OH)2(S)
M2+(aq)+2OH-(aq) Ksp=a,c(M2+)=b mol·L-1时,溶液的pH等于
A.
lg
B.
lg
C.14+
lg
D.14+
lg
难度: 中等查看答案及解析
-
已知室温下,Al(OH)3的Ksp或溶解度远大于Fe(OH)3。向浓度均为0.1 mol·L-1的Fe(NO3)3和Al(NO3)3混合溶液中,逐滴加入NaOH溶液。下列示意图表示生成Al(OH)3的物质的量与加入NaOH溶液的体积关系,合理的是
难度: 困难查看答案及解析
-
金属离子和硫离子在水溶液中的反应比较复杂,其产物和离子的水解、金属硫化物的的溶解度、离子氧化性或还原性等因素有关.资料表明,CuS的溶解度很小,在稀酸溶液中也不溶解;Ag2S的溶解度更小,但却溶于稀酸.下列有关说法正确的是( )
A.Cu2+和S2-在水溶液中反应的产物是CuS
B.Al3+和S2-在水溶液中发生相互促进水解,所以不存在Al2S3的水溶液
C.Fe3+和S2-在酸性溶液中反应的产物只可能是Fe2+和H2S
D.在酸性溶液中,将S2-加入Ag+和Cu2+的混合液中Ag2S先沉淀
难度: 困难查看答案及解析
-
常温下,一定浓度的某溶液,由水电离的出的c(OH-)=1×10-4 mol/L,则该溶液中的溶质可能是
A.H2SO4 B.NaOH C.KHSO4 D.CH3COONa
难度: 中等查看答案及解析
-
有关①100mL 0.1mol/LNaHCO3、②100mL 0.1mol/LNa2CO3两种溶液的叙述不正确的是
A.溶液中水电离出的H+个数:②>①
B.溶液中阴离子的物质的量浓度之和:②>①
C.①溶液中:c(CO32-)>c(H2CO3)
D.②溶液中:c(HCO3-)>c(H2CO3)
难度: 中等查看答案及解析
-
下列有关问题,与盐的水解有关的是
①NH4Cl与ZnCl2溶液可作焊接金属中的除锈剂
②用NaHCO3与Al2(SO4)3两种溶液可作泡沫灭火剂
③草木灰与铵态氮肥不能混合施用
④实验室盛放碳酸钠溶液的试剂瓶不能用磨口玻璃塞
⑤加热蒸干AlCl3溶液得到Al(OH)3固体
A.①②③ B.②③④ C.①④⑤ D.①②③④⑤
难度: 中等查看答案及解析
-
下列固体物质溶液水,再将其溶液加热,蒸发结晶、再灼烧,能得到化学组成与原固体物质相同的是①胆矾 ②氯化铝 ③硫酸铝 ④NaHCO3 ⑤氯化铜
A.③④ B.①③④ C.①②③④ D.全部
难度: 中等查看答案及解析
-
已知Zn(OH)2的溶度积常数为1.2×10-17(mol·L-1)3,则Zn(OH)2在水中的溶解度为
A.1.4×10-6 mol·L-1 B.2.3×10-6 mol·L-1
C.1.4×10-9 mol·L-1 D.2.3×10-9 mol·L-1
难度: 中等查看答案及解析
-
某温下,在BaSO4饱和溶液中加入少量BaCl2溶液,产生BaSO4沉淀,若以Ksp表示BaSO4的溶度积,则平衡后溶液中
A.C(Ba2+)·C(SO42-)≠Ksp;C(Ba2+)<C(SO42-)
B.C(Ba2+)·C(SO42-)>Ksp;C(Ba2+)=C(SO42-)
C.C(Ba2+)=C(SO42-)=Ksp1/2
D.C(Ba2+)·C(SO42-)=Ksp;C(Ba2+)>C(SO42-)
难度: 中等查看答案及解析
-
自然界地表层原生铜的硫化物经氧化、淋滤作用后变成CuSO4溶液,向地下深层渗透,遇到难溶的ZnS或PbS,慢慢转变为铜蓝(CuS)。下列分析一定正确的是
A.KSP(PbS)<Kap(CuS)
B.原生铜的硫化物具有还原性,而铜蓝没有还原性
C.CuSO4与ZnS反应的离子方程式是Cu2++S2-═CuS↓
D.整个过程涉及的反应类型有氧化还原反应和复分解反应
难度: 中等查看答案及解析
-
现有温度相同、pH=a和pH=b的两种NaOH溶液,已知b=a+2,将两种溶液等体积混合后,所得溶液的pH接近于
A.a-lg2 B.b-lg2 C.a+lg2 D.b+lg2
难度: 中等查看答案及解析
-
下列溶液中微粒浓度关系一定正确的是
A.氨水和氯化铵的pH=7的混合溶液中:c(Cl-)=c(NH4+)
B.pH=1的一元酸和pH=13的一元碱等体积混合:c(OH-)=c(H+)
C.0.1mol·L-1的硫酸铵溶液中:c(NH4+)>c(SO42-)>c(H+)>c(OH-)
D.0.1mol·L-1的硫化钠溶液中:c(OH-)=c(H+)+c(HS-)+c(H2S)
难度: 中等查看答案及解析
-
在t℃时,AgBr在水中的沉淀溶解平衡曲线如图所示.又知t℃时AgCl的Ksp=4×10-10,下列说法不正确的是
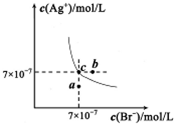
A.在t℃时,AgBr的Ksp为4.9×l0-13
B.在AgBr饱和溶液中加入NaBr固体,可使溶液由c点到b点
C.图中a点对应的是AgBr的不饱和溶液
D.在t℃时,AgCl(s)+Br-(aq)
AgBr(s)+Cl-(aq)平衡常数K≈816
难度: 困难查看答案及解析