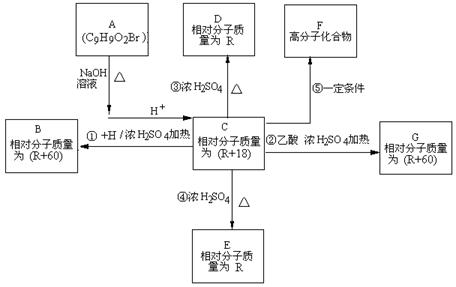
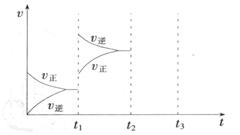
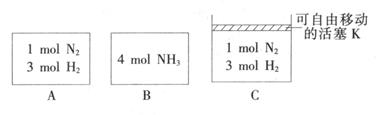
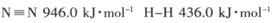-
若室温时,将pH=a的氨水与pH=b的盐酸等体积混合,恰好完全反应,则该氨水的电离度为( )
A.10a+b-12 % B.10a+b-14 % C.1012-a-b % D.1014-a-b %
难度: 简单查看答案及解析
-
向100 mL 0.1 mol·L-1硫酸铝铵[NH4Al(SO4)2]溶液中逐滴滴入0.1 mol·L-1 Ba(OH)2溶液。随着 Ba(OH)2溶液体积V的变化,沉淀总物质的量n的变化如图所示。则下列说法中正确的是( )
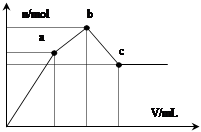
A.a点发生反应的离子方程式是:
Al3++2SO42-+2Ba2++3OH— = Al(OH)3↓+2BaSO4↓
B.b点消耗Ba(OH)2溶液体积为200mL
C.从a→b 、b→c点过程中发生反应的离子方程式依次为:NH4++OH-=NH3·H2O Al(OH)3+OH-=AlO2-+2H2O
D.沉淀的质量:a点>c点
难度: 简单查看答案及解析
-
①14Cu2++5FeS2+12H2O = 7Cu2S + 5Fe2+ + 24H++3SO42-
②Mn2+ + S2O82- + H2O— MnO4- + SO42-+ H+ 对上述两个反应判断正确的是( )
A.①②反应中SO42—都是氧化产物 B.两个反应中电子转移数目都是10mol
C.①反应中的硫元素既被氧化又被还原 D.氧化性:S2O82—>MnO4—
难度: 简单查看答案及解析
-
若pH=3的酸溶液和pH=11的碱溶液等体积混合后溶液呈酸性,其原因可能是( )
A.弱酸溶液和强碱溶液反应 B.生成了一种强酸弱碱盐
C.强酸溶液和弱碱溶液反应 D.一元强酸溶液和一元强碱溶液反应
难度: 简单查看答案及解析
-
下列说法中不正确的是( )
A.若XY3分子中X原子处于正三角形的中心,则XY3分子为非极性分子
B.C2H5OH与C2H5Br相比,前者的沸点远高于后者,其原因是前者的分子间存在氢键
C.同周期ⅠA族元素和 ⅦA族元素之间只能形成离子化合物
D.由两种非金属元素组成的化合物分子中只可能有极性键,不会有非极性键
难度: 简单查看答案及解析
-
硫代硫酸钠溶液与稀硫酸反应的化学方程式为:Na2S2O3+H2SO4===Na2SO4+SO2+S↓+H2O,
下列各组实验中最先出现浑浊的是( )
实验 反应温度/℃ Na2S2O3溶液 稀H2SO4 H2O
V/mL c/(mol·L-1) V/mL c/(mol·L-1) V/mL
A 25 5 0.1 10 0.1 5
B 25 5 0.2 5 0.2 10
C 35 5 0.1 10 0.1 5
D 35 5 0.2 5 0.2 10
难度: 简单查看答案及解析
-
硫酸锶(SrSO4)在水中的沉淀溶解平衡曲线如下。下列说法正确的是 ( )
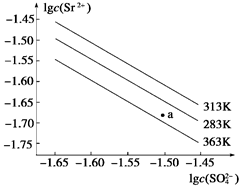
A.温度一定时,Ksp(SrSO4)随c(SO42- )的增大而减小
B.三个不同温度中,313 K时Ksp(SrSO4)最大
C.283 K时,图中a点对应的溶液是饱和溶液
D.283 K下的SrSO4饱和溶液升温到363 K后变为不饱和溶液
难度: 简单查看答案及解析
-
短周期元素X、Y、Z、R、W五种元素原子序数依次增大,其中X与Z、Y与W分别为同族元素。原子半径X<Y< W< R<Z,W原子的最外层电子数比内层电子总数少4,Z、R的核外电子数之和与Y、W核外电子数之和相等。下列说法不正确的是( )
A.Y、Z、R的简单离子具有相同的电子层结构
B.X2Y分子间存在氢键,故X2Y比X2W稳定
C.X、Z分别与Y均可形成A2B与A2B2型化合物,且A2B2均有较强的氧化性
D.由X、Y、Z形成的化合物能与X、Y、R形成的化合物发生反应
难度: 简单查看答案及解析
-
某同学按图所示的装置进行电解实验。下列说法错误的是( )
A.电解初期,石墨电极上有H2产生
B.整个电解过程中,H+的浓度不断增大
C.电解一定时间后,石墨电极上有铜析出
D.电解初期,总反应方程式为:Cu+H2SO4
CuSO4+H2↑
难度: 简单查看答案及解析
-
中学常见物质A、B、C、D、E、X,存在下图转化关系 (部分生成物和反应条件略去)。下列推断不正确的是( )

A.若D是一种强碱,则A、B、C均可与X反应生成D
B.若D为NaCl,且A可与C反应生成B,则E可能是CO2
C.若D是一种白色沉淀,在空气中最终变为红褐色,则A可能是铁
D.若D是一种强酸,则A既可以是单质,也可以是化合物,且D可与铜反应生成B或C
难度: 简单查看答案及解析
-
下列化学用语或图示表达正确的是( )
A.CO2的电子式
B.Na+的结构示意图
C.葡萄糖的实验式C6H12O6 D.乙烯的比例模型
难度: 简单查看答案及解析
-
下列物质与其用途完全符合的有( )条
①Na2CO3—制玻璃;②SiO2—太阳能电池;③AgI—人工降雨;④NaCl—制纯碱;
⑤Al2O3—焊接钢轨;⑥NaClO—消毒剂⑦Fe2O3—红色油漆或涂料 ⑧MgO—耐火材料
A.4 B.5 C.6 D.7
难度: 简单查看答案及解析
-
下表中所示物质或概念间的从属关系符合右图的是( )
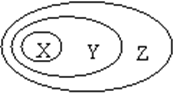
X Y Z
A 钠元素 主族元素 短周期元素
B 电解质 化合物 纯净物
C 氢氧化铁 胶体 分散系
D 置换反应 氧化还原反应 放热反应
难度: 简单查看答案及解析
-
NA为阿伏加德罗常数的数值,下列说法中正确的是( )
A.在密闭容器中加入l.5mol H2和0.5molN2,充分反应后得到NH3分子数为NA
B.一定条件下,2.3g的Na完全与O2反应生成3.6g产物时失去的电子数为0.1NA
C.1.0L的0.1 mol·L-1Na2S溶液中含有的S2-离子数为0.1NA
D.标准状况下,22.4L的CHCl3中含有的分子数为NA
难度: 简单查看答案及解析
-
常温下,下列各组离子在指定溶液中一定能大量共存的是( )
A.pH=1的溶液中: Fe2+、NO3-、SO42-、Na+
B.由水电离的c(H+)=1×10-14 mol·L-1的溶液中:Ca2+、K+、Cl-、HCO3-
C.c(H+)/c(OH-)=1012的溶液中: NH4+、Al3+、NO3-、Cl-
D.c(Fe3+)="0.1" mol·L-1的溶液中: K+、ClO-、SO42-、SCN-
难度: 简单查看答案及解析
-
两种有机物以一定比例混合,一定条件下在a LO2(足量)中充分燃烧恢复到原状态,再通过足量的过氧化钠,得到气体仍是 a L,下列组合中符合此条件的是( )
A.CH4、C2H4 B.CH3CH2OH 、CH3COOH
C.C2H6、HCHO D.HCOOH、CH3COOCH3
难度: 简单查看答案及解析
-
将11.9 g由Mg、Al、Fe组成的合金溶于足量的NaOH溶液中,合金质量减少了2.7 g。另取等质量的合金溶于过量稀硝酸中,生成了6.72 L NO(标准状况下),向反应后的溶液中加入适量NaOH溶液恰好使Mg2+、Al3+、Fe3+完全转化为沉淀,则沉淀的质量为( )
A.22.1 g B.27.2 g C.30 g D.无法计算
难度: 简单查看答案及解析
-
下列实验操作中一定会造成实验值偏小的是( )
A.将pH试纸用蒸馏水湿润后测某溶液的pH
B.配制500mL 0.10mol/L NaCl溶液,定容时俯视
C.以标准盐酸溶液滴定未知浓度的NaOH溶液时,酸式滴定管未用标准溶液润洗
D.用标准NaOH溶液滴定未知浓度的盐酸溶液,开始时滴定管尖嘴处没有气泡,结束时有气泡
难度: 简单查看答案及解析
-
I2在KI溶液中存在下列平衡:I2(aq)+I-(aq)
I3-(aq), 某I2、KI混合溶液中,I3-的物质的量浓度c(I3-)与温度T的关系如图所示(曲线上任何一点都表示平衡状态)。下列说法正确的是( )
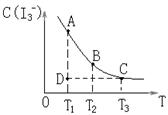
A.反应 I2(aq)+I-(aq)
I3-(aq)的 △H>0
B.若温度为T1、T2时,反应平衡常数分别为K1、K2,则K2>K1
C.若反应进行到状态D时,一定有v正>v逆
D.状态A与状态B相比,状态A的c(I2)大
难度: 简单查看答案及解析
-
下列离子方程式与所述事实相符且正确的是( )
A.磁性氧化铁溶于稀硝酸:Fe3O4+8H++NO3-=3Fe3++NO↑+4H2O
B.Ca(HCO3)2溶液中加入少量NaOH溶液:
Ca2++2HCO3-+2OH-=CaCO3↓+CO32-+H2O
C.明矾溶液中加入Ba(OH)2溶液至生成的沉淀物质的量最多:
Al3++2SO42-+2Ba2++4OH-=AlO2-+2BaSO4↓+2H2O
D.向含有0.4 mol FeBr2的溶液中通入0.3 mol Cl2充分反应:
4Fe2++2Br-+3Cl2=4Fe3++6Cl-+Br2
难度: 简单查看答案及解析
-
下列说法正确的是( )
A.已知:H2(g)+
O2(g)===H2O(l);ΔH=-285.8 kJ·mol-1 ,则H2的燃烧热为-285.8 kJ·mol-1
B.已知:S(g)+O2(g)===SO2(g) ΔH1=-Q1 ;S(s)+O2(g)===SO2(g) ΔH2=-Q2,则Q1<Q2
C.已知:
H2SO4(浓)+NaOH(aq)="=="
Na2SO4(aq)+H2O(l) ΔH1;
CH3COOH(aq)+NH3·H2O(aq)===CH3COONH4(aq)+H2O(l) ΔH2,则有|ΔH1|<|ΔH2|
D.已知:Fe2O3(s)+3C(石墨)===2Fe(s)+3CO(g)ΔH=+489.0 kJ·mol-1
CO(g)+
O2(g)===CO2(g) ΔH=-283.0 kJ·mol-1
C(石墨)+O2(g)===CO2(g) ΔH=-393.5 kJ·mol-1
则4Fe(s)+3O2(g)===2Fe2O3(s) ΔH=-1641.0 kJ·mol-1
难度: 简单查看答案及解析
-
有关下图所示化合物的说法不正确的是( )
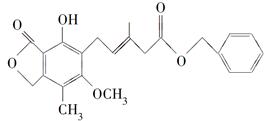
A.既可以与Br2的CCl4溶液发生加成反应,又可以在光照下与Br2发生取代反应
B.1 mol该化合物最多可以与3 mol NaOH反应
C.既可以催化加氢,又可以使酸性KMnO4溶液褪色
D.既可以与FeCl3溶液发生显色反应,又可以与NaHCO3溶液反应放出CO2气体
难度: 简单查看答案及解析
-
下列说法中,正确的一组是( )
①1H、2H、3H是氢元素的三种核素,互称为同位素
②饮用水可以用明矾、漂白粉来净化,两者的作用原理相同
③化合反应不一定是氧化还原反应
④有些吸热反应,不需要加热也能进行
⑤NH4Cl、 MgCl2均为离子化合物,均含有离子键和共价键
⑥除去水垢中的CaSO4,可以先用饱和的碳酸钠溶液浸泡,再加酸处理
A.①④⑤ B.②⑤⑥ C.①②③④ D.①③④⑥
难度: 简单查看答案及解析