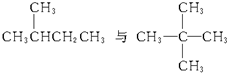-
运用元素周期律分析下面的推断,其中错误的是( )
A.砹(At)为有色固体,HAt不稳定
B.铊(T1)是铝的同族元素,原子核外有6个电子层,推测T1(OH)3是两性氢氧化物
C.已知锶Sr与镁同族且原子半径大于钙,硫酸锶(SrSO4)是难溶于水的白色固体
D.硒化氢(H2Se)比硫化氢稳定性差难度: 中等查看答案及解析
-
在周期表主族元素中,甲元素与乙、丙、丁三元素相邻,甲、乙的原子序数之和等于丙的原子序数;这四种元素原子的最外层电子数之和为20.下列判断中,正确的是( )
A.原子半径:丙>乙>甲>丁
B.气态氢化物的稳定性:甲>丙
C.最高价氧化物对应水化物的酸性:丁>甲
D.乙和甲或乙和丁所能形成的化合物都是有毒物质难度: 中等查看答案及解析
-
2760Co是γ射线放射源,可用于农作物诱变育种,我国用该方法培育出了许多农作物新品种,下列叙述正确的是( )
A.60是Co元素的相对原子质量
B.由Co的不同种同位素组成的单质,其化学性质与物理性质均不同
C.60是2760Co这种核素的质量数
D.2760Co原子中,中子数是27,电子数是33难度: 中等查看答案及解析
-
有机化学知识在生活中应用广泛,下列说法错误的是( )
A.利用天然气做燃料可以有效地减少“温室效应”的气体产生
B.由于乙醇能够溶解很多有机物和无机物,所以可用乙醇提取中药的有效成分
C.可以用浸泡过高锰酸钾溶液的硅土来吸收水果或花朵产生的乙烯,达到保鲜目的
D.从石油中可以获得乙烯,乙烯是一种重要的基本化工原料难度: 中等查看答案及解析
-
有关化学用语正确的是( )
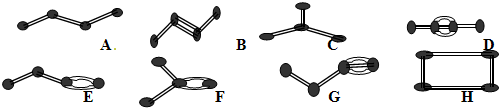
①羟基的电子式②乙烯的结构简式:CH2CH2]③硫化氢的电子式
④丙烷分子的球棍模型: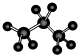 ⑤苯分子的比例模型
⑤苯分子的比例模型  ⑥甲烷的结构式
⑥甲烷的结构式
A.①④
B.②③④
C.④⑤⑥
D.②③⑤难度: 中等查看答案及解析
-
下列有关物质结构和元素周期律的表述正确的是( )
A.ⅦA族元素是同周期中非金属性最强的元素
B.第二周期ⅣA族元素的原子核电荷数和中子数分别为6
C.主族元素的最高正价均等于其族序数
D.非金属元素的气态氢化物溶于水后,水溶液均为酸性难度: 中等查看答案及解析
-
常温常压下,取下列四种有机物各1mol,分别在足量的氧气中燃烧,消耗氧气最多的是( )
A.C2H5OH
B.CH4
C.C3H8O2
D.C2H4O难度: 中等查看答案及解析
-
标准状况下,0.56L CH4和C2H4的混合气体通入足量溴水中,溴水增重0.28g(假设C2H4完全被吸收),则乙烯占混合气体体积的( )
A.20%
B.40%
C.60%
D.80%难度: 中等查看答案及解析
-
下列说法中正确的是( )
A.石油裂解可以得到氯乙烯
B.油脂水解可得到氨基酸和甘油
C.所有烷烃和蛋白质中都存在碳碳单键
D.淀粉和纤维素的组成都是(C6H10O5)n,水解最终产物都是葡萄糖难度: 中等查看答案及解析
-
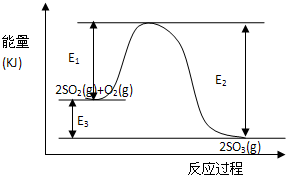
已知可逆反应2SO2+O2
2SO3,当生成2mol SO3时放出热量为Q,现将1mol SO2和0.5mol O2在相同条件下反应生成SO3放出的热量为Q1,则( )
A.Q1=Q
B.Q1<Q
C.2Q1>Q
D.无法判断难度: 中等查看答案及解析
-
下列各组混合物,能用分液漏斗分开的是( )
①四氯化碳和水 ②苯和溴苯 ③乙醇和水 ④苯和水 ⑤硝基苯和水 ⑥苯和四氯化碳.
A.①②③
B.②④⑥
C.①④⑤
D.④⑤⑥难度: 中等查看答案及解析
-
短周期金属元素甲~戊在元素周期表中的相对位置如右表所示.下列判断正确的是( )
A.原子半径:丙<丁<戊
B.氢氧化物碱性:丙>丁>戊
C.金属性:甲>丙
D.最外层电子数:甲>乙难度: 中等查看答案及解析
-
右图为短周期的一部分,推断关于Y、Z、M的说法正确的是( )
X Y Z M
A.非金属性:Y>Z>M
B.ZM2分子各原子最外层均满足8e-稳定结构
C.原子半径:M>Z>Y
D.Y离子的结构示意图可表示为:难度: 中等查看答案及解析
-
主族元素X、Y、Z的离子为aX+、bY2-、cZ-,半径大小关系是aX+<cZ-<bY2-下列说法错误的是( )
A.b一定小于c
B.单质的还原性X>Z
C.Y2-的还原性大于Z¯
D.X可位于Y的上一周期、下一周期或同周期难度: 中等查看答案及解析
-
乙烯和乙醇的混合气体VL,完全燃烧后生成CO2和H2O,消耗相同状态下的氧气3VL,则混合气体中乙烯和乙醇的体积比是( )
A.1:1
B.2:1
C.1:2
D.任意比难度: 中等查看答案及解析
-
利用下列反应制备括号中的物质,不合理的是( )
A.乙烯与氯气加成(1,2-二氯乙烷)
B.乙烯与水加成(乙醇)
C.等物质的量的氯气与乙烷在光照条件下反应(氯乙烷)
D.氯气与苯用氯化铁做催化剂反应(氯苯)难度: 中等查看答案及解析
-
某化合物的分式为C5H11Cl,分析数据表明:分子中有两个-CH3、两个-CH2-、一个-CH-和一个-Cl,则它的可能结构有几种( )
A.2种
B.3种
C.4种
D.5种难度: 中等查看答案及解析
-
某烃的结构简式为
,它可能具有的性质是( )
A.它能使溴水褪色,但不能使酸性高锰酸钾溶液褪色
B.它既不能使溴水褪色,也不能使酸性高锰酸钾溶液褪色
C.易溶于水,也易溶于有机溶剂
D.能发生加成反应,一定条件下1mol该有机物最多可与4mol氢气加成难度: 中等查看答案及解析