-
下列说法正确的是
A.食盐、稀醋酸和蔗糖都是电解质
B.甲烷和乙烯均可使酸性KMnO4溶液褪色
C.纤维素、淀粉和蛋白质都是高分子化合物
D.乙酸乙酯和植物油均可水解生成乙醇
难度: 中等查看答案及解析
-
下列物质间关系判断正确的是
A.1H2、2H2 ——同位素
B.
、
——同素异形体
C.HCOOH、C15H31COOH ——同系物
D.HCOOCH3、CH3OCHO ——同分异构体
难度: 中等查看答案及解析
-
某有机物含有下列一种官能团,该有机物既能发生消去反应、氧化反应和酯化反应,又能跟某些活泼金属发生置换反应,该官能团最可能的是
A.—Cl B.—OH C.—COOH D.—CHO
难度: 中等查看答案及解析
-
下列分子式表示的物质一定是纯净物的是
A C5H10 B CH4O C C2H6 O D C2H4Cl2
难度: 中等查看答案及解析
-
下列各原子或离子的基态电子排列式错误的是
A.N3+ 1s22s22p6 B.F- 1s22s22p6
C.Fe2+ 1s22s22p63s23p63d6 D.O2- 1s22s22p6
难度: 中等查看答案及解析
-
某烷烃的结构简式为
 ,下列命名正确的是
,下列命名正确的是A.2,4 -二甲基 -3-乙基己烷 B.3-异丙基 -4-甲基已烷
C.2-甲基-3,4-二乙基戊烷 D.3-甲基-4-异丙基已烷
难度: 中等查看答案及解析
-
用乙炔为原料制取CH2Br—CHBrCl,可行的反应途径是
A.先加Cl2,再加HBr B.先加Cl2,再加Br2
C.先加HCl,再加HBr D.先加HCl,再加Br2
难度: 中等查看答案及解析
-
苹果酸的钠盐()可作为调味剂、缓冲剂、保水剂以及防腐保鲜剂,广泛应用于饮料、肉制品、口服液等。有关说法错误是
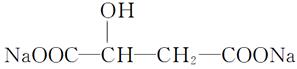
A.苹果酸的酸性强于醋酸
B.分别对苹果酸、苹果酸钠溶液微热,溶液的pH均增大
C.苹果酸在一定条件下发生消去反应可生成HOOCCH=== CHCOOH
D.苹果酸在一定条件下发生取代反应可生成
难度: 困难查看答案及解析
-
某饱和一元醇14.8 g和足量的金属Na反应,生成标准状况下氢气为2.24 L,该醇可氧化成醛,则其结构可能有几种
A.2种 B.3种 C.4种 D.5种
难度: 中等查看答案及解析
-
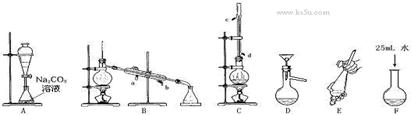
用下列装置进行相应实验,能达到实验目的的是

难度: 中等查看答案及解析
-
已知苯与一卤代烷在催化剂作用下可生成苯的同系物(x= Cl或 Br 或I)
在催化剂存在下,由苯和下列各组物质合成乙苯最好应选用的是
A.CH3CH3和I2 B.CH2=CH2和HCl
C.CH2=CH2和Cl2 D.CH3CH3和HCl
难度: 中等查看答案及解析
-
一氯代物的同分异构体有2种,二氯代物的同分异构体有4种的烷烃是
A.乙烷 B.丙烷 C.正丁烷 D.新戊烷
难度: 中等查看答案及解析
-
下列各组混合物中,不论二者以什么比例混合,只要总质量一定,完全燃烧时生成CO2的质量也一定,不符合上述要求的是
A.苯、甲苯 B.乙炔、苯乙烯 C.甲醛、甲酸甲酯 D.乙烯、环己烷
难度: 中等查看答案及解析
-
已知戊烷有3种同分异构体,戊醇的同分异构体(属醇类)的数目有
A.5 B.6 C.7 D.8
难度: 中等查看答案及解析
-
某温度下,1g某有机物在足量氧气中充分燃烧,其燃烧产物立即与过量的Na2O2充分反应,固体质量增加了2g。该有机物可能为
A.乙醛 B.甲酸甲酯 C.甲烷 D.苯
难度: 中等查看答案及解析