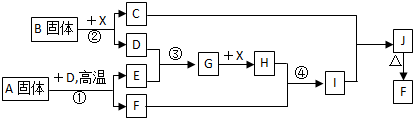
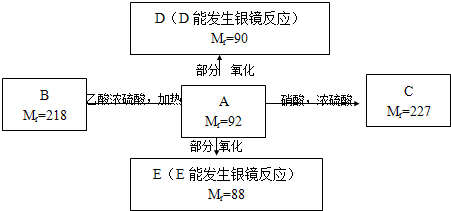
-
下列化学用语表达正确的是( )
A.丙烷的分子结构模型示意图:
B.Na2S的电子式:
C.丙烯的结构简式:CH3CH2CH2
D.氢硫酸的电离方程式:H2S+H2O=H3O++HS-难度: 中等查看答案及解析
-
下列说法正确的是( )
A.H与D,16O2与18O2互为同位素
B.H216O、D216O、H218O、D218O互为同素异形体
C.在NaCl晶体中,每个氯离子周围都有8个钠离子
D.L层电子为奇数的所有短周期元素所在族的序数与该元素原子的L层电子数相等难度: 中等查看答案及解析
-
下列现象或应用中,不涉及胶体性质的是( )
A.在饱和氯化铁溶液中逐滴加入NaOH溶液,产生红褐色沉淀
B.清晨,在茂密的树林中,常可以看到从枝叶间透过的光柱
C.用半透膜分离淀粉和食盐的混合液
D.肾功能衰竭等疾病引起的血液中毒,可用血液透析进行治疗难度: 中等查看答案及解析
-
某温度下,重水(D2O)的离子积常数为1.6×10-15若用定义pH一样来规定pD=-lg[D+],则在该温度下,下列叙述正确的是( )
A.纯净的重水中,pD=7
B.1 L溶解有0.01 mol DC1的重水溶液,其pD=2
C.1 L溶解有0.01 mol NaOD的重水溶液,其pD=12
D.纯净的重水中,[D+][OD-]>1.0×10-14难度: 中等查看答案及解析
-
化学家们合成了如下图所示的一系列的星烷,如三星烷、四星烷、五星烷等.下列说法正确的是( )
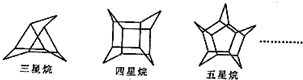
A.它们的一氯代物均只有三种
B.它们之间互为同系物
C.三星烷与乙苯互为同分异构体
D.六星烷的化学式为C18H24难度: 中等查看答案及解析
-
用如图表示的一些物质或概念间的从属关系中不正确的是( )
X Y Z 例 氧化物 化合物 纯净物 A 苯的同系物 芳香烃 芳香族化合物 B 胶体 分散系 混合物 C 电解质 离子化合物 化合物 D 碱性氧化物 金属氧化物 氧化物 
A.A
B.B
C.C
D.D难度: 中等查看答案及解析
-
以下实验装置一般不用于分离物质的是( )
A.
B.
C.
D.难度: 中等查看答案及解析
-
对于Al与重氢氧化钠(NaOD)的水溶液反应,下列说法正确的是( )
A.生成的氢气中只含有D2
B.生成的氢气中含有H2、HD、D2
C.生成的氢气中只含有H2
D.以上判断都不正确难度: 中等查看答案及解析
-
恒温下,容积均为2L的密闭容器M、N中,分别有以下列两种起始投料建立的可逆反应 3A(g)+2B(g)⇌2C(g)+xD(s) 的化学平衡状态,相关数据如下:M:3molA 2molB; 2min达到平衡,生成D1.2mol,测得从反应开始到平衡C的速率为0.3mol/Lmin.N:2molC ymolD; 达到平衡时c(A)=0.6mol/L.下列推断的结论中不正确的是( )
A.x=2
B.平衡时M中c(A)=0.6mol/L
C.y>0.8
D.y=2难度: 中等查看答案及解析
-
下列离子方程式书写正确的是( )
A.足量硫化氢气体通入硫酸铁溶液中:H2S+Fe3+=Fe2++S↓+2H+
B.Ca(HCO3)2溶液中加入少量Ca(OH)2溶液:Ca2++OH-+HCO3-=CaCO3↓+H2O
C.用铂电极电解硫酸铜溶液2Cu2++4OH-2Cu+O2↑+2H2O
D.FeI2溶液中通入少量Cl2:2Fe2++Cl2=2 Fe3++2Cl-难度: 中等查看答案及解析
-
下列各溶液中,各离子可能大量共存的有( )
A.含有大量Ba2+的溶液中:HCO3-、Fe3+、Ag+、SO42-、SCN-
B.由水电离的c(OH-)=10-14mol•L-1 的溶液中:CH3COO-、C6H5O-、Na+、K+
C.滴加无色酚酞试液后仍无色的溶液中:Na+、CO32-、K+、ClO-、AlO2-
D.加入铝粉后产生氢气的溶液中:NH4+、Na+、NO3-、Cl-、S2-难度: 中等查看答案及解析
-
NA表示阿佛加德罗常数,下列说法正确的是( )
A.常温下,1L 0.1mol•L-1 CH3COOH溶液中含CH3COO-数为0.1NA
B.标准状况下,2.24L NH3和CH4的混合气体,所含电子总数为NA
C.含1mol硅原子的SiO2晶体中Si-O键的个数为NA
D.分解H2O2制O2,每生成1mol O2转移4NA个电子难度: 中等查看答案及解析
-
将两个铂电极插入KOH溶液中,向两极分别通入CH4和O2,即构成甲烷燃料电池.已知通入甲烷的一极,其电极反应为:CH4+10OH--8e-=CO32-+7H2O;下列叙述正确的是( )
A.通入甲烷的一极为正极
B.通入氧气的一极发生氧化反应
C.该电池总反应为:CH4+2O2+2OH-=CO32-+3H2O
D.该电池在工作时,溶液中的阴离子向正极移动难度: 中等查看答案及解析
-
已知C-C键可以绕键轴自由旋转,结构简式为
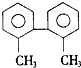 的烃,下列说法正确的是( )
的烃,下列说法正确的是( )
A.分子中至少有8个碳原子处于同一平面上
B.分子中至少有9个碳原子处于同一平面上
C.该烃的一氯取代物最多有四种
D.该烃是苯的同系物难度: 中等查看答案及解析
-
0.1mol/L的NaOH溶液0.2L,通入448mL(标准状况)H2S气体,所得溶液离子浓度大小关系正确的是( )
A.c(Na+)>c(HS-)>c(OH-)>c(H2S)>c(S2-)>c(H+)
B.c(S2-)+c(OH-)=c(H+)+c(H2S)
C.c(Na+)=c(H2S)+c(HS-)+c(S2-)+c(OH-)
D.c(Na+)+c(H+)=c(HS-)+c(S2-)+c(OH-)难度: 中等查看答案及解析
-
有100mL 溶质为MgCl2和AlCl3的混合溶液,c(Cl-)=1.0mol•L-1,c(Mg2+)=0.2mol•L-1.若不考虑水解因素,则要使其中的Mg2+全部转化为Mg(OH)2沉淀而分离出来,至少需要4mol•L-1的NaOH溶液的体积是( )
A.25mL
B.5mL
C.30mL
D.100mL难度: 中等查看答案及解析