-
空气的成分中,体积分数约占21%的气体是( )
A. 氮气 B. 氧气 C. 二氧化碳 D. 稀有气体
难度: 简单查看答案及解析
-
下列符号能表示2个氯分子的是( )
A. Cl2 B. 2Cl2 C. 2Cl D. 2Cl-
难度: 简单查看答案及解析
-
决定元素种类的是
A. 质子数 B. 中子数 C. 电子总数 D. 最外层电子数
难度: 简单查看答案及解析
-
紫薯富含淀粉、蛋白质、维生素、钾、铁、钙、硒等,具有特殊的保健功能。其中的押、铁、钙、硒指的是( )
A. 单质 B. 原子
C. 分子 D. 元素
难度: 中等查看答案及解析
-
下列含金属元素的物质是( )
A. H2SO4 B. Al2O3 C. NO2 D. P2O5
难度: 简单查看答案及解析
-
下列元素的符号书写不正确的是
A. 碳C B. 氯CL C. 钾K D. 铜Cu
难度: 简单查看答案及解析
-
地壳中含量最多的元素是
A. 氧 B. 硅 C. 铝 D. 铁
难度: 简单查看答案及解析
-
下列属于氧化物的是( )
A. O2 B. H2O C. H2SO4 D. KClO3
难度: 简单查看答案及解析
-
下列物质中,含有氧分子的是
A. 二氧化碳 B. 高锰酸钾 C. 过氧化氢 D. 空气
难度: 简单查看答案及解析
-
镍在元素周期表中的信息如下图所示,下列有关镍元素的说法不正确的是
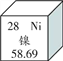
A. 原子序数是28 B. 属于金属元素
C. 原子中的质子数是28 D. 相对原子质量为58.69 g
难度: 中等查看答案及解析
-
下列生活中的做法,不利于节约用水的是( )
A. 用淘米水浇花 B. 用洗过衣服的水冲马桶
C. 隔夜的白开水直接倒掉 D. 洗手打肥皂时暂时关闭水龙头
难度: 简单查看答案及解析
-
下列物质中,属于纯净物的是
A. 牛奶 B. 蒸馏水 C. 矿泉水 D. 海水
难度: 简单查看答案及解析
-
下列方法能鉴别氧气和空气的是
A. 闻气味 B. 将集气瓶倒扣在水中
C. 观察颜色 D. 将带火星的木条伸入集气瓶中
难度: 中等查看答案及解析
-
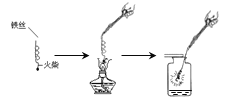
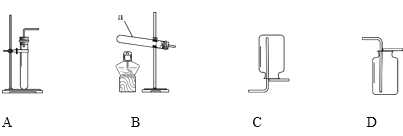
下列实验操作中,正确的是( )
A. 点燃酒精灯
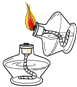 B. 检查装置气密性
B. 检查装置气密性C. 倾倒液体
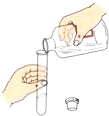 D. 过滤
D. 过滤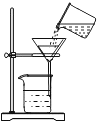
难度: 简单查看答案及解析
-
水的相对分子质量是
A. 16 B. 17 C. 18 D. 18g
难度: 简单查看答案及解析
-
下列物质在氧气中燃烧,火星四射并生成黑色固体的是
A. 硫 B. 镁条 C. 红磷 D. 铁丝
难度: 简单查看答案及解析
-
化学变化前后发生改变的是( )
A. 元素种类 B. 原子个数 C. 分子种类 D. 原子质量
难度: 简单查看答案及解析
-
牙膏中的含氟化合物对牙齿有保护作用.一种氟原子的原子核内有9个质子和10个中子,该原子的核电荷数为( )
A. 7 B. 9 C. 10 D. 19
难度: 简单查看答案及解析
-
下列有关实验现象的描述中,正确的是
A. 碳酸钙与稀盐酸反应,生成氯化钙、二氧化碳和水
B. 硫粉在氧气中剧烈燃烧,发出明亮的蓝紫色火焰
C. 碳酸钠粉末中滴加稀盐酸,观察到有大量白色气泡产生
D. 水加热沸腾,试管口的玻璃片上有水雾出现
难度: 简单查看答案及解析
-
卫星运载火箭的动力由高氯酸铵(NH4ClO4)发生反应提供,化学方程式为:2NH4ClO4
N2↑+Cl2↑+2O2↑+4X.则X的化学式是( )
A. H2 B. H2O C. H2O2 D. HCl
难度: 中等查看答案及解析
-
葡萄糖的化学式为C6H12O6,下列有关葡萄糖的说法正确的是
A. 葡萄糖是由24个原子构成的 B. 葡萄糖是由碳、氢气和氧气组成的
C. 葡萄糖由三种元素组成 D. 葡萄糖分子由碳原子和水分子构成
难度: 简单查看答案及解析
-
用如图所示装置收集一瓶纯净氧气,以下说法不正确的是
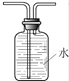
A. 集气瓶中应装满水,确保无气泡
B. 左端导管口连接产生氧气的发生装置
C. 右端导管口连接产生氧气的发生装置
D. 排出水的体积即为收集到氧气的体积
难度: 简单查看答案及解析
-
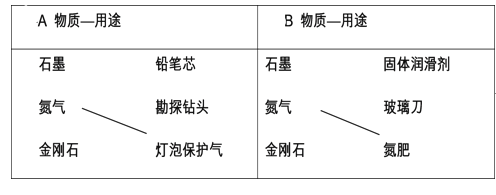
石墨烯是从石墨中分离出来的单原子层石墨,它具有超强导电、导热的性能。下列关于石墨烯的说法中,不正确的是
A. 属于一种新型的化合物 B. 可做散热材料
C. 可做电池的电极 D. 在一定条件下能与氧气反应
难度: 简单查看答案及解析
-
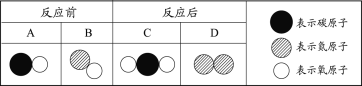
下列关于2CO + O2
2CO2的说法中,正确的是
A. 反应后原子种类减少
B. 表示一氧化碳加氧气等于二氧化碳
C. 参加反应的一氧化碳与氧气的质量比为2∶1
D. 参加反应的氧气与生成的二氧化碳的分子个数比为1∶2
难度: 中等查看答案及解析
-
如图为尿素【CO(NH2)2】中各元素质量分数的示意图,其中表示氮元素质量分数的是( )
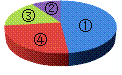
A. ① B. ② C. ③ D. ④
难度: 中等查看答案及解析
-
为了证明人呼出的气体中含有CO2且能有效排除空气中CO2的干扰,某学生设计了如图所示的实验装置。A、B中均放入足量的澄清石灰水后进行实验。下列说法不正确的是
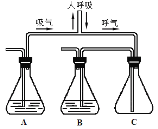
A. 可以根据A中的澄清石灰水比B中的澄清石灰水更浑浊验证人呼出气体比吸入气体中的二氧化碳的含量高
B. A瓶作用是除去被人体吸入的空气中CO2
C. C瓶作用防止人在吸气时将澄清石灰水吸入嘴中(安全瓶)
D. B瓶作用是检验人呼出的气体中是否含有CO2
难度: 简单查看答案及解析
-
下列关于用红磷验证质量守恒定律说法不正确的是
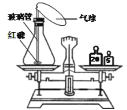
A. 暗红色的红磷燃烧,放热,产生大量白烟
B. 小气球的作用之一是为了使装置保持密闭
C. 该实验不能用于验证质量守恒定律
D. 冷却到室温时,拔开橡胶塞后又盖好,称量,指针偏左
难度: 简单查看答案及解析
-
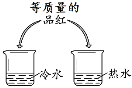
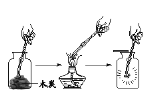
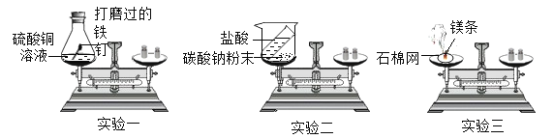
根据下图所示的验证实验进行分析,得出的结论不正确的是




A.黄铜比纯铜
硬度大
B.蜡烛中含有氢、氧元素
C.呼出的气体中二氧化碳含量比空气高
D.分子在不断地运动
A. A B. B C. C D. D
难度: 简单查看答案及解析
-
纳米材料具有特殊的性质和功能。纳米二氧化钛(TiO2)参与的光催化反应可使吸附在其表面的甲醛等物质被氧化,降低空气中有害物质的浓度。正钛酸(H4TiO4)在一定条件下分解失水可制得纳米TiO2。下列说法不正确的是
A. 甲醛对人体健康有害
B. 纳米TiO2添加到墙面涂料中,可消除甲醛
C. 纳米TiO2与普通的TiO2的性质、功能完全相同
D. 制备纳米TiO2的反应:H4TiO4
TiO2 + 2H2O
难度: 中等查看答案及解析
-
已知:2KClO3
2KCl + 3O2↑,如图表示一定质量的KClO3和MnO2固体混合物受热过程中,某变量y随时间的变化趋势。纵坐标表示的是(资料:KClO3和KCl均为白色体)
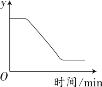
A. 固体中氧元素的质量 B. 生成O2的质量
C. 固体中MnO2的质量 D. 固体中钾元素的质量分数
难度: 困难查看答案及解析
-
某烟气脱硫的工艺不仅能消除
,还能将其转化为石膏(
)等产品,实现“变废为宝”。主要物质转化关系如下:
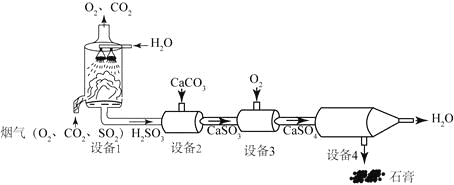
(1)设备1中,通过喷淋水脱去烟气中的
,该反应的化学方程式为 。
(2)设备2中,加入
的目的是将
转化为 。
(3)设备3中,反应前后化合价发生改变的元素是 。
难度: 中等查看答案及解析