-
下列过程属自发的是
A.气体从低密度处向高密度处扩散 B.水由低处向高处流
C.煤气的燃烧 D.室温下水结成冰
难度: 中等查看答案及解析
-
下列各图所表示的反应是吸热反应的是
A.
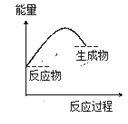 B.
B. 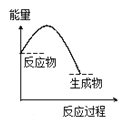 C.
C.  D.
D. 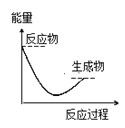
难度: 简单查看答案及解析
-
乙醇在空气中燃烧生成二氧化碳和水,下列说法正确的是( )
A.断裂H-O键放出能量 B.形成H-O键吸收能量
C.该反应是放热反应 D.该反应是吸热反应
难度: 简单查看答案及解析
-
下列有关金属铁的腐蚀与防护,说法不正确的是
A.酸雨后易发生析氢腐蚀、炒锅存留盐液时易发生吸氧腐蚀
B.当镀锡铁镀层破损时,铁不易被腐蚀
C.铁与电源负极连接可实现电化学保护
D.将钢管与锌管一起堆放时可保护钢管少受腐蚀
难度: 中等查看答案及解析
-
有关图所示原电池的叙述正确的是
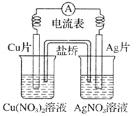
A.电流沿导线由Cu片流向Ag片
B.正极的电极反应是Ag++e-=Ag
C.Cu片上发生还原反应,Ag片上发生氧化反应
D.反应时盐桥中的阳离子移向Cu(NO3)2溶液
难度: 中等查看答案及解析
-
P4(白磷,s)⇌4P(红磷,s) ΔH=-17kJ·mol-1,根据以上热化学方程式,下列推论正确的是( )
A.正反应是一个吸热反应
B.白磷比红磷稳定
C.当1mol白磷完全转变成红磷时放出17kJ热量
D.当4g红磷转变成白磷时吸收17kJ热量
难度: 中等查看答案及解析
-
用惰性电极电解下列溶液,电解一段时间后,电解质溶液的pH减小的是( )
A.KCl B.KOH C.Cu(NO3)2 D.Na2SO4
难度: 简单查看答案及解析
-
已知:在298K、100kPa时,
①C(s,石墨)+O2(g)=CO2(g) △H1=-393.5kJ·mol-1;
②2H2(g)+O2(g)=2H2O(l) △H2=-571.6kJ·mol-1;
③2C2H2(g)+5O2(g)=4CO2(g)+ 2H2O(l) △H3=-2599kJ·mol-1;
则反应2C(s,石墨)+H2(g)=C2H2(g)的反应热△H为( )
A.-237.46kJ·mol-1 B.+226.7kJ·mol-1
C.-226.7kJ·mol-1 D.+237.46kJ·mol-1
难度: 简单查看答案及解析
-
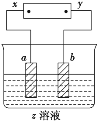
如图所示,x、y分别是直流电源的两极,通电后发现a极极板处有无色、无味的气体放出,b极极板质量增加,符合这一情况的是( )
选项
a极板
b极板
x电极
z溶液
A
锌
石墨
正极
CuSO4
B
石墨
石墨
负极
NaOH
C
石墨
银
正极
AgNO3
D
铜
石墨
负极
CuCl2
A.A B.B C.C D.D
难度: 中等查看答案及解析
-
如图所示,a、b是石墨电极,通电一段时间后,b极附近溶液显红色。下列说法错误的
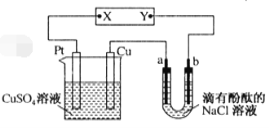
A.X极是电源正极,Y极是电源负极 B.Cu电极上增重6.4g时,b极产生2.24 L气体
C.电解过程中CuSO4溶液的pH逐渐减小 D.a极的电极反应式为2Cl――2e-=Cl2↑
难度: 中等查看答案及解析
-
Mg-H2O2电池可用于驱动无人驾驶的潜航器。该电池以海水为电解质溶液,示意图如下。该电池工作时,下列说法正确的是( )
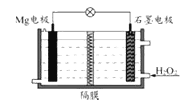
A.Mg电极是该电池的正极 B.H2O2在石墨电极上发生还原反应
C.石墨电极附近溶液的pH减小 D.溶液中Cl-向石墨电极移动
难度: 中等查看答案及解析
-
一定温度下的恒容容器中,能标志某可逆反应2A(g)+2B(g)
C(g)+3D(g)己达平衡状态的是
A.混合气体的密度保持不变 B.气体A的质量不随时间变化而变化
C.2v正(A)=3v逆(D) D.混合气体的压强不随时间变化而变化
难度: 中等查看答案及解析
-
用酸性氢氧燃料电池为电源进行电解的实验装置示意图如图所示。下列说法不正确的是( )

A.燃料电池工作时,正极反应为O2+4H++4e﹣=2H2O
B.a极是铜,b极是铁时,可实现铁上镀铜
C.a极是含锌、铁的粗铜,b极是纯铜,a极溶解铜的质量与b极析出的铜质量相等
D.若a、b两极均为石墨时,在相同条件下,a极产生的气体与电池中消耗的H2体积不相同
难度: 中等查看答案及解析
-
在一密闭容器中,aA(g)
bB(g)达到平衡后,保持温度不变,将容器体积增大一倍,当达到新的平衡时,B的浓度是原来的40%,则( )
A.物质A的转化率减小
B.a<b
C.物质B的质量分数增大了
D.平衡向正反应方向移动了
难度: 中等查看答案及解析
-
对于反应C(s)+H2O(g)
CO(g)+H2(g) ΔH >0,下列有关说法正确的是( )
A.增加C(s)的物质的量,平衡正向移动
B.平衡常数表达式为K=
C.升高体系温度,平衡常数K减小
D.增大体系压强,平衡常数K不发生变化
难度: 简单查看答案及解析
-
用石墨电极电解200mLH2SO4和CuSO4的混合溶液,通电一段时间后,两极均收集到2.24L气体(标准状况),原混合溶液中Cu2+的物质的量浓度为( )
A.0.2mol·L-1 B.0.3mol·L-1 C.0.4mol·L-1 D.0.5mol·L-1
难度: 中等查看答案及解析