-
下列说法不正确的是
A.将容易吸水的物质放在已知质量的烧杯里用托盘天平称量
B.用试管夹夹持试管时,应由试管底部套上,取下
C.振荡试管时,用手紧握试管,拇指堵住试管口,上下晃动
D.滴加液体时,滴瓶滴管的尖端不能触及已加过其它试剂的试管内壁
难度: 简单查看答案及解析
-
日常生活中时刻发生着变化下列变化中包含化学变化的是( )
A.美酒飘香 B.塑料降解 C.切割玻璃 D.滴水成冰
难度: 简单查看答案及解析
-
从化学学科角度看,下列说法正确的是
①煤中含有硫和氮元素,燃烧会产生SO2和NO2等污染物,大量排放到空气中能形成酸雨;
②烟草燃烧释放的物质中,尼古丁能与血红蛋白结合而引起中毒;
③洗涤剂具有乳化作用能去除油污:
④米和面中含有的糖类物质主要是淀粉,它在人体的消化系统中经淀粉酶的催化作用,最终变为葡萄糖;
⑤硝酸铵(NH4NO3)能促进植物茎、叶生长茂盛;
⑥亚硝酸盐是有毒的物质,不能代替食盐使用;
⑦房间里着火应立即打开门窗。
A.①②③④⑥ B.④⑤⑥⑦ C.①③④⑤⑥ D.②③⑤⑦
难度: 中等查看答案及解析
-
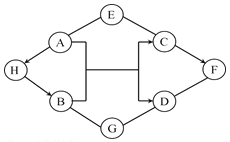
对于反应
,下列说法错误的是( )
A.若N是盐酸,M为碳酸盐,则C和D中一定有一种易分解
B.若M为可溶性盐,N为可溶性碱,则C和D可能都难溶于水
C.若N,D为单质,M,C为化合物,则M一定是可溶性盐或酸
D.若M和N是盐,则C和D也都是盐
难度: 困难查看答案及解析
-
已知复分解反应
可进行。在常温下,测得相同浓度的下列六种溶液的pH:表中数据揭示出复分解反应的一条规律,即碱性较强的物质发生类似反应可以生成碱性弱的物质。依照该规律,请你判断下列反应不能成立的是
溶质
CH3COONa
NaHCO3
Na2CO3
NaClO
NaCN
pH
8.8
8.6
11.6
10.3
11.1
A.
B.
C.
D.
难度: 中等查看答案及解析
-
下列说法中正确的是
A.石油主要含碳、氢两种元素,属于可再生能源
B.石油的分馏是物理变化,各馏分均是纯净物
C.煤的气化和液化是化学变化
D.可燃冰属于清洁能源,不会对环境产生任何影响
难度: 中等查看答案及解析
-
下列图像能正确反映所对应叙述关系的是
A.
一定量的木炭还原氧化铜,剩余固体质量与反应时间的关系
B.
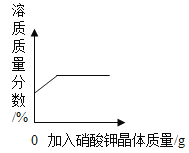 t℃时,向饱和硝酸钾溶液中加入硝酸钾晶体,溶质质量分数与加入硝酸钾质量的关系
t℃时,向饱和硝酸钾溶液中加入硝酸钾晶体,溶质质量分数与加入硝酸钾质量的关系C.
将锌粒加入到一定量的稀硫酸中,溶液的质量与反应时间的关系
D.
向硫酸和硫酸铜混合溶液中加入氢氧化钠溶液,沉淀质量与加入量的关系
难度: 困难查看答案及解析
-
化学与生产、生活关系密切,下列现象或事实及其分析都正确的是
选项
现象或事实
分析
A
发电厂将燃煤产生的废气通入高温下的石灰石
主要目的是生产CaSO4,并得到副产品CO2
B
ClO2代替Cl2对饮用水消毒
ClO2消毒杀毒效率高,二次污染小
C
小苏打、苛性钠都可用于治疗胃酸过多
小苏打、苛性钠都能与胃酸反应
D
用绿色环保融雪除冰剂代替氯化钙、氯化钠融雪除冰
氯化钙 、氯化钠会造成环境污染,但不会加速桥梁等设备腐蚀
A.A B.B C.C D.D
难度: 困难查看答案及解析
-
甲物质的溶解度(S)随温度(t)变化曲线如图所示,下列说法正确的是( )
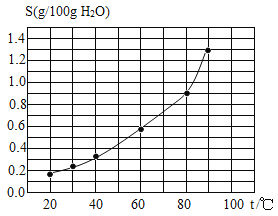
A.60℃时,甲的溶解度约为0.6
B.20℃时,甲可溶于水
C.90℃时,在50g水中加入0.7g甲,充分搅拌后得到饱和溶液
D.将80℃时甲的溶液降温至60℃,一定析出甲晶体
难度: 简单查看答案及解析
-
固体X可能由氢氧化钠、碳酸钠、氯化钠、硝酸镁、硝酸钡、硫酸钠、硫酸铜中的一种或几种物质组成(提示:以上物质中,只有氢氧化钠和碳酸钠的水溶液显碱性)。为确定其组成,进行如下实验:
①将固体X加入水中充分溶解,得到无色溶液;
②测X溶液的pH,pH= 13;
③向X的溶液中加入足量的硝酸钡溶液,产生白色沉淀,过滤;
④向步骤③所得沉淀中加入足量的稀盐酸,沉淀不溶解;
⑤向步骤③所得的滤液中加入过量的稀硝酸,再加入硝酸银溶液,产生白色沉淀。
根据以上实验信息,关于固体X组成的判断有以下几种说法:
①不能确定是否有硝酸镁;
②硝酸钡、硫酸铜、碳酸钠一定不存在;
③硫酸钠和氢氧化钠一定存在;
④不能确定是否有氯化钠。
以上说法中正确的个数是
A.1个 B.2个 C.3个 D.4个
难度: 困难查看答案及解析