-
下列说法正确的是
A.分子晶体中一定存在分子间作用力,不一定存在共价键
B.分子中含两个氢原子的酸一定是二元酸
C.含有金属阳离子的晶体一定是离子晶体
D.元素的非金属性越强,其单质的活泼性一定越强
难度: 中等查看答案及解析
-
下列反应中一定不能自发进行的是( )
A.2KClO3(s)=2KCl(s)+ 3O2(g) △H<0,△S>0
B.CO(g)=C(s,石墨)+ O2(g) △H>0,△S<0
C.4Fe(OH)2(s)+2H2O(l)+O2(g)=4Fe(OH)3(s) △H<0,△S<0
D.NH4HCO3(s)+CH3COOH(aq)=CO2(g)+CH3COONH4(aq)+H2O(l) △H>0,△S>0
难度: 简单查看答案及解析
-
第四周期中,最外层有两个电子的元素有()种
A.3 B.6 C.9 D.12
难度: 简单查看答案及解析
-
下列结构属于从NaCl晶体中分割出来的结构示意图是( )
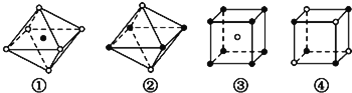
A.①和③ B.①和④ C.只有③ D.只有④
难度: 中等查看答案及解析
-
下列无机含氧酸分子中酸性最强的是()
A. HNO2 B. H2SO3 C. HClO3 D. HClO4
难度: 简单查看答案及解析
-
下列给出的几种氯化物的熔点和沸点:
NaCl
MgCl2
AlCl3
SiCl4
熔点/℃
801
714
190(5×101 kPa)
-70
沸点/℃
1413
1412
180
57.57
据表中所列数据判断下列叙述与表中相吻合的是( )
A.AlCl3在加热条件下能升华 B.SiCl4晶体属于原子晶体
C.AlCl3晶体是典型的离子晶体 D.NaCl的晶格能比MgCl2小
难度: 简单查看答案及解析
-
已知:2H2(g)+O2(g)=2H2O(l) ΔH=−571.6kJ·mol−1
2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l) ΔH=−1452kJ·mol−1
H+(aq)+OH−(aq)=H2O(l) ΔH=−57.3kJ·mol−1
下列说法正确的是
A.H2(g)的燃烧热为571.6kJ·mol−1
B.H2SO4(aq)+Ba(OH)2(aq)=BaSO4(s)+H2O(l) ΔH=−57.3 kJ·mol−1
C.3H2(g)+CO2(g)=CH3OH(l)+H2O(l) ΔH=+135.9 kJ·mol−1
D.等质量的H2(g)和CH3OH(l)完全燃烧,H2(g)燃烧放出的热量多
难度: 简单查看答案及解析
-
同体积的1mol/L的HCl、H2SO4、CH3COOH、HNO3分别加入过量的Mg。下列叙述正确的是( )
A.HNO3、HCl、H2SO4中放出H2的速率相同
B.HCl、HNO3中放出H2的量相等
C.HCl、CH3COOH中放出H2的量相等
D.H2SO4中放出H2的量最多,其余的相等
难度: 中等查看答案及解析
-
在密闭容器中,一定条件下进行如下反应2NO(g)+2CO(g)
N2(g)+2CO2(g),△H=-373.2kJ·mol-1,达到平衡后,为提高该反应的速率和NO的转化率,采取的正确措施是( )
A.加催化剂同时升高温度 B.加催化剂同时增大压强
C.升高温度同时充入N2 D.降低温度同时增大压强
难度: 中等查看答案及解析
-
某恒容密闭容器中充入1molPCl5气体,发生反应:PCl5(g)
PCl3(g)+Cl2(g) △H<0。仅改变某一条件,该平衡由状态I移动到状态II,变化曲线如图所示。可能改变的条件是
A.继续通入1mol PCl5气体 B.继续通入1mol PCl3气体
C.升高 D.加入催化剂
难度: 中等查看答案及解析
-
在容积一定的密闭容器中,置入一定量的一氧化氮和足量碳发生化学反应:C(s)+2NO(g)
CO2(g)+N2(g),平衡时c(NO)与温度T的关系如图所示,则下列说法正确的是( )
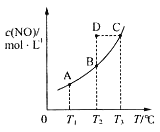
A.该反应的ΔH>0
B.若该反应在T1、T2℃时的平衡常数分别为K1、K2,则K1<K2
C.在T2℃时,若反应体系处于状态D,则此时v正>v逆
D.若状态B、C、D的压强分别为p(B)、p(C)、p(D),则p(C)=p(D)>p(B)
难度: 中等查看答案及解析
-
在25℃时,用蒸馏水稀释1mol·L-1的氨水至0.01mol·L-1,随着溶液的稀释,下列各项比值中始终不变的是( )
A.
B.
C.
D.
难度: 中等查看答案及解析
-
下图是电解饱和 NaCl 溶液的实验装置,x、y 都是惰性电极,a 是饱和 NaCl 溶液,同时在两边各滴入几滴酚酞试液,下列有关该实验正确的说法是
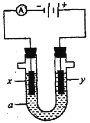
A.x 电极为阳极,y 电极为阴极
B.x 电极附近溶液变红色,且有刺激性气味气体产生
C.若将两电极产生的气体收集起来,X电极得到的气体与Y电极得到的气体之比之比略大于 1:1
D.电解后,将溶液混匀,电解前后溶液的 pH 未发生变化
难度: 中等查看答案及解析
-
在一密闭容器中有如下反应:aX(g)+bY(g)
nW(g)ΔH=Q某化学兴趣小组的同学根据此反应在不同条件下的实验数据,作出了如图曲线图:其中ω(W)表示W在反应混合物中的百分含量,t表示反应时间。其它条件不变时,下列分析可能正确的是( )
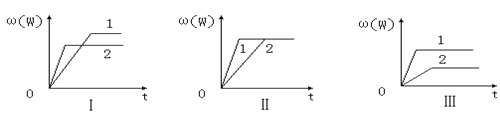
A.图Ⅱ可能是不同压强对反应的影响,且P1>P2,n<a+b
B.图Ⅲ可能是不同温度对反应的影响,且T1>T2,Q<0
C.图Ⅰ可能是不同压强对反应的影响,且P2>P1,a+b<n
D.图Ⅱ可能是在同温同压下催化剂对反应的影响,且2使用的催化剂效果好
难度: 中等查看答案及解析
-
将1 L含有0.4 mol Cu(NO3)2和0.4 mol KCl的水溶液,用惰性电极电解一段时间后,在一电极上析出19.2 g Cu。此时,在另一电极上放出气体的体积在标准状况下为(不考虑产生的气体在水中的溶解)( )
A.6.72 L B.13.44 L C.3.36 L D.5.6 L
难度: 中等查看答案及解析
-
LED即发光二极管,是一种能够将电能转化为光能的固态半导体器件。如图是某课外活动小组设计的用化学电源使LED灯发光的装置。下列说法不正确的是
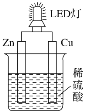
A.装置中存在“化学能→电能→光能”的转化
B.铜片上发生的反应为2H++2e-=H2↑
C.锌片是负极,其质量逐渐减小
D.如果将稀硫酸换成稀盐酸,则导线中不会有电子流动
难度: 简单查看答案及解析
-
对于可逆反应N2(g)+3H2(g)
2NH3(g) ΔH<0,下列各项对示意图的解释与图像相符的是
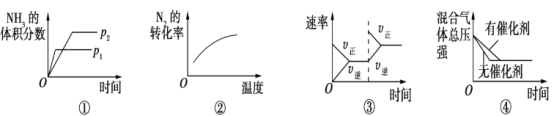
A.①压强对反应的影响(p2>p1) B.②温度对反应的影响
C.③平衡体系增加N2对反应的影响 D.④催化剂对反应的影响
难度: 中等查看答案及解析
-
工业上合成CH3OH的原理为:2H2(g)+CO
CH3OH(g),一定温度下,向1L恒容密闭容器中充入H2和CO,反应达平衡时CH3OH的体积分数与反应物投料之比(n(H2)/n(CO))的关系如图所示。下列说法错误的是

A.相同条件下,达到平衡时混合气体的密度与反应前相同
B.a、b、c、d四点中,c点CO的转化率最大。
C.若投料时n(CO)不变,a、b、c、d四点中d处CH3OH的物质的量最大
D.图像中 c点到d点,平衡向正反应方向移动
难度: 中等查看答案及解析
-
将 CO2 在一定条件下与 H2 反应转化为甲醇(CH3OH)是变废为宝的好办法,一定条件下,每转化 44 kg CO2 放出的热量为 49000 kJ,CO2 转化为甲醇过程中浓度随时间的变化曲线如图所示(已知反应物和生成物在此条件下均为气体),下列叙述中正确的是
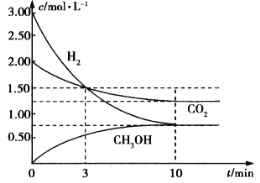
A.0~3 min 内,用 CO2 和 H2 来表达的平均反应速率相等,均为 0.5 mol/(L·min)
B.此反应的热化学方程式为 CO2(g) + 3H2(g) CH3OH(g) + H2O(g) △H = - 49 kJ/mol
C.此条件下反应的平衡常数K=0.753×1.25/(0.75×0.75)
D.降低温度,此反应的平衡常数可能为 0.8
难度: 中等查看答案及解析