-
某卡车上贴有
 标志,则它运输的化学品可能是( )
标志,则它运输的化学品可能是( )A.蔗糖 B.浓硫酸 C.酒精 D.食盐
难度: 简单查看答案及解析
-
下列有关实验安全问题的叙述中正确的是( )
A.少量的浓硫酸沾到皮肤上时,先用大量的水冲洗,再涂上2%-3%的硼酸溶液
B.取用化学药品时,应特别注意观察药品包装容器上的安全警示标志
C.在实验室里可用品尝的办法区别食盐和蔗糖晶体
D.各放一张质量相同的滤纸于天平的两托盘上,将NaOH固体放在右盘纸上称量
难度: 简单查看答案及解析
-
下列各项说法正确的是( )
A.可以直接加热的仪器有:坩埚、烧杯、试管、蒸发皿
B.量筒的“0”刻度位置在量筒的下端
C.用如图所示装置进行实验:从B口进气,收集CO2
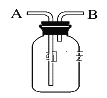
D.在稀释浓硫酸时将浓硫酸沿器壁慢慢注入水中,并用玻璃棒不断搅拌
难度: 简单查看答案及解析
-
下列有关物质的量的说法正确的是( )
A.物质的量的符号是:mol
B.摩尔是国际单位制的七个基本物理量之一
C.1molSO2约含有6.02×1023个二氧化硫分子
D.0.012kg12C中所含碳原子数是1mol
难度: 简单查看答案及解析
-
下列有关说法正确的是( )
A.液态HCl不导电,但属于电解质
B.强电解质溶液的导电能力一定比弱电解质溶液强
C.硫酸钡不溶于水,所以硫酸钡是非电解质
D.二氧化碳溶于水得到的溶液能导电,所以二氧化碳是电解质
难度: 简单查看答案及解析
-
NA代表阿伏加德常数,下列说法中正确的是( )
A.2g氢气所含原子数目为NA
B.在常温常压下,11.2L氮气所含的原子数目为NA
C.17gNH3所含电子数目为10NA
D.1L1mol/LHNO3溶液中所含氧原子数为3NA
难度: 简单查看答案及解析
-
下列装置或操作能达到实验目的是
实验目的
A. 检查装置的气密性
B. 蒸发操作中移开蒸发皿
C. 实验室制取蒸馏水
D. 分离水和酒精
装置或操作

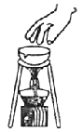

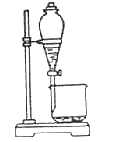
A.A B.B C.C D.D
难度: 中等查看答案及解析
-
常温下,下列各组离子在指定溶液中能大量共存的是( )
A.强酸性溶液中:Na+、K+、Cl-、SO42-
B.无色透明溶液中:Cu2+、Ba2+、Cl-、NO3-
C.含有大量Fe2+的溶液中:H+、Na+、NO3-、SO42-
D.使酚酞试液变红的溶液中:Fe3+、Al3+、SO42-、Cl-
难度: 简单查看答案及解析
-
“阳光穿透墙壁上的小缝,原本昏暗的屋子突然变得通亮起来,一条条明亮的通路里,许多细小的尘埃像一个个身材苗条的少女,踏着清晨的脚步,和着天籁般的鸟鸣声,翩翩起舞”。阳光穿过缝隙形成的景象产生的本质原因是( )
A.阳光是一种胶体
B.尘埃是一种胶体
C.屋内空气中的尘埃微粒直径大小约为1~100nm
D.发生丁达尔效应
难度: 简单查看答案及解析
-
下列溶液中,Cl-的物质的量浓度最大的是( )
A.75mL4mol/L的KClO3溶液
B.50mLAl3+浓度为1mol/L的AlCl3溶液
C.9.5gMgCl2溶于水所配得的100mL溶液
D.1L密度为1.1g/cm3、质量分数为3.65%的HCl溶液
难度: 简单查看答案及解析
-
下列有关气体摩尔体积的说法,正确的是( )
A.64gSO2的体积约为22.4L
B.1molO2的体积约为22.4L,则一定处于标准状况
C.在标准状况下,1molH2O的体积约为22.4L
D.总质量为28g的N2和CO的混合气体,在标准状况下的体积约为22.4L
难度: 简单查看答案及解析
-
在体积相同的两个密闭容器中分别充入O2和O3气体,当这两个容器内的温度和密度相等时,下列说法正确的是( )
A.O2比O3的质量大 B.两种气体的压强相等
C.两容器中气体所含质子数相等 D.O2与O3的分子数相等
难度: 中等查看答案及解析
-
H3AsO3是一种剧毒物,可加入祛毒剂SnCl2来除去,反应方程式为:2H3AsO3+3SnCl2+12X=2As↓+3H2SnCl6+6H2O。下列关于该反应的说法中正确的是( )
A.还原剂是H3AsO3
B.X的化学式为HCl,是该反应的氧化剂
C.每生成0.2molAs,还原剂得到0.6mol电子
D.该反应转移2mol电子,则消耗祛毒剂SnCl2为1mol
难度: 简单查看答案及解析
-
复印机工作时易产生臭氧(O3),少量的臭氧有消毒空气之功效,但臭氧浓度过高时,对人的呼吸道、肺部有刺激。已知臭氧可发生如下反应:O3+2KI+H2O=2KOH+O2+I2,对该反应的下列说法不正确的是( )
A.KI发生的是氧化反应
B.O3是氧化剂,O3被还原生成的产物是KOH
C.氧化产物I2与还原产物O2的物质的量之比为1:1
D.H2O既不是氧化剂也不是还原剂
难度: 中等查看答案及解析