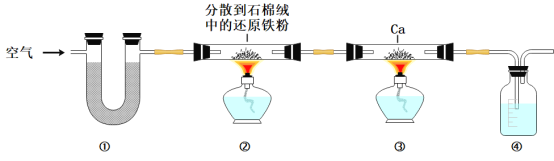
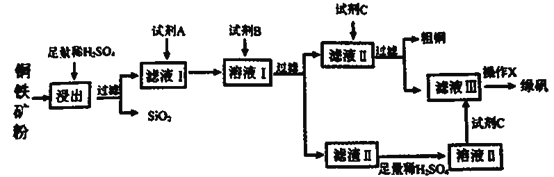
-
化学与生活密切相关。下列叙述错误的是
A.镍铬烤瓷牙是一种由镍铬合金制成的牙齿,它耐腐蚀,价格低廉,是国内做的最多的烤瓷牙,28号镍元素属于过渡元素。
B.燃放烟花是利用了某些金属元素的焰色反应
C.氢氧化铝是医用胃酸中和剂的一种
D.青花瓷、石英玻璃的主要成分都是硅酸盐
难度: 中等查看答案及解析
-
下列化学用语正确的是
A.中子数为78的碘原子:78I
B.HClO的结构式为H-O-Cl
C.N2的电子式:
D.硫原子的结构示意图:
难度: 中等查看答案及解析
-
设NA代表阿伏加德罗常数的值,下列说法正确的是
A.13.6g液态KHSO4中含有0.3NA个离子
B.25℃ 1 L pH=2的硫酸溶液中,含有的H+数目为0.02NA
C.在标准状况下,11.2L HF中含有的原子数为NA
D.56g铁粉与1 mol Cl2完全反应后,转移电子数目为2NA
难度: 中等查看答案及解析
-
某学习小组需1.0000 mol/L的NaOH溶液240mL。下列有关配制时的说法正确的是
A.称量时,托盘天平两边应放等质量的两张纸
B.配置时需用托盘天平称取9.6gNaOH固体
C.溶解NaOH固体后,将所得溶液立即转移到容量瓶中,会导致所配溶液浓度偏大
D.配制好的NaOH溶液应转移到带有玻璃塞的试剂瓶中
难度: 中等查看答案及解析
-
将饱和的氯化铁溶液分成两等份,把其中一份溶液滴加到沸水中,继续煮沸至溶液呈红褐色,停止加热,得到分散系I;把另一份溶液滴加到凉水中,得到分散系II。则下列说法正确的是
A.两份分散系中的分散质均为氯化铁
B.两份分散系均能全部通过半透膜
C.分别向两份分散系中滴加足量NaOH溶液,最终都能得到沉淀
D.两份分散系均能发生丁达尔效应
难度: 中等查看答案及解析
-
下列关于SO2和NO2的叙述中正确的是
A.均只能使紫色石蕊溶液变红
B.与水反应都发生氧化还原反应
C.均是酸性氧化物
D.均能将FeSO4溶液氧化为Fe2(SO4)3溶液
难度: 中等查看答案及解析
-
室温下,下列各组离子在指定的溶液中能大量共存的是
A.0.1 mol·L-1 FeCl2溶液中,NH4+、ClO-、Br-、SO42-
B.饱和氯水中,Fe3+、NO3-、Al3+、SO42-
C.PH=7的溶液中,Cl-、SO42-、Na+、Fe3+
D.0.l mol/L NaAlO2溶液中,HCO3-、Cl-、Ba2+、K+
难度: 中等查看答案及解析
-
对Zn+2MnO2+2H2O=2MnO(OH)+Zn(OH)2,下列说法错误的是
A.氧化产物和还原产物的物质的量之比为2:1
B.MnO(OH)中Mn的化合价为+3价
C.MnO2在反应中被还原
D.Zn是此反应中还原剂
难度: 中等查看答案及解析
-
56号元素在元素周期表中的位置是
A.第六周期IIA族 B.第四周期IVA族
C.第五周期IIA族 D.第五周期IVA族
难度: 中等查看答案及解析
-
P、S、Cl位于同一周期,下列说法正确的是
A.量高价氧化物对应的水化物酸性:H2SO4>HClO4
B.气态氢化物稳定性:PH3>H2S>H2O
C.非金属性:P>S>Cl
D.还原性:H2S>HCl
难度: 简单查看答案及解析
-
下列离子方程式书写正确的是
A.向Ba(OH)2溶液中滴加NaHSO4溶液至溶液显中性:Ba2++OH-+H++SO42-=BaSO4↓+H2O
B.稀硫酸中加入铁粉:2Fe+6H+=2Fe3++3H2↑
C.KMnO4溶液与草酸溶液混合:2MnO4-+5H2C2O4+6H+=2Mn2++8H2O+10CO2↑
D.铁粉溶于过量稀硝酸:3Fe+8H++2NO3-=3Fe2++4H2O+2NO↑
难度: 中等查看答案及解析
-
下图是某元素的价类二维图,A为正盐,通常条件下Z是无色溶液,D的相对分子质量比E小16,各物质转化关系如图所示。下列说法不正确的是
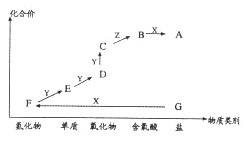
A.若X是一种强碱,则F为硝酸
B.若X是一种强酸,则F为硫酸
C.B和F在一定条件下均能发生反应,且都生成
D.B在一定条件下可直接与Y反应生成D
难度: 中等查看答案及解析
-
NaNO2是一种食品添加剂,但食用过量可能致癌。质监部门常用酸性KMnO4溶液检验NaNO2,并测定其含量。以确定食品是否符合国家规定。下列说法正确的是
A.该上述反应中KMnO4是氧化剂
B.NO2-被还原为N2
C.测定NaNO2含量时,当溶液变为紫色时,就能立即停止滴加酸性KMnO4溶液
D.反应过程中溶液的pH减少
难度: 简单查看答案及解析
-
用下面装置制备干燥的NH3,下列说法不正确的是
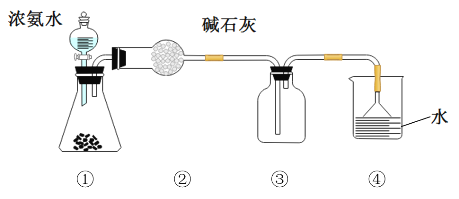
A.装置①,锥形瓶中的试剂可能是碱石灰 B.装置②,作用是干燥NH3
C.装置③,可以收集NH3 D.装置④,作用是尾气处理
难度: 中等查看答案及解析
-
下列实验与图象不对应的是
选项
A
B
C
D
实验
向NH4C1溶液中加入过量Na2O2固体
向稀硝酸溶液中加入过量的铁粉
明矾溶液中逐滴加Ba(OH)2溶液至过量
向含等物质的量的NaOH和Na2CO3的混合溶液中滴加过量的稀盐酸
图象
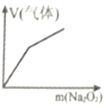
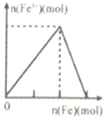
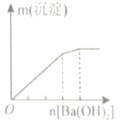
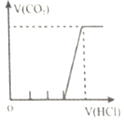
A.A B.B C.C D.D
难度: 中等查看答案及解析
-
2016年IUPAC命名117号元素为Ts,下列说法不正确的是
A.Ts的原子核外最外层电子数是7
B.Ts是一种非金属元素
C.其中一种核素
的中子数为176
D.Ts在周期表的第七周期第VIIA族
难度: 简单查看答案及解析
-
下列实验操作、实验现象及实验结论均正确的是
选项
实验操作
实验现象
实验结论
A
向某无色溶液中滴加稀盐酸
溶液变浑浊
原溶液中一定存在Ag+
B
向某溶液中逐滴加入足量的盐酸
先产生白色淀后,后白色沉淀溶解,直至消失
该溶液中一定含有AlO2﹣
C
向某溶液中通入Cl2,再滴入KSCN溶液
溶液变红
原溶液中一定含有Fe2+
D
向某溶液中加入NaOH溶液,充分反应
没有产生能使湿润的红色石蕊试纸变蓝的气体
溶液中一定不含NH4+
A.A B.B C.C D.D
难度: 中等查看答案及解析
-
W、X、Y、Z均为短周期主族元素,原子序数依次增大,W是周期表中原子半径最小的原子,X与Y形成的某种化合物能与水发生氧化还原反应,且生成酸,W、X、Y三种元素的核电荷数之和等于Z的原子序数,则下列说法正确的是
A.原子半径:X>Y>Z>W
B.W和X形成的某种化合物中,可能既有离子键,又有共价键
C.单质的氧化性:Y<Z
D.简单氢化物的稳定性:X<Y<Z
难度: 中等查看答案及解析
-
为测定某碘水(其溶质为I2)中碘单质的浓度,取该碘水10.00mL,加入淀粉溶液作为指示剂,用0.01 mol·L-1 Na2S2O3滴定此碘水,当溶液由蓝色变为无色时,消耗Na2S2O3的体积为20.00 m1。已知Na2S2O3被氧化为Na2SO4,则碘单质的浓度为
A.0.08 mol·L-1 B.0.16 mol·L-1 C.0.04 mol·L-1 D.0.06 mol·L-1
难度: 中等查看答案及解析
-
将mg铜粉和锌粉的混合物分成两等份,将其中一份加入200mL的稀硝酸中并加热,固体和硝酸恰好完全反应,并产生标准状况下的NO2.24L(标准状况下);将另一份在空气中充分加热,的到n g固体,将所得固体溶于上述稀硝酸,消耗硝酸的体积为V ml。下列说法不正确的是
A.V=150Ml
B.硝酸的浓度为2 mol·L-1
C.m g铜粉和锌粉的物质的量之和为0.3 mol
D.n=m+2.4
难度: 困难查看答案及解析