-
化学家戴维最早制得了曾用作麻醉剂的笑气(化学式为N2O),其中氮元素的化合价是( )
A. -1 B. -2 C. +1 D. +5
难度: 简单查看答案及解析
-
“绿水青山就是金山银山”,说的是自然环境与人们的生活关系密切,倡导大家要爱护自然环境。下列做法符合这一理念的是
A. 农业上为增加农作物产量,可以大量施用化肥农药
B. 任意排放工业产生的废气、废水、废渣
C. 大量植树造林,严禁乱砍滥伐森林
D. 采取就地掩埋的方法来处理各种生活垃圾
难度: 中等查看答案及解析
-
下列说法中正确的是( )
A. 所有原子的原子核一定是由质子和中子构成
B. 在同一种物质中同种元素的化合价可能不相同
C. 具有相同质子数的粒子一定是同一种元素
D. 分子、原子都是不显电性的粒子,所以构成物质的粒子一定不显电性
难度: 简单查看答案及解析
-
在一密闭容器内有氧气、二氧化碳、水和一种未知物质M,在一定条件下充分反应,测知反应前后各物质的质量如下:
物质
氧气
二氧化碳
水
M
反应前质量/g
132
2
2
32
反应后质量/g
4
90
74
x
下列说法正确的是
A.x应为64
B.M中一定不含氧元素
C.该反应是分解反应
D.M的化学式为C2H5OH
难度: 简单查看答案及解析
-
下列空气中各成分与其用途不对应的是( )
A.稀有气体的性质稳定﹣﹣作保护气
B.氧气难溶于水﹣﹣用于急救病人
C.干冰容易升华吸热﹣﹣用于人工降雨
D.氮气不活泼﹣﹣用于食品防腐
难度: 简单查看答案及解析
-
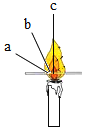
下列物质在氧气中燃烧,实验现象和反应类型正确的是( )
A.硫—淡蓝色火焰—化合反应 B.红磷—大量白雾—氧化反应
C.蜡烛—黄色火焰—分解反应 D.细铁丝—火星四射—化合反应
难度: 中等查看答案及解析
-
下列有关实验现象的描述,错误的是()。
A.细铁丝在氧气中剧烈燃烧,火星四射,生成黑色固体
B.分别点燃一小块棉纤维和羊毛纤维,都产生烧焦羽毛的气味
C.红磷在空气中燃烧,产生大量白烟
D.一氧化碳高温还原氧化铁时,红棕色粉末逐渐变成黑色
难度: 简单查看答案及解析
-
运用推理、归纳、类比、对比的方法得出下列结论,其中合理的是( )
A.水沸腾时可冲起壶盖,说明温度升高分子会变大
B.水和过氧化氢的组成元素相同,则两者的化学性质相同
C.同温下分解氯酸钾,加催化剂的反应速率快,说明催化剂可以改变反应速率
D.Na+、Cl﹣的最外层电子数均为8,由此得出离子的最外层电子数均为8
难度: 中等查看答案及解析
-
现将X、Y两种金属片分别插入硫酸铜溶液中,X无明显变化,Y表面有铜析出,则X、Y、Cu三种金属的活动性由强到弱的顺序是
A.X > Y > Cu B.Cu > X > Y
C.Y > Cu > X D.X > Cu > Y
难度: 简单查看答案及解析
-
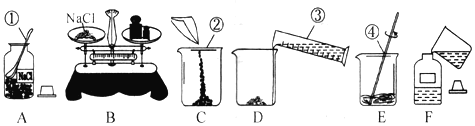
为准确配制80g10%的氯化钠溶液,要尽量减小计量仪器称量时的误差。该实验用到了下列仪器,其中属于计量仪器的是
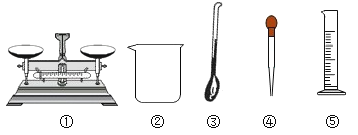
A.①⑤ B.③④⑤ C.①③④⑤ D.①②③④⑤
难度: 简单查看答案及解析
-
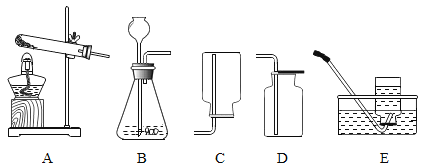
下图所示实验操作中,正确的是( )
A. 量取液体
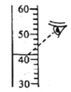 B. 检查装置的气密性
B. 检查装置的气密性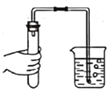
C. 加热液体
 D. 倾倒液体
D. 倾倒液体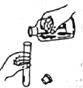
难度: 简单查看答案及解析